
2025年02月14日,FDA批准Sanofi-Aventis U.S. LLC的 Merilog(insulin-aspart-szjj)作为 Novolog(门冬胰岛素)的生物仿制药,用于改善成人和儿童糖尿病患者的血糖控制。Merilog 是一种速效人胰岛素类似物,是FDA批准的首款速效胰岛素生物仿制药。作为一种速效胰岛素,Merilog有助于降低进餐时血糖飙升,从而改善糖尿病患者的血糖控制。剂量及规格批准包含3 ml单患者使用的预装注射笔和10 ml多剂量西林瓶。
胰岛素是一种由胰腺产生的激素,可帮助葡萄糖进入人体细胞以用作能量。患有糖尿病时,胰腺无法产生足够的胰岛素来将血糖水平保持在正常范围内,这可能导致患者出现严重的健康问题。速效胰岛素(如门冬胰岛素)对于控制餐后血糖峰值至关重要,因此这项批准对餐时血糖控制尤其重要。
本次批准基于以下临床研究:
(1)1型糖尿病成人患者:
开展了两项为期24周、开放标签、活性药物对照的研究,以比较门冬胰岛素与常规人胰岛素注射液在成年1型糖尿病患者中的安全性和有效性。由于这两项研究的设计和结果相似,此处仅展示其中一项研究的数据(见下表)。
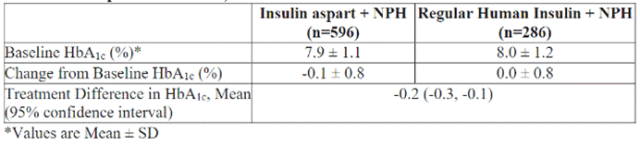
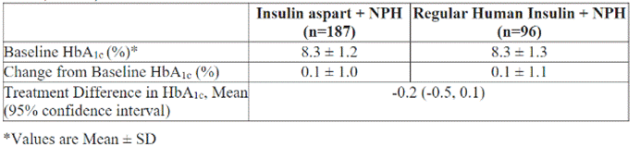
(2)1型糖尿病儿科患者:基于一项针对1型糖尿病儿科患者的正规人胰岛素充分且对照良好的试验(见下表)。这项为期24周、针对283名6至18岁1型糖尿病儿科患者的平行组研究,比较了两种皮下多次给药治疗方案:门冬胰岛素(n = 187)或正规人胰岛素(n = 96)。中性鱼精蛋白锌胰岛素(NPH胰岛素)作为基础胰岛素使用。两个治疗组在糖化血红蛋白(HbA1c)方面观察到相似的效果。
研究还对26名2至6岁的1型糖尿病儿科患者进行了皮下注射门冬胰岛素和正规人胰岛素的比较,发现二者对HbA1c的影响相似。
(3)成人 2 型糖尿病患者皮下注射的临床研究:
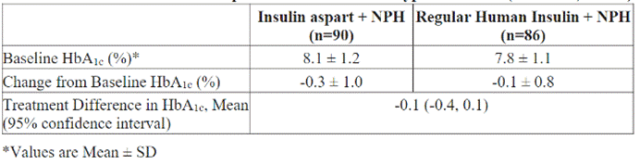
开展了一项为期6个月、开放标签、活性药物对照的研究,以比较门冬胰岛素与常规人胰岛素在2型糖尿病患者中的安全性和有效性(见下表)。
试验人群的平均年龄为56.6岁,糖尿病平均病程为12.7年。63%为男性。76%为白种人,9%为黑人,15%为其他种族。平均体重指数(BMI)约为29.7kg/m2。
门冬胰岛素在餐前即刻进行皮下注射,而常规人胰岛素在餐前30分钟皮下注射。中性鱼精蛋白锌胰岛素(NPH胰岛素)作为基础胰岛素,每日可单次给药或分次给药。两种治疗方案在糖化血红蛋白(HbA1c)的变化上相近。
与Novolog一样,Merilog应在用餐开始前5到10分钟内给药。Merilog通过注射到胃、臀部、大腿或上臂进行皮下(皮下)给药。Merilog的剂量应个体化,并根据患者的需要进行调整。
Merilog可能会引起严重的副作用,包括低血糖症(低血糖)、严重的过敏反应和低钾血症(血液中的低钾)。其他常见的副作用可能包括注射部位反应、瘙痒、皮疹、脂肪代谢障碍(注射部位皮肤增厚或凹陷)、体重增加和手脚肿胀。
生物仿制药也是一种生物制品,与FDA批准的生物制品(也称为参比品)高度相似,且没有临床意义的差异。患者可以预期生物仿制药的安全性和有效性与参比产品相同。迄今为止,FDA已批准65种生物仿制药产品用于治疗各类疾病健康。生物仿制药以更低的成本增加获得安全、有效和高质量药物的机会仍然是各国药监部门的持续优先事项,使得患者能有更多的治疗选择。
“对于数百万依赖每天注射胰岛素来治疗糖尿病的人来说,为他们的速效胰岛素注射提供生物仿制药选择确实可以产生影响,因为生物仿制药有可能增加获得这些救命药物的机会,”FDA CDER治疗性生物制品和生物仿制药办公室主任Sarah Yim医学博士说道。此项批准标志着朝着确保所有需要胰岛素等基本药物的人都能获得和负担得起迈出了积极的一步。
参考来源:FDA官网
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论