
如果把药物研发比作一场马拉松,那么早期工艺开发就是决定选手能否顺利通过第一个补给站的关键赛段。
在过去,这可能仅仅是大型制药公司内部的一个按部就班的环节。但如今,商业环境和监管格局早已发生了翻天覆地的变化。研发成本的飙升像一把悬在头顶的达摩克利斯之剑,迫使药企必须以更少的资源做更多的事。
我们看到了一种明显的趋势:传统的“大包大揽”模式正在瓦解,取而代之的是更加灵活的内外部整合模式。新兴市场的合同研究机构(CRO)和合同制造机构(CMO)正在崛起,它们像毛细血管一样渗透进药物开发的每一个环节。无论是依靠内部深厚的技术积累,还是借助外部的制造能力,核心目标只有一个:在保证质量的前提下,通过速度和效率的极致优化,降低总体拥有成本。
本文我们将聚焦于原料药(活性药物成分,API)的早期工艺开发——这个连接“科学发现”与“临床验证”的桥梁,看看它是如何运作的。
一、什么是“早期工艺开发”?
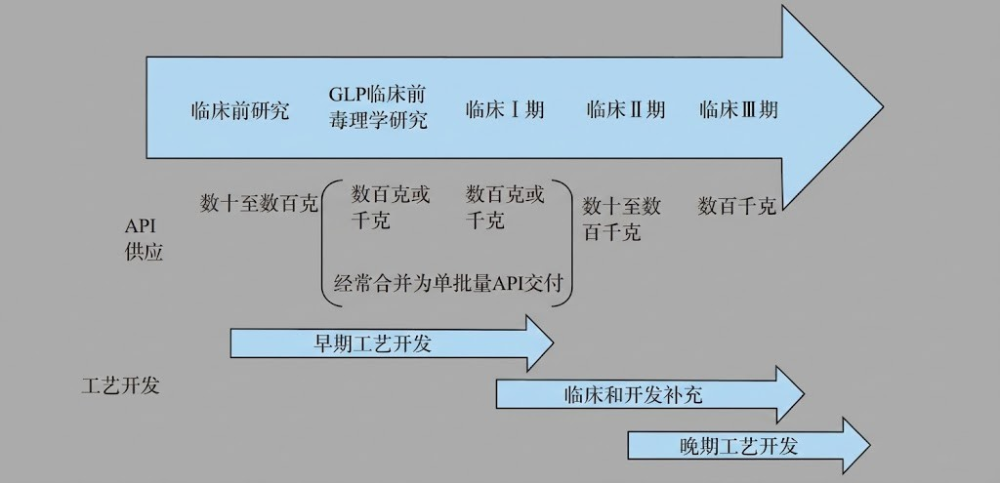
在这一语境下,“早期”并非指时间的绝对早晚,而是指药物生命周期中的特定阶段。具体来说,它是指从为满足GLP(药物非临床研究质量管理规范)毒理学研究提供API开始,直到交付足以支持I期临床试验的大量API为止。
这一阶段的任务极其艰巨,因为数量级的跨越是惊人的:
- 临床前研究:可能只需要数十至数百克。
- GLP毒理学研究:需求激增至数百克甚至数千克。
- I期临床:同样需要数百克或千克级。
更有趣的是,为了效率,我们经常会将GLP毒理学研究和I期临床的API需求合并为一个批次进行生产。这意味着,工艺化学家必须在很短的时间内,拿出一个能从实验室玻璃瓶无缝切换到“千克级实验室”大设备的工艺路线。实验室里那种精雕细琢的小规模合成,到了大釜里可能完全行不通,这就是早期开发的魅力与挑战所在。
标准药物申请途径的典型API供应数量和工艺开发阶段
二、驱动早期开发的铁律
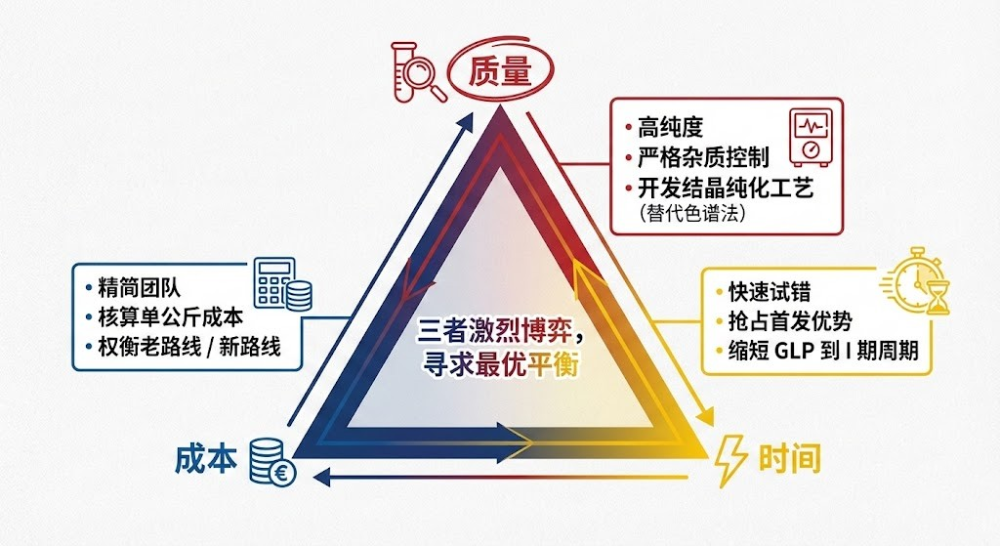
在任何项目管理中,我们都熟悉“质量、时间、成本”这个不可能三角。在API早期开发中,这三者的博弈尤为激烈。
1. 质量:不可逾越的红线
无论开发阶段多早,最终产品是要进入人体(或模拟人体的毒理实验)的。因此,患者的安全永远不能向工艺妥协。
- 纯度要求:必须足够高。
- 杂质控制:不仅要控制一般杂质,更要严防死守起始原料带入的杂质和工艺杂质。
- 纯化策略:这是早期开发的重头戏。虽然色谱法(过柱子)在实验室很常用,但在放大量级时,它的成本高且效率低。因此,开发出高效的结晶纯化工艺,往往被视为工艺成熟的标志。
2. 速度:唯快不破
制药行业是残酷的竞技场。针对同一个治疗靶点,往往有数家甚至数十家公司在赛跑。“首发优势”(First-in-class)带来的经济效益是惊人的。
- 快速试错:早期临床研究(如PK/PD数据)能让我们窥探候选药物的潜力。毕竟,即便在这个阶段,药物获批的成功率依然低于10%。
- 资源最大化:只有尽快完成GLP毒理研究,才能拿到开启I期临床的钥匙。没有API,一切研究都要停摆。缩短这个周期,就是为整个项目争取生命。
3. 成本:戴着镣铐跳舞
早期开发团队通常很精简,可能只有1-2名化学家。他们必须在有限的预算和人力下,计算出“单公斤合成成本”。 这里面临一个经典的决策困境:是沿用药物发现阶段的老路线,还是重新设计一条新路线?
- 老路线:虽然熟悉,但可能是为了合成微量样品设计的,放大风险极高,成本昂贵。
- 新路线:效率高,但开发新路线需要时间。化学家必须权衡:如果现有路线放大风险太大,或者新路线能显著减少步骤、节约时间,那么推倒重来才是最经济的选择。
三、关键转折点:从“发现”到“开发”的交接棒
当药物发现团队敲定候选分子时,接力棒就被递交给了工艺开发团队。这个交接点,通常发生在为GLP毒理学研究准备数百克API的前夕。
1. 为什么不能直接用发现阶段的工艺?
这涉及到一个根本性的思维差异。药物发现化学家的目标是“多快好省地合成少量、多样的分子”,只要能拿到几毫克做测试,用什么昂贵的试剂、跑多少次柱子都无所谓。而工艺化学家的目标是“稳定、安全、低成本地生产大量单一产品”。
2. 实战案例:铃木偶联(Suzuki) vs 熊田偶联(Kumada)
我们来看看这两个例子,展示了两种思维的碰撞:
药物发现的选择(Suzuki-Miyaura偶联):
Suzuki-Miyaura Cross-Coupling反应机理
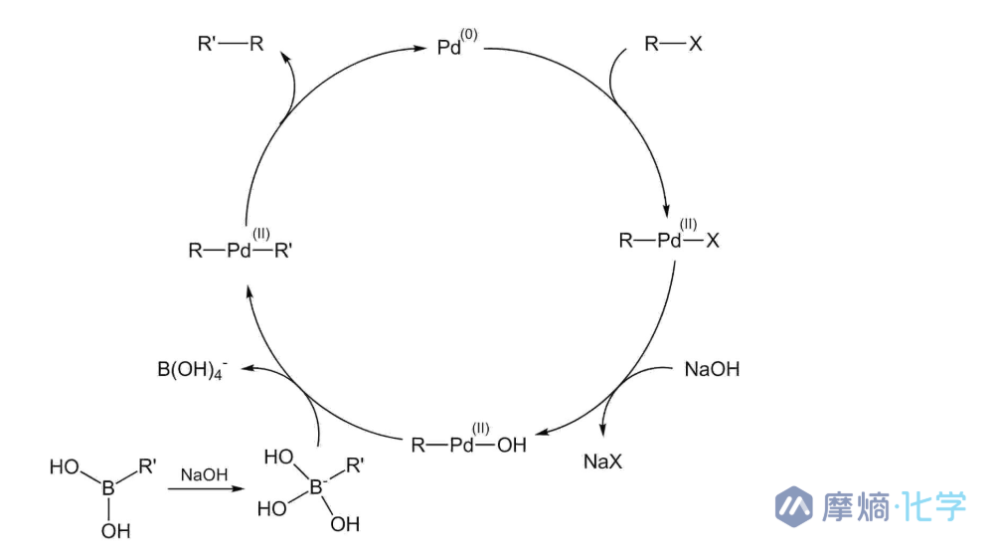
- 优点:反应成功率极高,硼酸试剂稳定且易得,非常适合构建化合物库。
- 缺点(放大时):需要用到钯(Palladium)催化剂。钯是贵金属,且有毒,必须在API中清除到ppm(百万分之一)级别。此外,硼酸衍生物本身往往有潜在的遗传毒性(Ames阳性),若残留在最终产品中,必须控制在极低的毒性阈值(TTC)之下。
工艺开发的选择(Kumada偶联):
Kumada Cross-Coupling反应机理
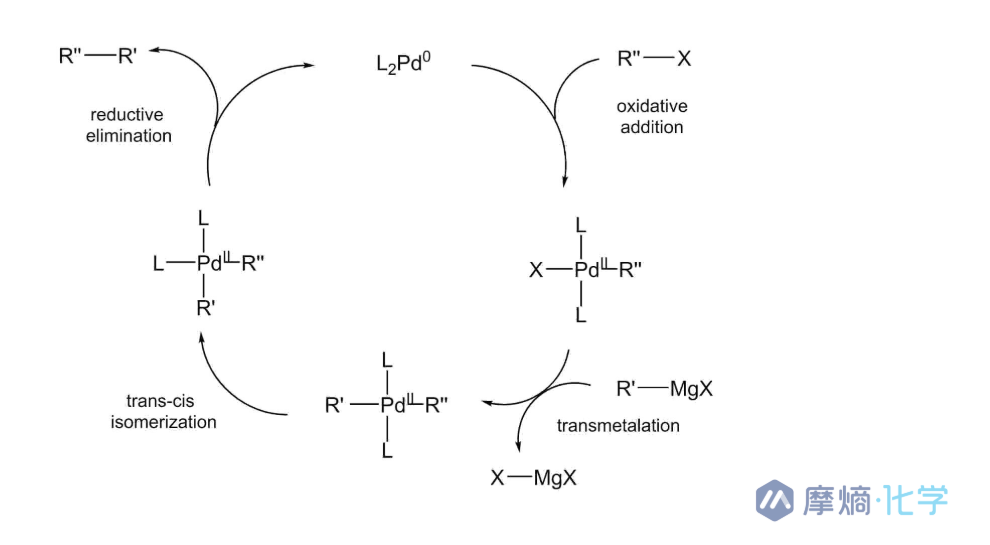
- 策略:使用铁(Fe)催化剂和格氏试剂。
- 优点:铁和试剂都无毒、便宜。更重要的是,它减少了合成步骤(不需要像制备硼酸那样多一步),直接由前体原位制备。
- 结论:虽然Kumada反应在小规模筛选时不如Suzuki方便,但在工业化生产中,它是更优解。
3. 不同的合作模式
为了平滑这个过渡,各家药企有不同的打法:
- 顾问模式:工艺化学家在早期介入,给发现团队当顾问。
- 混合团队(如辉瑞模式):成立“合成管理团队(SMT)”,由发现和工艺部门的人员共同组成,专门负责攻克首批GLP和FIH(首次人体)物料的供应,这种跨学科团队能极大加速靶点验证的过程。
四、排兵布阵:现代工艺开发组织的解剖
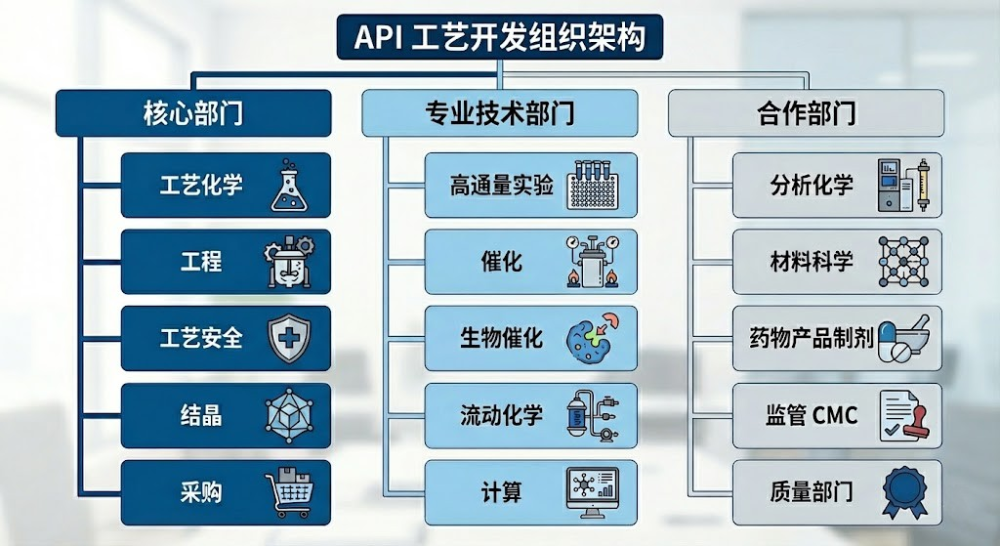
一个成熟的API工艺开发组织,不再是几个化学家在实验室里单打独斗,而是一个精密咬合的齿轮组。我们可以将其分为三个层级:核心部门、专业技术部门、合作部门。
1. 核心部门
这是作战的主力部队。
工艺化学家:项目的总指挥。他们必须具备敏锐的风险嗅觉。比如,起始原料突然变了,杂质谱不一样了,或者放大后出现了不可预见的副产物,他们必须像拆弹专家一样迅速解决问题。
工程师:这是化学家的物理外脑。当反应从烧瓶放大到反应釜,传热和传质会发生剧变。工程师通过简单的实验(如搅拌效率测试、放热测试)来预防“炸釜”或反应不完全的风险。
工艺安全:安全是底线。DSC(差示扫描量热法)是标配,用于检测放热风险。到了大生产,还需要更高级的热检测装置(TSU)来确保反应不会失控。
结晶团队:虽然他们通常服务于后期项目,但在早期,他们能帮助化学家摆脱对色谱柱的依赖,设计出能除杂的结晶工艺。
采购部门:在早期开发中,“买”往往比“做”更重要。采购部门负责寻找高质量的中间体供应商(尤其是亚洲的低成本供应商)。但这并非大海捞针,借助摩熵医药(原料药专版)的全球供应链数据,采购人员可以快速筛选出具备合规资质与产能匹配的供应商,从而规避供应链风险。毕竟,如果供应商掉链子(延期或质量不合格),整个项目都会瘫痪。
2. 专业技术部门
这些是“特种部队”,拥有高精尖武器,能解决常规手段无法解决的问题。
高通量实验(HTE):这是现代化学的“加特林机枪”。以前一个个试反应条件,现在HTE平台可以在几毫克级别上,一次性筛选数百种条件。这对于物料极其珍贵的早期开发来说,简直是神器。
催化中心:专注于加氢、高压反应。这些反应往往涉及易燃易爆气体(如氢气),需要专门的设备和受过特训的人员。
生物催化:利用酶来进行反应。虽然早期开发很难进行基因工程改造酶,但使用现成的脂肪酶、酮还原酶等,往往能实现化学法难以做到的高选择性转化。
流动化学:从“批处理”走向“连续流”。对于那些危险的、不稳定的中间体,或者传统釜式反应无法扩大的工艺,流动化学提供了全新的解决方案。它还能让过程控制(PAT)变得更容易。
计算化学:利用计算机模拟(In silico)预测反应路径、pKa值、晶型稳定性等,为实验指明方向,减少盲目试错。
3. 合作部门
分析化学:没有他们开发的高精度方法(UPLC/MS, NMR),化学家就是瞎子,无法看到ppm级别的基因毒性杂质。
监管CMC:负责撰写IND(新药临床试验申请)文件,确保所有数据符合法规要求。
质量部门(QA):确保生产过程符合GMP要求,最终放行产品用于临床。
五、硬件革命:工欲善其事,必先利其器
早期的工艺实验室里,圆底烧瓶和旋转蒸发仪是主角。但现在,实验室设备经历了一场数字化革命。
1. 自动化反应器
现在的实验室更倾向于使用自动化夹套反应器(如Mettler Toledo的EasyMax等)。
- 优势:它们能精确控制温度、搅拌速度和加料速率。这不仅仅是方便,更是为了模拟大生产环境。在实验室里就能复现大釜中的混合和热分布情况,大大降低了放大失败的概率。
2. 过程分析技术(PAT)
以前我们得从反应瓶里取样去测HPLC,现在我们将探头直接插入反应液中。
典型PAT过程控制前馈/反馈系统示意图
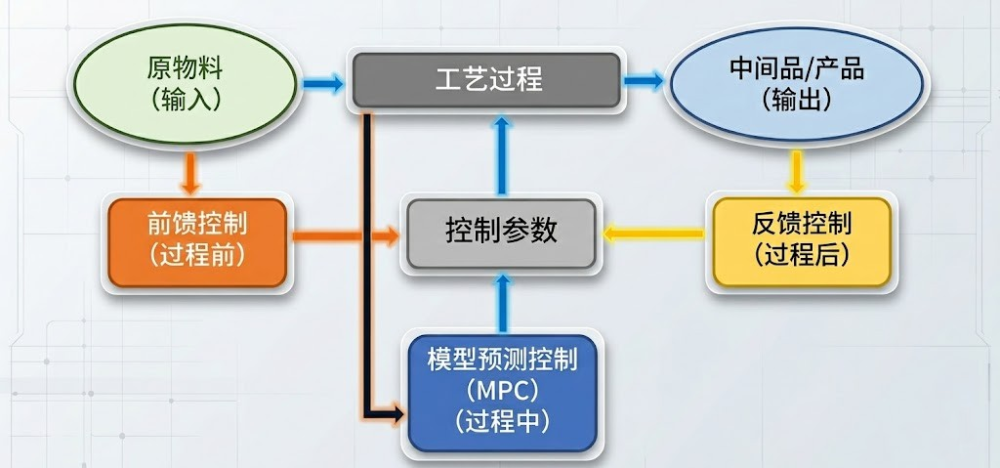
原位红外(ReactIR)/拉曼光谱:实时监控反应进程,看原料怎么消失,产物怎么生成。
聚焦光束反射测量(FBRM):这是结晶的神器,能实时监测颗粒的粒径变化,告诉我们晶体是在生长还是在破碎。
六、监管的高墙:GMP与物料控制
当API用于人体临床试验时,游戏规则就变了。虽然GLP毒理物料不需要完全遵循cGMP(现行药品生产质量管理规范),但FIH物料必须严格合规。
ICH Q7指南:这是全球公认的API生产圣经。特别是第19节,专门针对临床试验用API的生产。它强调控制工艺应与药物开发的阶段相适应——即“阶段适应性GMP”。
物料分级:
- 常规化学品:目录试剂,买来就能用。
- 特定中间体:通常是Pre-GMP(非GMP)级别,可以外包给CMO生产,这有助于降低成本和加快速度。但必须保证其质量不会污染最终API。
- API及最后几步:必须在符合cGMP的车间内,由受过培训的人员,按照严格的文件体系进行生产。
七、结语
早期工艺开发是一个充满活力但也充满矛盾的领域。它要在极其有限的时间和物料资源下,通过快速的技术迭代,交付高质量的产品。
一个成功的早期工艺开发团队,不仅仅是一群合成高手的集合,更是一个集成了工程、安全、分析、法规和供应链管理的有机生命体。在这个阶段,化学家们不仅是在合成一个分子,更是在为这个分子未来的商业化命运铺设第一块基石。通过引入高通量筛选、流动化学和数字化工具,我们正在将这一过程从传统的“经验主义”推向精准的“科学工程”。
对于制药人来说,没有什么比看着自己亲手放大的几公斤白色粉末,被装入药瓶,最终走向临床去治愈患者更令人激动的了。这就是早期工艺开发的终极价值。
扩展阅读:
1. 摩熵·原料药 https://api.bcpmdata.com/
2. 药物研发“幕后英雄”:动物模型有效性大揭秘,同源、同构与预测性模型全解析
3. 生物技术革命简史:重组DNA、基因泰克与人类基因组计划如何催生千亿美元抗体药物市场
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论