
慢性乙型肝炎(CHB)长期被视为“只能控制、难以治愈”的疾病。2025年11月,在美国肝病学会年会(AASLD 2025)上,南方医科大学南方医院侯金林教授团队公布的 HT-101注射液 联合 HT-102注射液 的Ib/IIa期临床数据,为这一困境带来了突破性希望:联合治疗组在第20周HBsAg清除率最高达到90%,刷新了乙肝功能性治愈纪录,标志着慢乙肝治疗从“长期抑制”向“功能性治愈”迈出了关键一步。
一、HT-101/HT-102注射液:双机制协同,实现“抑制+清除”闭环
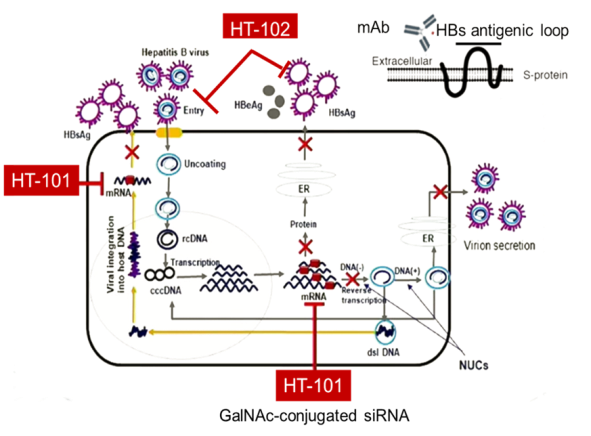
HT-101是 苏州星曜坤泽生物制药 开发的一款GalNAc偶联小干扰RNA(siRNA),它能精准进入肝细胞,沉默所有乙肝病毒转录本(包括来自cccDNA和整合DNA的mRNA),从源头抑制HBsAg等病毒蛋白的合成。
HT-102(BM-012)则是一款全人源中和抗体,它能高效捕获并清除血液循环中已存在的HBsAg和亚病毒颗粒,减轻其对宿主免疫系统的抑制,帮助机体重建抗病毒免疫应答。
二者联用形成了“源头抑制病毒产生+外周快速清除抗原”的双重打击模式。这不仅实现了HBsAg的快速深度下降,还可能为恢复免疫系统功能创造关键窗口,是追求持久功能性治愈的科学策略。
二、突破性临床数据:刷新治愈纪录的“中国方案”
该研究是一项随机、多中心的Ib/IIa期临床试验(NCT07183306),共纳入56例NUC长期抑制下的HBeAg阴性慢性乙肝患者,受试者基线HBsAg在100~3000 IU/mL之间,HBV DNA<100 IU/mL,分为5组接受不同治疗方案,受试者每月给药1次,治疗24周,后续进行长期随访。停药标准为达到“完全应答”(CR),即HBsAg降至检测不到水平(<0.05 IU/mL)且HBV DNA持续阴性。
试验结果显示,联合治疗组在HBsAg清除率方面表现出显著优势。在第24周时,联合治疗组的总应答率达到79%(22/28例),其中高剂量联合治疗组(E组,HT-101 400 mg+HT-102 300 mg)的HBsAg清除率最高,在第20周时已有90%的患者实现了HBsAg清除。更为突出的是,该组中有20%的患者在治疗开始后仅4周就实现了HBsAg清除。
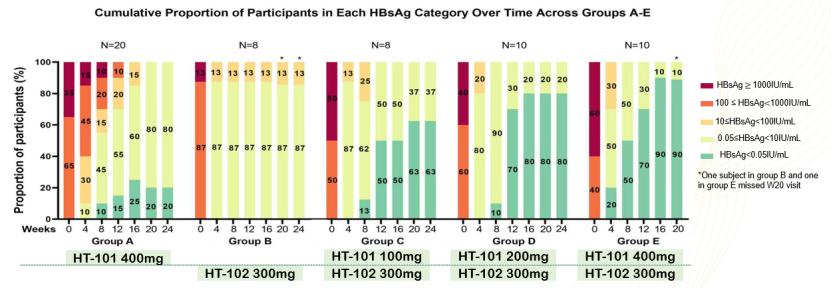
相比之下,单药治疗组的HBsAg清除率明显较低:HT-101 单药组在24周时的HBsAg清除率为21.4%,HT-102 单药组为33.3%。从HBsAg水平的降低幅度来看,联合治疗组的效果同样优于单药组。
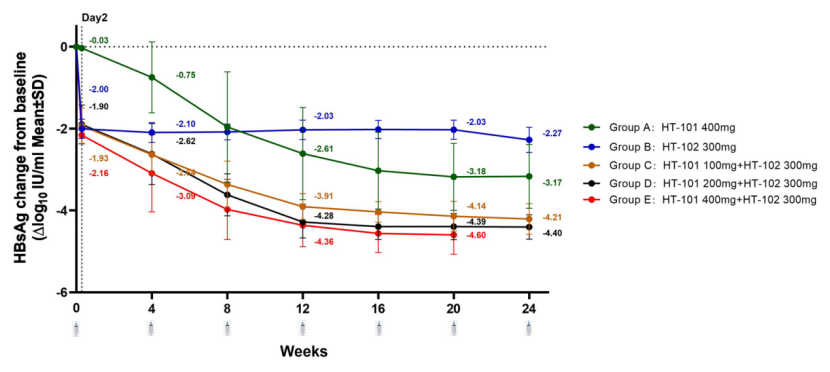
研究中还观察到,基线HBsAg水平与清除率密切相关:基线HBsAg低于1000 IU/mL的患者在第20周时的清除率达100%,而基线HBsAg≥1000 IU/mL的患者清除率为57%。这表明较低的初始病毒抗原水平可能预示着更好的疗效。
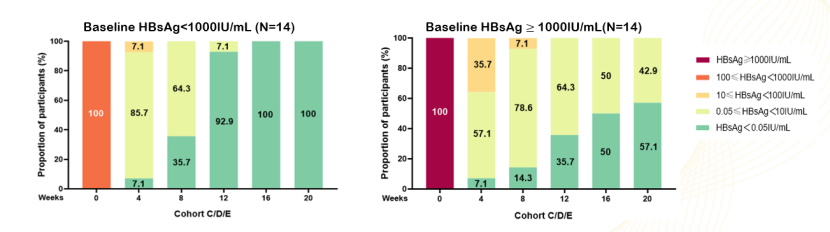
此外,所有患者均顺利完成了治疗,没有因不良反应而停药,也未发生3级及以上严重不良事件。主要不良事件为轻度的注射部位红肿,通常可自行缓解;肝功能和肾功能指标在治疗前后保持稳定,未出现与药物相关的严重不良事件。总体而言,HT-101联合HT-102治疗表现出良好的安全性和耐受性。
摩熵医药数据库显示,基于这一优异的临床数据,HT-101 与 HT-102 于2025年9月23日被CDE正式纳入“突破性治疗品种”,并于2026年1月19日获得美国FDA批准开展II期临床试验,拟用于慢性乙型肝炎治疗。
三、乙肝治疗药物市场:未满足的临床需求与巨大商业潜力
根据世界卫生组织(WHO)发布的《2024年全球肝炎报告》,截至2022年,全球慢性HBV感染者约为2.54亿,其中中国慢性感染者约8600万,慢性乙肝患者达2000-3000万例。尽管患者基数庞大,但诊断率和治疗率分别仅为22%和15%,凸显出显著的“诊疗鸿沟”。
目前,乙肝的标准治疗方案主要包括核苷(酸)类似物(NAs)和干扰素(IFN),但两者均存在明显局限性。摩熵医药数据库显示,国内已有5款一线核苷(酸)类原研药物获批上市,包括百时美施贵宝的 恩替卡韦(ETV)、吉利德的 富马酸替诺福韦二吡呋酯(TDF)和 丙酚替诺福韦(TAF)、豪森药业的 艾米替诺福韦(TMF),以及西安新通药物的 甲磺酸普雷福韦,且均已纳入国家医保目录。
在干扰素方面,长效产品为主流。由于罗氏与歌礼制药终止了 派罗欣 在中国大陆的推广合作,目前市场基本由特宝生物的 聚乙二醇干扰素α-2b(派格宾)一家独大。
聚乙二醇干扰素α-2b医院终端销售竞争格局
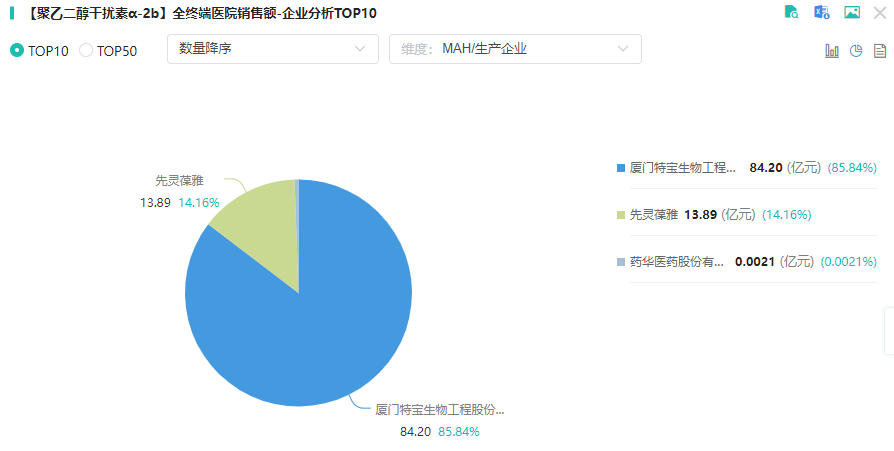
查数据,找摩熵!图源:摩熵医药-全终端医院销售数据库
核苷类似物虽能强效抑制病毒DNA复制,但对HBsAg的清除率极低(0-3%),且需终身服药,给患者带来沉重的心理和生理负担。干扰素的HBsAg清除率略高(3%-11%),但副作用明显(如流感样症状、骨髓抑制等),且需注射给药,导致患者依从性差。
即便采用NAs联合干扰素的优化方案,HBsAg清除率也仅能提升至接近30%(部分优势患者可达80%),仍远不能满足临床需求。这种“高患病率与低治愈率”并存的现状,催生了庞大的创新药物市场空间。据弗若斯特沙利文预测,随着创新药物上市,中国乙肝药物市场规模预计到2030年将达到723亿元。
四、全球竞争格局:多技术路线并行,中国药企强势抢滩
当前乙肝新药研发呈现“多技术路线并进、联合用药成主流”的竞争格局。针对HBV生命周期不同环节,全球药企在衣壳抑制剂、反义寡核苷酸(ASO)、小干扰RNA(siRNA)、HBsAg抑制剂、治疗性疫苗及细胞疗法等领域全面布局。
随着国内创新药研发能力的提升,目前中国药企在乙肝治疗创新领域的布局已日益完善,形成了以广生堂、星曜坤泽、恒瑞医药、腾盛博药、东阳光药等为代表的企业矩阵,且在多个治疗路径中均已占据领先身位。
1. siRNA赛道:疗效突出,国内企业表现亮眼
siRNA疗法可抑制HBV抗原表达,阻断病毒复制,减轻免疫耐受,还能抑制来自整合HBV-DNA和cccDNA的HBsAg,是实现乙肝功能性治愈的核心技术路线之一。据摩熵医药数据库显示,目前全球尚无乙肝siRNA药物获批上市,已进入临床阶段的管线包括Vir Biotechnology的 VIR-2218(elebsiran/BRII-835,II期临床)、GSK的 GSK5637608(JNJ-3989,II期临床)、Arbutus Biopharma的 AB-729(imdusiran,II期临床)等国外管线,以及国内星曜坤泽 HT-101、瑞博生物 RBD1016(II期临床)、恒瑞医药 HRS-5635等。
其中,星曜坤泽的 HT-101 凭借联合 HT-102 的优异临床数据,成为国内siRNA赛道的领军者,其90%的HBsAg清除率在目前全球siRNA和ASO产品中处于前列;恒瑞医药的 HRS-5635 是新型共价偶联三触角型GalNAc的双链小干扰RNA,单药II期研究显示其具备良好的功能性治愈潜力,目前正在开展联合 聚乙二醇干扰素α(Peg-IFNα)的II期研究;腾盛博药从Vir Biotechnology引进的 VIR-2218,联合 Peg-IFNα 治疗HBV显示出优异的HBsAg清除率,目前处于II期临床。
HRS-5635注射液(CTR20241805)临床试验信息(部分)
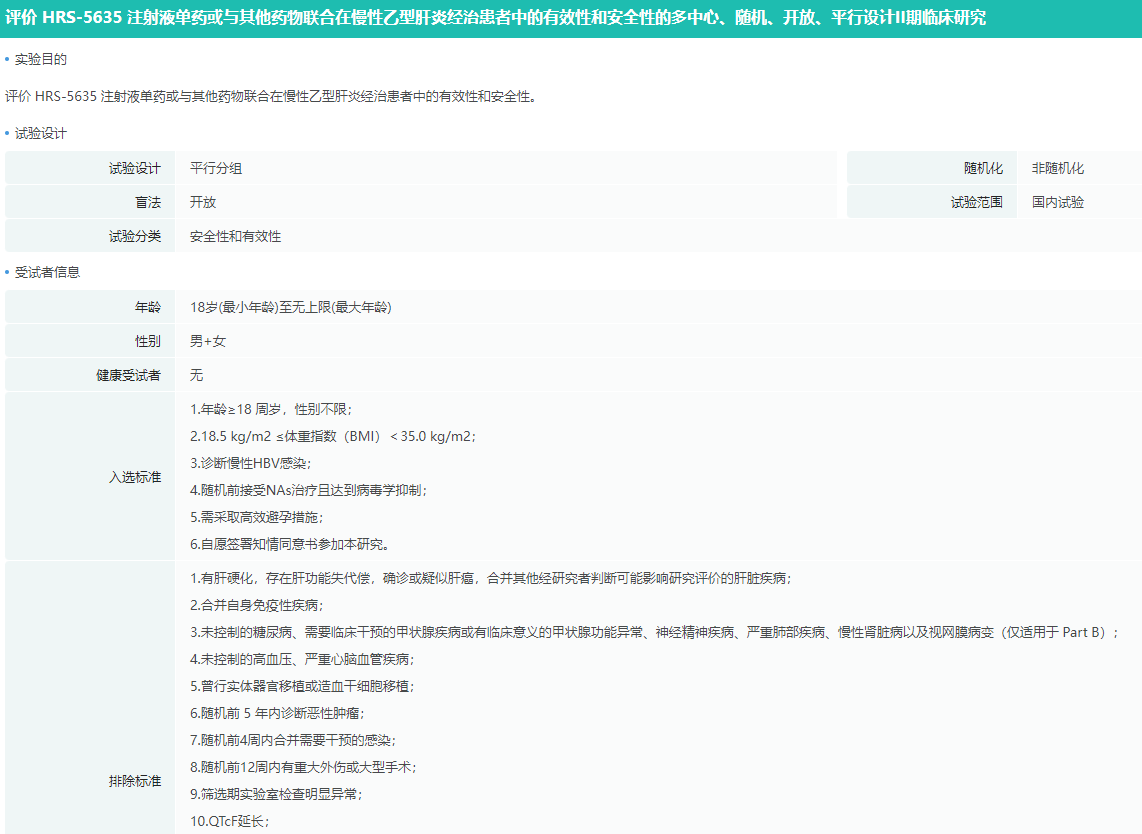
查数据,找摩熵!图源:摩熵医药-中国临床试验数据库
2. ASO赛道:进度领先,有望率先实现上市突破
ASO药物通过碱基互补配对原则,与乙肝病毒的mRNA或其他关键RNA序列结合,影响cccDNA的转录过程,让cccDNA处于“沉默”状态,从而实现乙肝功能性治愈。目前全球进度最快的ASO药物是Ionis Pharmaceuticals开发并授权葛兰素史克(GSK)的 Bepirovirsen(GSK836/IONIS-HBVRx),该药物已宣布III期成功,有望成为全球首个“功能性治愈”慢性乙型肝炎的药物,预计2026年第一季度向美国、欧盟、中国等提交上市申请,目前日本已受理 bepirovirsen 的新药申请(NDA)。此外,浩博医药的非偶联型ASO药物 AHB-137 也处于临床III期阶段。
3. 衣壳抑制剂赛道:口服优势明显,国内企业接近临床终点
衣壳自组装是病毒生命周期的关键步骤且具有极强的保守性,衣壳抑制剂可干扰HBV衣壳组装,从而强烈抑制HBV复制及成熟病毒颗粒的产生,具备口服给药、耐受性好等优势。目前已进入临床阶段的管线包括东阳光药的 甲磺酸莫非赛定(GLS4)、广生堂的 GST-HG141(奈瑞可韦)、挚盟医药的 ZM-H1505R(Canocapavir,科诺卡帕韦)、Aligos Therapeutics的 ALG-000184 等,其中前三者均已进入临床III期阶段,距离上市仅一步之遥。
国内企业中,广生堂的 GST-HG141(奈瑞可韦)是新型口服乙肝病毒核心蛋白调节剂,可针对乙肝病毒复制的多个关键环节发挥作用,既能抑制衣壳组装,又能阻断HBV在肝细胞核脱壳,从而耗竭cccDNA储备池,其Ib期和II期临床结果显示,该药物安全性良好,具有优异的HBV DNA和pgRNA抑制效果,已被纳入突破性治疗品种;东阳光药的 甲磺酸莫非赛定(GLS4)是核心蛋白变构调节剂(CpAM),其改良产品 福瑞赛定(Freethiadine)也处于II期阶段;Aligos Therapeutics的 ALG-000184 是泛基因型II型衣壳组装调节剂,II期研究显示,300mg单药治疗96周可实现持续、显著的HBV DNA抑制,且无病毒突破。
4. 其他赛道:多点布局,补充治愈路径
除上述三大核心赛道外,HBsAg抑制剂、治疗性疫苗、细胞疗法等也在快速发展,成为乙肝功能性治愈的重要补充。HBsAg抑制剂主要通过阻断HBsAg和亚病毒颗粒的释放控制HBV复制,目前已进入临床阶段的包括Replicor的 REP2139/REP2165、广生堂的 GST-HG131 和 GST-HG121 等,其中广生堂的 GST-HG131 是全球首个完成II期临床研究的口服HBsAg抑制剂,12周可使患者血清表面抗原平均下降0.9log IU/ml,76.5%的患者表面抗原水平降至100IU/ml以下,目前正在开展联合GST-HG141的II期研究。
治疗性疫苗方面,腾盛博药从VBI Vaccines引进的 BRII-179(VBI-2601)处于II期临床,其II期研究显示,抗-HBs应答者HBsAg下降速度更快、幅度更大,有望缩短PEG-IFNα治疗周期;细胞疗法方面,星汉德生物的HBV特异性TCR-T细胞疗法 SCG101 表现亮眼,2025年EASL大会公布的数据显示,单次输注后,94%的患者HBsAg在28天内降幅达1.0-4.6log,23.5%的患者实现HBsAg完全清除,且随访一年持续维持清除状态,展现出抗病毒和抗肿瘤双重效果。
BRII-179(VBI-2601)全球临床试验信息查询

查数据,找摩熵!图源:摩熵医药-全球临床试验数据库
五、结语:乙肝功能性治愈时代的前夜
HT-101注射液 及其联合疗法的突破性进展,为2.54亿全球慢乙肝患者带来了前所未有的治愈希望。90%的HBsAg清除率不仅是一个临床数字,更象征着乙肝治疗从“终身管理”向“功能性治愈”的历史性跨越。
然而,功能性治愈的终局尚未到来。无论是 HT-101、Bepirovirsen 还是其他在研药物,停药后的持久应答仍是决定其临床价值与商业成功的终极考验。未来2-3年,随着多个IIb/III期研究的停药数据陆续公布,乙肝治疗市场的竞争格局将逐渐清晰。
在GSK、强生等跨国药企与广生堂、恒瑞医药、腾盛博药等国内领先企业的同台竞技下,乙肝治疗市场正迎来翻天覆地的变化。2026年,随着GSK提交上市申请以及更多中国II期、III期数据的出炉,我们距离“告别乙肝”的梦想正越来越近。
参考来源:
[1] 官方披露资料
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 2025年乙肝新药最新动态丨“功能性治愈”再升级!贺普拉肽、HH-003、GSK836...
2. HH-003乙肝新药最新消息丨全球首创!阻断病毒+免疫清除,乙肝治疗新答案
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论