
帕金森病(PD)作为全球老年人群中最高发的神经退行性疾病之一,正在影响着数以百万计的患者生活。尽管近年来分子生物学和病理发病机制的研究高歌猛进,但直至今日,人类依然没有找到能够彻底治愈帕金森病的“终极武器”。目前的临床治疗策略,其核心仍然是控制症状、延缓病情并尽量改善患者的生存质量。
在这一长期的抗争中,多巴胺前体药物——左旋多巴(L-dopa)自20世纪60年代末问世以来,始终稳坐帕金森病治疗的“第一把交椅”。然而,这顶王冠并不完美。长期服用左旋多巴不可避免地会带来药效衰退、运动波动以及令人痛苦的异动症。为了破解这一困局,医药界开始了长达数十年的外周代谢酶抑制剂的探索之旅。本文将带您深入解析第三代儿茶酚-O-甲基转移酶(COMT)抑制剂——奥匹卡朋(Opicapone)的硬核研发历程,看科学家如何通过精妙的药物化学分子设计,在疗效与毒性之间走钢丝,最终寻得破局之法。
一、 左旋多巴的代谢困境与COMT靶点的确立
左旋多巴的临床应用面临着一个巨大的生理学障碍:复杂的药物外周代谢。当患者口服左旋多巴后,绝大部分药物在进入大脑前,就会在外周组织中被外周氨基酸脱羧酶(AADC)无情地代谢掉。为了保卫左旋多巴,临床上常将其与AADC抑制剂(如卡比多巴或苄丝肼)联用。
但这仅仅是按下了葫芦浮起了瓢。抑制了脱羧途径后,另一种生物代谢途径被迅速激活:在儿茶酚-O-甲基转移酶(COMT)的催化下,左旋多巴被大量甲基化,转化为无活性的3-O-甲基-L-多巴胺(3-OMD)。这直接导致进入大脑的左旋多巴浓度大幅缩水。由此,科学家明确了一个战略方向:只有同时抑制AADC和COMT,才能最大化左旋多巴的生物利用度,从而降低给药剂量并缓解晚期患者的症状波动。

COMT抑制剂的“前世”与痛点
COMT这一靶点在制药界并不陌生,它广泛存在于哺乳动物体内,主要负责催化儿茶酚底物的甲基化。
第一代试水:以多酚类物质(如邻苯二酚、环庚三烯酚酮、没食子酸)为代表。这类化合物不仅体内药效极其惨淡,靶点选择性差,还伴随着难以接受的强毒性。
第二代登场:科学家在邻苯二酚的邻位引入了硝基,诞生了托卡朋(Tolcapone)、恩他卡朋(Entacapone)以及奈比卡朋(Nebicapone)等知名药物。它们与COMT的亲和力极高。但临床现实依然骨感:
- 托卡朋药效长效,但上市后引发了致命的暴发性肝炎,导致其临床应用被严格限制。
- 恩他卡朋虽然肝脏安全性好,但存在致命的药代动力学缺陷——半衰期太短,导致患者每天需要高剂量服药多达8次,依从性和临床有效性大打折扣。
第二代经典COMT抑制剂的临床特性与局限性对比

行业迫切呼唤一种结构新颖、外周组织高度选择性、超长效(每日仅需给药1次)且安全的第三代COMT抑制剂。
二、 破茧成蝶:奥匹卡朋的药物化学发现之旅
奥匹卡朋(内部研发代号 BIA 9-1067)的横空出世绝非科学史上的偶然,它是葡萄牙BIAL制药公司研发团队运用基于结构的药物设计逻辑,经历无数次构效关系(SAR)试错与优化的心血结晶。研发团队的破局点,来自于对海量儿茶酚类化合物库的系统筛查。
1. 苗头初现:打破传统的吡唑类衍生物
通过体外活性筛选,研发团队锁定了一个具有中等活性的苗头化合物——吡唑类化合物4a (BIA 9-693)。与第二代的经典结构不同,4a为药物化学家提供了一个极具潜力的“骨架”,其中心吡唑环、酚羟基位置等均留有巨大的结构修饰空间。
苗头化合物BIA 9-693的化学结构
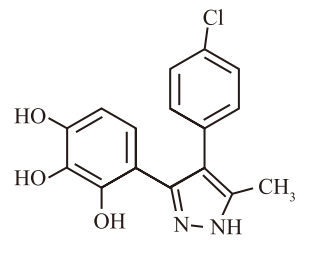
团队随即展开了严密的构效关系(SAR)研究。首先对儿茶酚药效团进行“开刀”。实验数据给出了明确的结论:想要获得强大的体外COMT抑制活性,强吸电子基团(尤其是硝基)是绝对必需的。硝基的强吸电子效应能够显著降低邻位羟基的亲核性,从而抵抗酶促反应的失活。一旦将硝基替换为其他基团(如氟、溴或羧基),抑制活性便呈现断崖式下跌。
2. 核心杂环的“排列组合”与魔法
在确认了硝基邻苯二酚的绝对地位后,团队将目光转向了连接该基团的“桥梁”——中心杂环。这一步,展现了药物设计中神奇的“杂原子效应”。
研究人员系统性地合成了大量五元和六元杂环类似物,并在小鼠体内评估其长效抑制能力:
- 失败的尝试:将吡唑环中的氮原子排列方式稍微改变,换成咪唑环(化合物5),令人大跌眼镜的是,化合物竟然完全丧失了对COMT的抑制能力。引入氧原子或硫原子的噁唑、噻唑环,同样无法在体内产生长效的抑制作用。
- 突破性进展:当团队尝试在核心五元环中增加第三个杂原子,引入噁二唑环时,奇迹发生了。特别是当采用1,2,4-噁二唑环,并将硝基邻苯二酚基团连接在杂环的5位时(化合物11a),抑制活性大幅飙升,甚至可以与阳性药托卡朋比肩。
- 绝佳的选择性:更令人振奋的是,化合物11a不仅活性强,其对外周COMT的抑制选择性比中枢COMT高出至少3倍,完美契合了开发外周靶向药物的初衷。化合物11a顺理成章地成为了进一步优化的先导化合物。
3. 跨越“脂溶性与毒性”的陷阱:奥匹卡朋的最终定型
找到了优秀的骨架,但在成药性的道路上,一只“拦路虎”出现了。
在针对杂环3位取代基的优化中,研究人员发现了一个清晰但令人头疼的规律:化合物的亲脂性(logP值)越高,体内COMT抑制活性越强;但同时,潜在的细胞毒性风险也呈正比例急剧放大。那些活性比肩托卡朋的高脂溶性化合物,在神经母细胞瘤细胞系实验中,均表现出了令人无法接受的毒性。而降低脂溶性引入极性基团,虽然毒性消失了,但药效也随之崩塌。
如何在“高活性”与“低毒性”之间找到完美的平衡点?
团队做出了一项极具创造性的化学改造:引入吡啶N-氧化物。
- 吡啶环的氮原子被氧化后,极大地增加了分子的极性,未取代的烟酸N-氧化物衍生物(12a)表现出了零毒性,但代价是口服吸收变差,药效有所下降。
- 为了弥补口服吸收问题,团队开始进行精细的“微调”。他们在吡啶N-氧化物环的特定位置引入不同数量和种类的亲脂性基团(如三氟甲基、甲基、卤素),试图将logP值一点点拉回理想区间。
- 终极分子诞生: 经过上百次的试错,最终的破局者——化合物12m(BIA 9-1067,即奥匹卡朋)脱颖而出。它通过精巧的甲基和氯原子取代组合,实现了不可思议的平衡:COMT抑制活性获得了进一步的提升,而毒性风险甚至比目前市面上最安全的恩他卡朋还要低! 这款分子正式拿到了走向临床的通行证。
奥匹卡朋的结构式
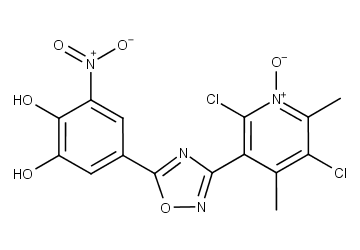
图源:摩熵医药数据库
三、 从实验室到患者:奥匹卡朋的临床验证
带着极具天赋的化学结构,奥匹卡朋在后续的药理学和临床试验中,交出了一份无可挑剔的答卷。
1. 强大的临床前数据支持
动物模型证实了奥匹卡朋非凡的药效学特征。在大鼠体内,单次低剂量给药即可对肝、肾外周COMT产生超过80%的强烈抑制,且作用极其持久,但其在血浆中的半衰期却非常短。这意味着药物不仅靶向精准,且不易在体内蓄积。

奥匹卡朋对COMT活性的剂量-反应曲线。Wistar大鼠分别给予0.03、0.1、0.3、0.6、1.0和3.0 mg·kg⁻¹的奥匹卡朋,并在给药后2小时和6小时评估肝脏、肾脏和红细胞中的COMT活性。数据为4-10只大鼠的平均值±标准误。
在食蟹猴模型中,奥匹卡朋表现出了强大的协同效应。它能使动物体内的左旋多巴全身水平翻两倍,同时将有害代谢物3-OMD的脑内水平骤降58%至86%。在至关重要的肝毒性风险评估中,奥匹卡朋对人类原代肝细胞线粒体膜电位和ATP含量的影响,远远低于托卡朋和恩他卡朋,展现了极宽的安全窗。
2. 决胜三期临床试验 (BIPARK I & II)
在一期和二期临床中,奥匹卡朋展现了良好的耐受性,证实了其剂量依赖性的S-COMT抑制作用,并且其复合物解离时间明显长于恩他卡朋,确立了每日1次给药的巨大优势。
随后开展的两项大规模国际多中心、双盲三期临床试验(BIPARK I 和 BIPARK II),彻底奠定了奥匹卡朋的临床地位:
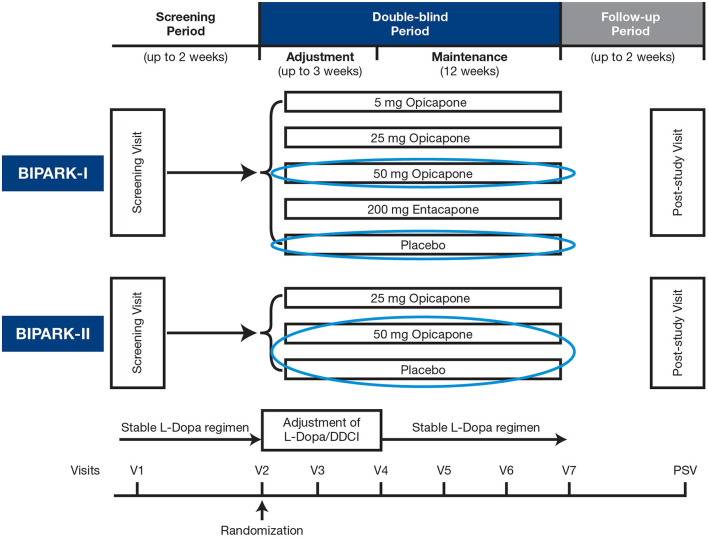
研究设计。DDCI,多巴脱羧酶抑制剂;L-Dopa,左旋多巴;PSV,研究后访视;V,访视。
- 显著缩短“关闭期”:在接受左旋多巴治疗并出现运动波动的患者中,每日1次服用50mg奥匹卡朋,相较于安慰剂组,患者每日的绝对关闭期(药物失效、症状恶化的时间)平均减少了54至61分钟,具有极高的临床统计学意义。
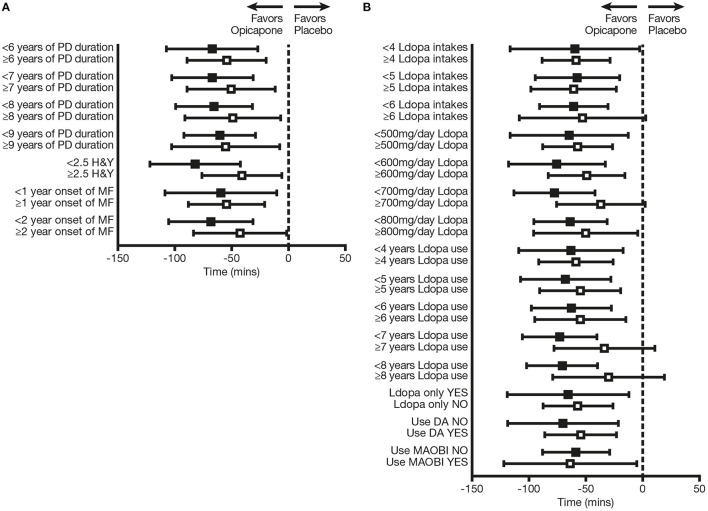
根据(A)基线疾病相关特征和(B)基线治疗相关特征划分的患者亚组,绝对“关期”时间较基线的变化。黑色方块表示疾病进程和左旋多巴治疗路径中处于“早期”的患者亚组;空心方块表示疾病进程和左旋多巴治疗路径中处于“晚期”的相应对照患者亚组。DA,多巴胺激动剂;H&Y,Hoehn 和 Yahr 分级;L-DOPA,左旋多巴;MAO-BI,单胺氧化酶-B 抑制剂;MF,运动波动;PD,帕金森病。
疗效优于竞品:其疗效不劣于对照药恩他卡朋,并在临床医生和患者的整体印象量表(CGI-C/PGI-C)评估中,均显著优于安慰剂和恩他卡朋。
安全性与依从性:尽管因为左旋多巴生物利用度的提高,奥匹卡朋治疗组出现了较高比例的运动障碍(患者大多认为程度不严重),但至关重要的是,没有发现任何严重肝脏副作用的报告,不良反应停药率极低。此外,它不会像恩他卡朋那样引起尿液变色等尴尬的不良反应。
四、 结语
从一个简单的吡唑类苗头化合物,到跨越脂溶性与毒性的研发天堑,奥匹卡朋(Opicapone)的诞生是一部教科书级别的药物化学进化史。
作为具有全新结构的第三代COMT抑制剂,它不仅在疗效上超越了前辈,更凭借每日一次的极简给药方案和卓越的安全性,为晚期帕金森病患者提供了一种更优效、更安全的左旋多巴辅助治疗策略。它毫无疑问将成为替代托卡朋和恩他卡朋的新一代标杆药物。
时至今日,由BIAL公司原研的奥匹卡朋(商品名:Ongentys)已相继在欧洲(2016年)、美国FDA(2020年)、日本及全球众多核心医药市场获得最高级别的监管批准,并被广泛应用于临床一线的抗帕金森病辅助治疗。
扩展阅读:
1. 前列腺癌非甾体AR拮抗剂进化史:氟他胺破冰、比卡鲁胺称王、恩扎卢胺重塑生存期
2. 匹托利生:从硫丙咪胺的肝毒性到全球首款H3受体反向激动剂,攻克血脑屏障,改写嗜睡症治疗指南
3. 曲氟尿苷-替匹嘧啶(TAS-102)研发复盘:从实验室到临床,解锁抗肿瘤新机制与多癌种潜力
查数据,找摩熵!想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论