当下,恶性肿瘤已成为威胁中国居民健康的首要因素之一,其中实体瘤以肺癌、乳腺癌、结直肠癌等为主要代表,凭借高发病率、高死亡率的显著特征,成为医疗领域重点攻坚的方向。
近年来,随着分子生物学、免疫学等基础学科取得突破性进展,加之政策支持与技术创新的双重驱动,中国实体瘤治疗行业实现了从传统治疗向精准治疗、联合治疗的跨越式发展,药物研发格局与市场生态也随之发生了深刻变革。
本报告聚焦中国实体瘤流行病学趋势及热门靶点药物市场表现,系统梳理行业发展脉络、核心驱动因素及前沿实践成果,为行业参与者、研究者及相关机构提供全面且具参考价值的专业洞察。
一、中国实体瘤行业概述
1. 肿瘤致病机制分析及治疗方案演进
按照肿瘤的生长形态、病变部位及组织起源,恶性肿瘤通常可划分为实体瘤和血液瘤两大类。两类肿瘤在细胞起源、核心致病因素、疾病进展路径及临床管理模式等方面存在系统性差异。
实体瘤与血液肿瘤致病机制对比
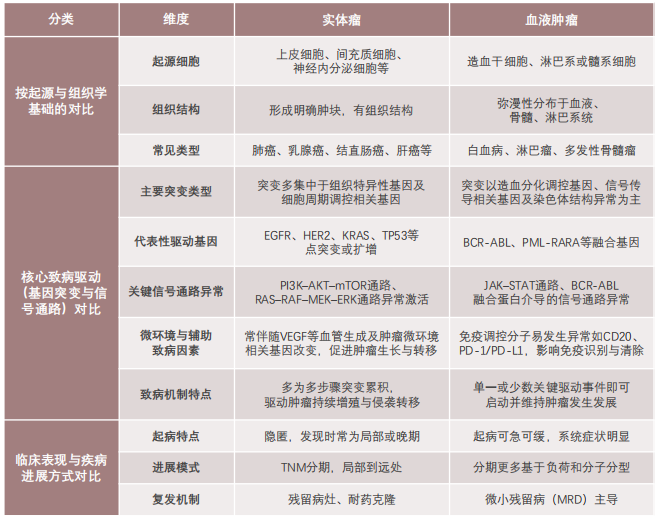
实体瘤(Solid Tumors)起源于上皮组织、间叶组织或神经内分泌系统等分化相对成熟的实体组织细胞, 如肺上皮细胞、乳腺导管上皮细胞、胃肠道黏膜细胞以及骨、软骨细胞等,其病理特征以局部占位性肿块形成核心,疾病早期通常局限于原发器官或组织。随着疾病进展,肿瘤细胞通过局部浸润、淋巴转移或血行转移等方式扩散至周围组织及远处器官,形成继发病灶。
血液肿瘤(Hematologic Malignancies)主要起源于骨髓造血干细胞或淋巴造血系统细胞,异常克隆多涉及白细胞及其前体细胞、淋巴细胞等造血相关细胞谱系。血液肿瘤通常不形成明确的实体肿块,而是表现为造血系统内异常细胞的弥漫性扩增。异常细胞在骨髓内大量堆积并进入外周血,同时浸润脾脏、淋巴结、肝脏等造血相关器官,最终导致正常造血功能受抑。
2. 中国实体瘤临床治疗方案演进历程
中国实体瘤临床治疗方案的发展,与药物研发、临床理念及技术进步紧密关联,其演进历程清晰展现了精准化、个体化的治疗趋势。
传统治疗阶段(20世纪末—2010年前):在此时期,中国实体瘤的临床治疗主要依赖手术切除、放射治疗及细胞毒性化疗等传统治疗手段。其中,手术切除是早期实体瘤的首选治疗方式,目标在于尽可能清除原发肿瘤病灶。放疗多作为术后辅助治疗或局部晚期患者的重要控制手段。而化疗则在无法手术或存在转移风险的患者中广泛应用。该时期中国实体瘤治疗策略主要以“降低肿瘤负荷”为核心目标,缺乏对肿瘤分子分型的系统认知,且药物选择相对有限,疗效与毒副作用并存。
靶向治疗兴起(2010年前后—2017年):随着中国肿瘤分子生物学研究的深入,EGFR、HER2、ALK、VEGF等关键驱动基因及信号通路逐步被解析,靶向治疗在实体瘤领域开始加速引入并应用于临床。以非小细胞肺癌、乳腺癌和结直肠癌为代表,靶向药物通过选择性抑制肿瘤驱动通路,在部分分子分型人群中显著改善了无进展生存期和治疗耐受性。这一阶段,中国实体瘤治疗逐步从“统一方案”向“人群分层”过渡,分子检测开始进入临床决策体系。
免疫治疗快速普及(2018年-2024年):自PD-1/PD-L1抑制剂在中国获批上市并快速纳入医保以来,免疫治疗成为实体瘤治疗格局中最具变革性的力量之一。在政策支持、国产创新药密集获批及价格可及性提升的共同推动下,免疫治疗在中国临床实践中的使用范围迅速扩大,逐步从后线治疗前移至一线治疗方案。这一阶段,治疗目标由单纯抑制肿瘤生长转向激活免疫系统长期控制肿瘤生存获益,维度从PFS延伸至总生存期,联合治疗策略逐渐成为主流探索方向。
联合与个体化治疗阶段(2025年至今):在当前阶段,中国实体瘤治疗正向多手段联合与高度个体化方向演进。免疫治疗与化疗、靶向治疗、抗血管生成治疗及放疗等多种手段的联合应用,成为提升疗效、延缓耐药的重要策略。同时,生物标志物如PD-L1表达、TMB、MSI状态等在治疗决策中的作用不断强化,推动临床方案从"经验驱动"向"数据与分子特征驱动"转变。整体来看,中国实体瘤临床治疗已进入一个疗效提升与精细化管理并重的新阶段,这一趋势也为创新药研发和差异化竞争提供了重要窗口。
3. 中国实体瘤相关政策
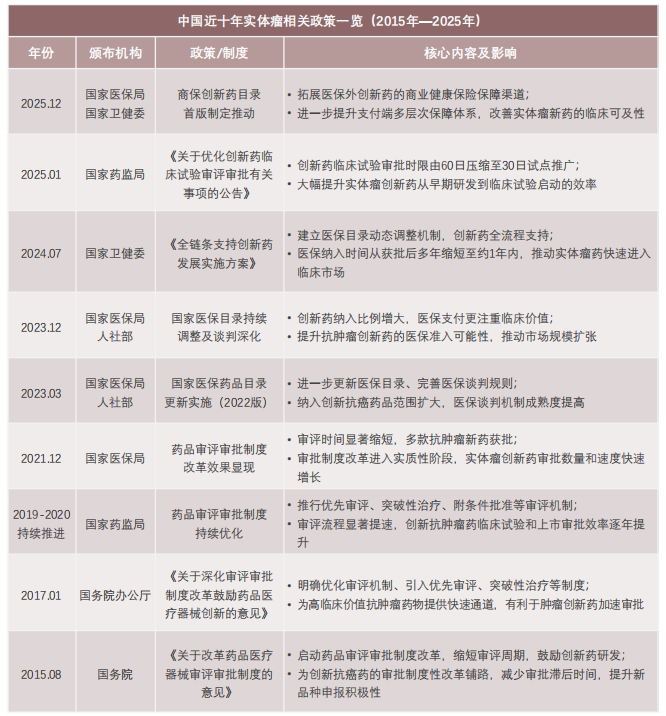
近年来,中国持续出台并优化针对实体瘤领域的系列政策,着力打通创新药从研发、审评、上市到医保准入的关键环节,全面提升药品临床可及性,系统构建覆盖全生命周期的政策支持体系。
中国实体瘤治疗相关政策,2015-2025
4. 中国实体瘤药物市场规模与增长趋势
实体瘤靶向治疗药物市场已从单纯的规模增长阶段,迈入以产品创新、差异化竞争、成本控制为核心的高质量发展新阶段,市场规模的震荡是行业结构优化、产业升级的阶段性体现。
中国实体瘤药物市场规模与增长趋势,2020-2030E
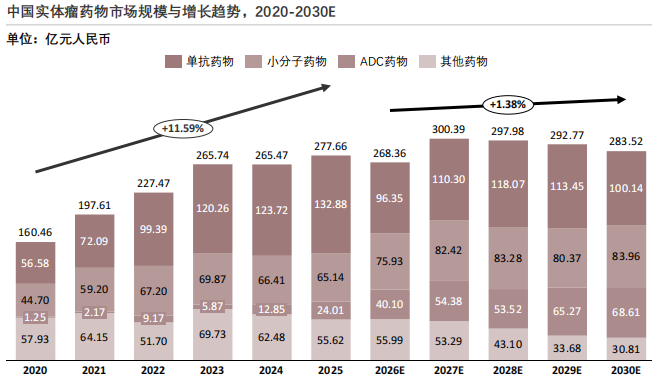
中国实体瘤靶向治疗药物市场规模呈现前期稳步增长、后期震荡下行的发展特征,行业发展从高速扩容逐步进入结构调整阶段。肿瘤精准医疗需求的持续释放、靶向药研发成果的集中落地,驱动中国实体瘤靶向治疗药物市场规模从2020年的160.46亿元持续攀升至2023年的265.74亿元,实现阶段性稳步增长,行业进入需求与政策双驱动的增长期。2023年后,市场规模陷入波动,2024年受区域集采落地导致多款成熟靶向药价格大幅下调,市场出现小幅回落。2026年,因国家医保谈判持续推进以量换价、多款进口原研药专利到期引发仿制药价格战、新一代靶向药研发产出出现阶段性断层,市场规模再度回落。随着新一代靶向药密集获批上市、精准医疗渗透率提升拓宽药物适用人群,预测2027年市场规模实现阶段性回升,但整体市场增长动力已明显衰减,行业增长逻辑也随之从单纯的规模扩张转向以创新质量和临床价值为核心的质量优化阶段。
市场变化背后,是多重行业因素的共同作用。医保谈判与集中采购的常态化推进,使得多款实体瘤靶向药大幅降价,虽实现了"以价换量"的市场普及,但短期内直接影响了市场规模的数值增长。靶向药研发领域出现同质化竞争,部分热门靶点扎堆布局,新增产品对市场规模的拉动效应减弱,而核心品种专利到期也带来了市场份额的重新分配。行业迎来治疗技术的迭代,ADC药物、双特异性抗体等新型靶向疗法逐步商业化,传统靶向药市场受到挤压,行业进入新旧产品的更替调整期。此外,DRG/DIP医保支付方式改革的落地,也对医疗机构的用药选择形成约束,进一步影响了实体瘤靶向药的市场规模走势。
5. AI在药物发现与临床试验中的作用
在实体瘤临床试验中,AI在患者招募、试验设计、影像评估和数据监测环节均能发挥显著作用,但各环节的效率提升效果和商业价值有所差异。
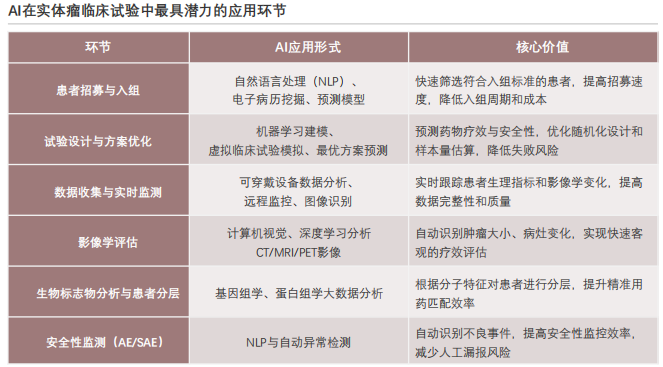
◼ 患者招募与入组:传统招募模式依赖人工筛选电子病历和患者咨询,周期长,尤其是复杂纳排标准的试验,招募难度更大,约30%的实体瘤临床试验因招募不足导致延期。通过NLP技术解析电子病历中的临床数据、基因检测结果等信息,结合预测模型快速筛选潜在受试者,精准匹配纳排标准后,招募周期从10个月可缩短至4.5个月,招募效率提升55%。
◼ 试验设计优化:传统试验设计依赖研究者经验和小样本预试验,样本量估算不精准、随机化方案效率低,导致实体瘤临床试验失败率较高,而通过AI可预测不同剂量组的疗效-安全性曲线后可设计出更精准的分层随机化方案。如目前在PD-1抑制剂联合化疗治疗晚期胃癌的Ⅲ期试验,采用AI优化设计后的样本量从600例减少至420例,试验周期缩短6个月,同时试验成功率从预计的45%提升至62%,显著降低了研发成本。
◼ 数据监测与影像学评估:实体瘤临床试验数据量大,人工数据整理和分析耗时且易出错,通过AI可实时监控可穿戴设备收集的患者生理数据,自动识别异常指标并预警。此外,还可通过AI深度学习算法分析CT/MRI/PET影像,自动测量肿瘤最长径、计算肿瘤负荷变化,实现RECIST标准的自动判定。如在乳腺癌临床试验中采用AI影像评估系统后,影像分析时间从每例患者20分钟缩短至3分钟,评估一致性Kappa值提升至0.89,评估效率提升70%以上,同时提高试验结果的客观性和可靠性。
二、肺癌靶向治疗药物市场分析
1. 肺癌疾病概述
肺癌(Lung Cancer)起源于支气管黏膜上皮或肺泡上皮,其发生发展是一个多因素、多阶段、多基因参与的复杂过程,主要受遗传易感性与环境致癌物暴露共同驱动。
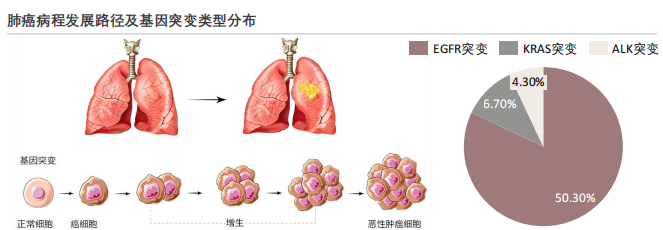
不同致癌因素及其累积效应,会导致肿瘤在细胞起源、生物学行为及分子特征方面呈现显著异质性。从分子机制层面看,长期吸烟、空气污染以及接触石棉、氡气、砷等职业性致癌物,或暴露于电离辐射等外源性危险因素,可导致肺上皮细胞DNA发生持续性损伤,进而引起原癌基因异常激活和抑癌基因功能失活,最终促使肺癌的发生和进展。基于这种生物学差异,肺癌在病理学上可分为小细胞肺癌和非小细胞肺癌两大类型。其中,小细胞肺癌起源于具有神经内分泌分化特征的细胞,表现为细胞体积小、增殖活跃、侵袭性强,早期即易发生转移等特征,约占所有肺癌的15%,非小细胞肺癌则约占全部肺癌的80%至85%。
非小细胞肺癌可进一步细分为腺癌、鳞状细胞癌、大细胞癌及腺鳞癌等混合亚型。分子分型是实施靶向治疗的核心依据,目前已明确的热门靶点包括EGFR、ALK、ROS1、BRAF、MET、RET及KRAS等。其中,EGFR、KRAS和ALK是中国NSCLC患者最常见的突变类型,复旦大学在对1770例手术切除NSCLC样本的回顾性分析中,显示中国EGFR、KRAS和ALK仍为NSCLC患者中最常见的三种突变,占比在整体人群中分别为50.3%、6.7%和4.3%。
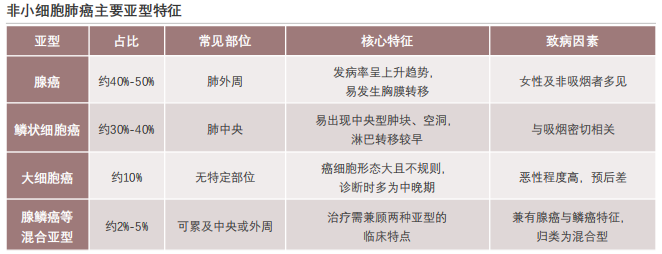
2. 肺癌临床分期与诊疗方案
肺癌的临床分期是精准制定诊疗方案的核心依据,直接决定着治疗策略的选择与患者的预后。目前,临床基于三个维度的TNM分期系统,将肺癌分为0期至Ⅳ期。
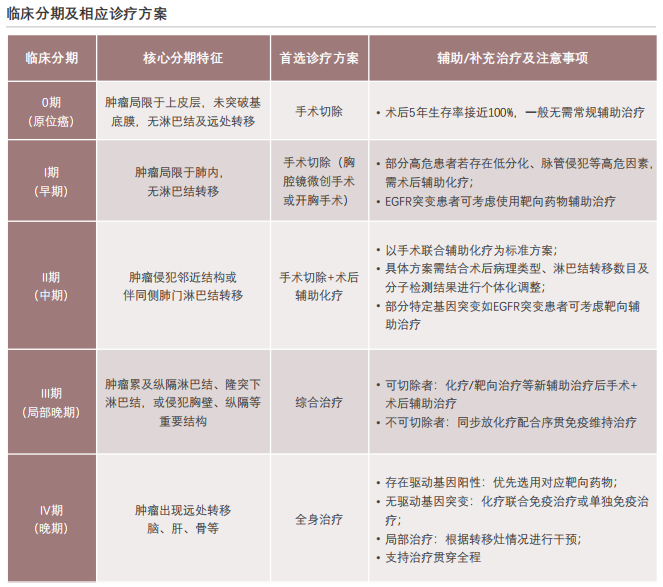
非小细胞肺癌的临床分期治疗始终遵循"分期而治+精准施策"的核心原则。0期仅需根治性手术切除即可实现临床治愈,5年生存率接近100%。Ⅰ期以手术切除为首选,部分存在高危因素的患者可辅以术后化疗,整体预后良好。Ⅱ期和可切除Ⅲ期需采用"手术+术后放化疗/免疫治疗"的综合模式,部分患者还可通过术前新辅助治疗缩小肿瘤、提高手术切除率,以最大程度降低复发风险。Ⅳ期已失去局部根治机会,治疗的核心转为基于基因检测和PD-L1免疫标志物的全身精准治疗,包括靶向治疗、免疫治疗或联合化疗。
3. 中国肺癌靶向治疗领域宏观环境分析
吸烟的数量和年数与肺癌患病风险成剂量反应关系,中老年吸烟群体尤为高危。此外,患者群体呈女性化、年轻化趋势,非小细胞肺癌占主导且靶向治疗日趋成熟,鳞癌与小细胞肺癌的治疗仍需突破。
(1)吸烟史与风险关联:长期吸烟仍是高危标志,二手烟危害凸显
吸烟是肺癌的首要高危因素,可使患病风险增加10至20倍。在肺癌患者中,有明确吸烟史,即每日≥1支且持续≥10年的群体占比高达42%。其中,吸烟指数每日吸烟支数×吸烟年数超过400的重度吸烟者,其肺癌发病风险更是不吸烟者的12至20倍,主要诱发肺鳞癌和小细胞肺癌。此外,二手烟暴露同样是明确的致癌风险。在不吸烟的肺癌患者中,约50%的女性和25%的男性长期生活在二手烟环境中,中老年女性是这一风险下的核心受害群体。
(2)发病率持续高位,早期诊断率显著提升
我国肺癌负担呈"高发病、高存量"特征。2024年全国肺癌新发病例达106.06万,占所有恶性肿瘤新发病例的22.0%,存量患者已超过800万,且每年新增病例稳定在70万左右。与高发病率形成对比的是,早期诊断率已从2006年的37.1%跃升至2021年的85%,健康体检发现的病例占比从44%升至70.5%,这一方面源于低剂量螺旋CT筛查的普及,另一方面也使更多患者获得早期干预机会,为靶向辅助治疗拓展了应用场景。
(3)患者人群呈现年轻化趋势转变
肺癌发病呈现年轻化趋势,并且性别差异加剧。男性患者中,45至65岁中年群体吸烟率仍维持在28%至42%的较高水平,65岁以上老年群体吸烟率约为23%。这部分人群是肺鳞癌等吸烟相关肺癌的高发群体。同时,女性肺癌的发病率和死亡率正逐年攀升,且发病年龄更年轻,根据国家癌症中心数据,2024年中国女性肺癌发病率为47.8/10万,其中城市52.1/10万,农村40.3/10万。虽然男性的肺癌发病率和死亡率都高于女性,但两性之间的差异正在缩小。
(4)腺癌成为绝对主导,分型结构与靶向需求高度契合
肺腺癌已成为中国肺癌中最常见的病理类型,尤其在女性和不吸烟人群中高发,占比超过五成。其发病与基因突变关系密切,因此靶向治疗和免疫治疗等精准疗法应用更为广泛。此外,肺鳞癌约占肺癌的三成,发病与吸烟高度相关,肿瘤多为中央型。虽然化疗和免疫治疗是主要手段,但整体治疗进展相对缓慢。
4. 中国肺癌靶向治疗药物——在研管线靶点覆盖
中国肺癌在研靶点高度集中,EGFR与PD-L1为两大最热门靶点,临床试验数量显著领先,EGFR罕见突变亚型、HER2等靶点仍以早期探索为主,存在差异化创新机遇。
2025年中国肺癌在研靶点数量Top10
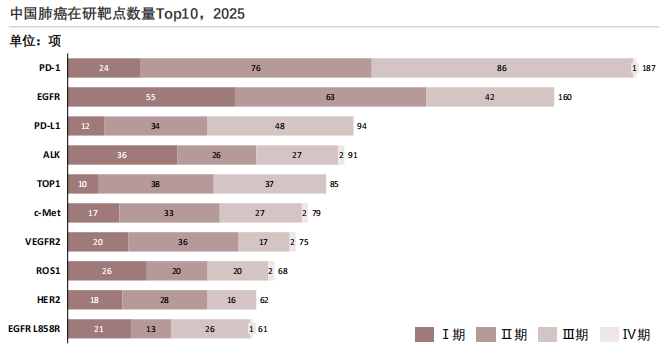
查数据,找摩熵!数据来源:摩熵医药数据库
研发热度TOP3靶点:EGFR和PD-1为当前肺癌领域的绝对热门靶点,总体试验数量显著高于其他靶点,充分反映其在肺癌治疗体系中的核心地位。其中,EGFR的BE试验数量达57项,明显高于其他靶点,提示大量仿制药或生物类似药仍处于研发阶段。同时,其Ⅰ期和Ⅱ期试验数量保持高位,说明围绕EGFR仍有较多新分子实体处于早期探索阶段。PD-1的Ⅲ期临床试验数量达86项,为所有靶点中最高,且上市后药物数量达到19项,表明该靶点的临床应用成熟度较高,同时仍有大量新药项目处于关键性临床验证阶段。
临床试验阶段分布特征:成熟靶点PD-1、VEGFR2的Ⅲ期+上市后药物数占比较高,分别为44.9%和37.7%,说明这些靶点的药物已进入后期临床或商业化阶段;早期研发靶点EGFRL858R、HER2的Ⅰ期+Ⅱ期试验数占比相对较高,分别为37.6%和50%,提示这些靶点仍以新药物探索为主;细分靶点机会方面,EGFRL858R作为EGFR的突变亚型,总试验数仅为EGFR的39.1%,存在针对突变亚型的差异化研发空间。
VEGFR家族靶点对比:VEGFR1、VEGFR2和VEGFR3在各临床阶段的试验数量分布高度相似,尤其是VEGFR1与VEGFR3的总试验数量仅相差1项,反映三者在肺癌治疗中的研发路径和技术布局具有较高重叠度。从商业化成熟度来看,VEGFR2的上市后药物数量达到38项,显著高于VEGFR1和VEGFR3均为17项,说明VEGFR2在抗血管生成治疗领域的临床应用和市场转化程度更为成熟。
5. 中国肺癌靶向治疗药物——企业在研管线分析
当前中国肺癌靶向治疗药物在研领域,本土药企研发布局分化显著,头部企业兼顾全周期研发,部分企业主攻早期靶点探索,形成与跨国药企差异化竞争的产业格局。
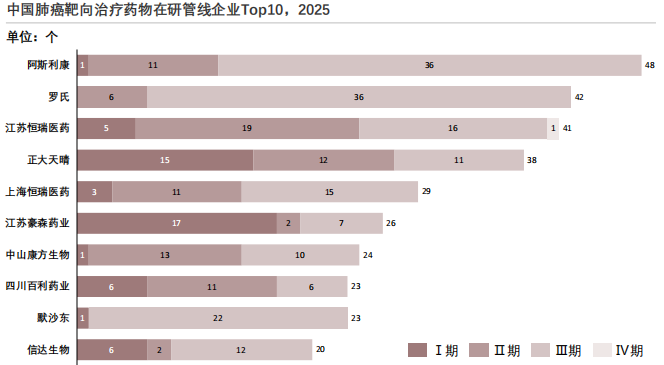
2025年中国肺癌靶向治疗药物在研管线企业Top10
查数据,找摩熵!数据来源:摩熵医药数据库
(1)跨国药企研发布局聚焦中后期以Ⅲ期临床为主
阿斯利康、罗氏、默沙东三家跨国药企的在研项目合计93项,其中Ⅲ期临床项目占比超60%。阿斯利康Ⅲ期项目达36项,罗氏Ⅲ期项目同样为36项,默沙东Ⅲ期项目22项,三家企业均无Ⅳ期临床项目,且Ⅰ期项目极少。这一布局体现出跨国药企在肺癌靶向治疗领域的成熟度与商业化导向,管线多集中于接近上市的关键阶段,风险相对较低。
(2)本土药企研发布局分化头部企业管线结构更均衡
江苏恒瑞医药在研项目41项,覆盖Ⅰ至Ⅳ期全阶段,其中Ⅱ期项目数量最多达19项,同时拥有1项Ⅳ期临床项目,反映出恒瑞在肺癌靶向治疗领域兼顾早期探索与后期验证,且重视上市后药物的疗效与安全性再评价。正大天晴、上海恒瑞管线以Ⅱ、Ⅲ期为主,整体偏向临床中后期,与跨国药企的布局逻辑相近,体现出本土头部企业加速推进管线商业化的战略目标。江苏豪森在研项目26项,Ⅰ期项目高达17项,Ⅱ、Ⅲ期项目数量极少,布局特点与其他本土企业形成鲜明对比,显示其聚焦于早期创新靶点的探索,研发风险相对较高,但未来潜力较大。
(3)本土企业整体研发活跃度高与跨国药企形成差异化竞争
本土药企在研项目总数远超三家跨国药企,且部分企业如江苏豪森聚焦早期研发,与跨国药企的中后期管线形成互补。这一格局表明,中国肺癌靶向治疗药物研发已形成"跨国药企主导成熟靶点商业化、本土药企兼顾创新靶点探索与跟进型研发"的差异化竞争态势。
6. 中国肺癌热门靶点药物年度销售额变化趋势
中国肺癌热门靶点医院端总销售额中EGFR靶点基数最大,ALK靶点凭药物迭代与检测普及持续增长,ROS靶点靠药物可及性提升扩容,PD-1因临床获益有限规模偏低。
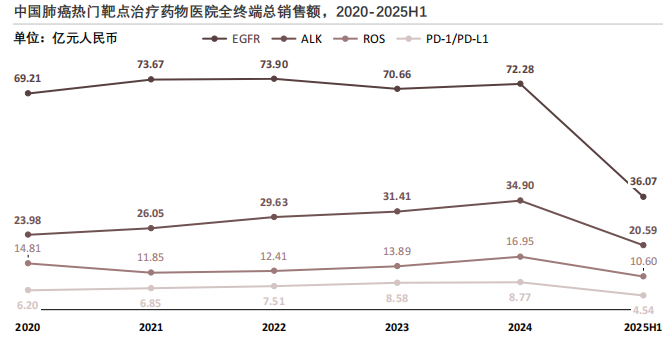
查数据,找摩熵!数据来源:摩熵医药数据库
从2020年至2025年上半年,中国肺癌热门靶点治疗药物中EGFR靶点始终是市场基数最大的品类。EGFR靶点治疗药物销售额从2020年的约69亿元稳步上升至2024年的约72亿元,体现出稳定的临床需求与用药基础。随着ALK、ROS等靶点精准治疗的渗透,部分EGFR突变患者的跨靶点用药选择有所增加,2023年后其规模的小幅回落。
- ALK靶点:临床迭代驱动的高增长赛道
ALK靶点销售额从2020年的24亿元增至2025年的36亿元,复合增长率达8.1%,是增长动能最强的靶点。核心驱动因素包括药物供给升级:二代ALK抑制剂如阿来替尼一线适应症获批,三代药物如洛拉替尼完成后线布局,实现了患者全程治疗需求的覆盖。此外,下一代测序技术(NGS)在肺癌基因检测中的普及率从2020年的不足30%提升至2024年的60%以上,ALK突变人群的检出率显著提高。
- ROS靶点:小众靶点的临床价值释放
ROS靶点销售额从6亿元增至11亿元,呈现"低基数高弹性"特征。这一增长源于靶向药物的可及性突破:2021年后,国产ROS1抑制剂如恩曲替尼等仿制药获批上市。同时,临床指南将ROS1检测纳入非小细胞肺癌常规推荐,患者用药转化率得以提升。
- PD-1/PD-L1:EGFR突变人群中的应用限制
该类药物在EGFR靶向药市场中的规模始终低于9亿元,核心瓶颈是临床获益的局限性。EGFR突变患者通常伴随PD-L1低表达、TMB(肿瘤突变负荷)偏低,其免疫治疗的客观缓解率仅为10%—15%,远低于化疗或靶向治疗,因此指南推荐级别较低,临床应用场景受限。
7. 中国肺癌热门靶点代表药物累计销售额结构分析(1/3)
肺癌热门靶点代表药物2020-2025H1医院端累积销售额为685.32亿元,其中EGFR靶向药物凭借强临床定位与成熟应用成为当前肺癌靶向治疗的核心支柱,ALK靶点处于次核心位置。
EGFR靶点是当前肺癌靶向治疗的临床核心支柱,该靶点药物凭借成熟的临床证据和广泛的患者人群,在医院端累计销售额中占比最高,成为市场绝对核心。
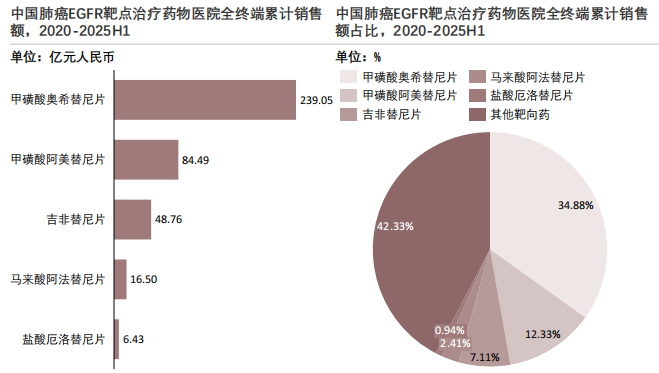
从整体市场格局角度,EGFR靶点相关药物合计销售额显著高于ALK、ROS等其他驱动基因靶点,构成肺癌靶向治疗市场的主要收入来源。从EGFR靶点具体数据看,甲磺酸奥希替尼片销售额为239.05亿元,占比约35%,为所有统计品种中规模最大的单一产品。甲磺酸阿美替尼片和吉非替尼片销售额分别为84.49亿元和48.76亿元,占比分别约12%和7%,处于第二梯队。马来酸阿法替尼片与盐酸厄洛替尼片销售额分别为16.50亿元和6.43亿元,占比均处于2%以下,反映出其在整体EGFR治疗体系中的边际化地位。
核心品种凭借先发优势和医保准入占据了主要市场份额。此外,靶点分化特征也较为明显,除EGFR外,ALK等其他靶点药物合计占比相对有限,反映出当前肺癌靶向治疗仍以EGFR为绝对核心,其他靶点尚处于快速增长但规模相对较小的阶段。
这一市场格局的形成,主要得益于EGFR靶点患者人群基数大、药物研发成熟度高,以及医保政策推动下用药可及性的提升。随着新一代EGFR抑制剂、ADC药物等新型疗法的商业化落地,未来市场格局将逐步向多靶点、多产品的方向演变,但EGFR靶点在短期内仍将是肺癌靶向治疗的核心支柱。
8. 中国肺癌热门靶点代表药物累计销售额结构分析(2/3)
肺癌热门靶点代表药物2020-2025H1医院端累计销售额为685.32亿元,ALK靶点是中国肺癌靶向治疗领域的重要组成部分,其代表药物展现出明确的梯队格局与集中化特征。
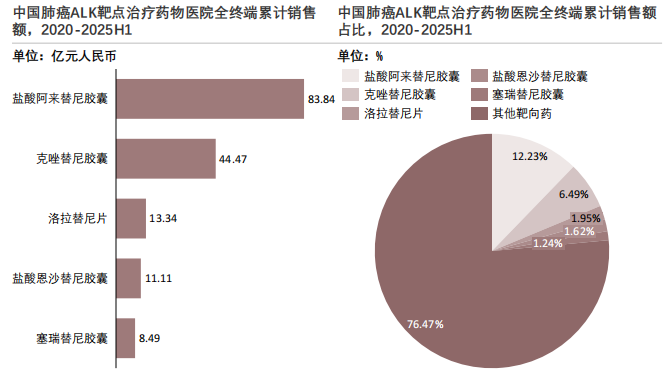
ALK靶点是中国肺癌靶向治疗领域的重要组成部分,在2020至2025年上半年的医院端市场中,其代表药物展现出明确的梯队格局与集中化特征。
基于精准医疗渗透率提升、医保政策支持与研发迭代带来的全病程治疗需求,ALK靶点靶向药市场形成了层次分明的产品梯队。其中,盐酸阿来替尼胶囊以累计销售额83.84亿元位居首位,凭借卓越的血脑屏障穿透能力和一线治疗的标准地位成为核心驱动力。克唑替尼胶囊以44.47亿元的销售额作为第一代标杆,奠定了广泛的市场基础。恩沙替尼11.11亿元和塞瑞替尼8.49亿元作为第二代药物,通过差异化的疗效和性价比优势覆盖了耐药及基层患者需求。洛拉替尼片13.34亿元作为第三代补位品种,凭借解决G1202R等难治突变的能力,成为患者的"最后一道防线"。这一梯队精准适配了不同治疗阶段和经济能力的患者,共同推动了ALK靶点市场的稳步发展。
从市场格局来看,ALK靶点药物的头部效应显著,仅盐酸阿来替尼胶囊就贡献了32.23%的销售额,核心品种凭借其临床优势和医保准入占据了主要市场份额。
整体上,ALK靶点的市场集中度较高,除了上述核心品种外,其他药物合计占比相对有限,反映出该领域目前仍由少数成熟产品主导,新进入者和后续产品尚处于逐步放量的阶段。这一格局的形成,主要得益于ALK靶点药物的精准治疗效果、医保政策推动下的可及性提升,以及药企对该领域的持续投入。
随着新一代ALK抑制剂的研发推进和商业化落地,未来该靶点市场有望在保持头部集中的同时,迎来更多产品的竞争与迭代,但核心品种的市场地位在短期内仍将保持稳固。
9. 中国肺癌热门靶点代表药物累计销售额结构分析(3/3)
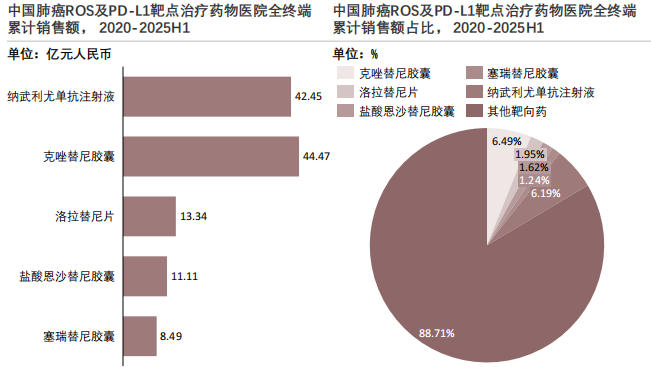
ROS及PD-1等其他靶点或治疗机制受患者基数、适应证范围及用药场景限制,整体市场规模相对有限,在肺癌系统治疗中更多体现为补充性和差异化。
查数据,找摩熵!数据来源:摩熵医药数据库
在ROS靶点相关用药中,受适应症人群规模限制,相关药物销售额整体较低。其中,克唑替尼胶囊作为该靶点的主要用药之一,累计销售额达44.47亿元,在肺癌靶向药整体市场中占比约6%。而洛拉替尼片及恩沙替尼胶囊的销售额均不足15亿元,进一步反映出ROS靶点因患者基数有限导致的市场规模瓶颈。
在PD-1靶点相关药品中,纳武利尤单抗注射液累计销售额为42.45亿元,在肺癌治疗领域占比同样约6%,虽与ROS靶点核心药物销售额处于同一量级,但该药物已在肺癌免疫治疗中形成较为稳定的应用场景,其市场需求更具持续性,且受益于免疫治疗适应症的持续拓展,未来仍具备一定的增长潜力。
总体而言,EGFR、ALK、ROS/PD-1三类靶点在肺癌治疗市场中呈现出显著的分化特征,核心差异集中在市场规模、患者基数与产品竞争力上。从市场价值与发展潜力来看,EGFR靶点依托患者基数与产品迭代优势,短期内仍将保持核心支柱地位,是肺癌靶向治疗市场的主要增长引擎。ALK靶点虽市场规模次之,但头部品种竞争格局稳固,随着新一代药物的迭代,有望维持稳健发展。ROS靶点受限于患者群体规模,市场增长空间相对有限,难以形成大规模扩容态势。而PD-1靶点虽当前销售额与部分小靶点靶向药物相当,但受益于免疫治疗适应症的持续拓展与联合治疗方案的成熟,未来增长潜力显著高于ROS等依赖小众人群的靶点,有望逐步拉开差距。
10. 中国肺癌靶向治疗药物市场规模分析
中国肺癌靶向治疗市场已迈入以精准分层、创新突破、支付优化为核心的高质量发展阶段。未来市场的增长将更多依赖于针对罕见靶点的原研创新药、新一代治疗方案,以及补充支付体系的完善。
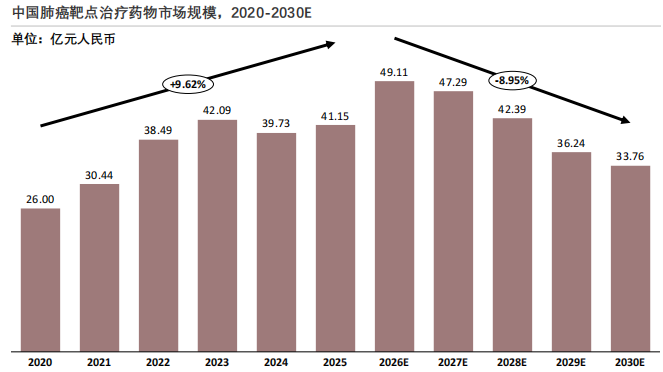
中国肺癌靶向药物治疗市场规模整体呈现先升后降、波动收窄的发展态势,行业从快速扩容逐步进入成熟调整期。肺癌靶向药物治疗市场规模在2020至2026年间持续攀升,从26.00亿元增至49.11亿元的阶段性峰值,这一阶段的增长主要得益于肺癌精准治疗需求的快速释放、EGFR/ALK等核心靶点药物的陆续上市,以及医保政策推动下用药可及性的显著提升。在此期间,靶向治疗逐渐成为肺癌治疗的主流方式之一,市场处于需求驱动的高速成长期。然而,在2026年达到49.11亿元的高点后,市场规模开始进入下行通道,虽有47.29亿元的短暂回稳,但整体呈现连续下滑趋势,最终降至33.76亿元。
市场规模下降的核心驱动因素:
(1)价格下探直接压缩规模,单个肺癌患者靶向药物治疗的年均花费从2020年的5.50万元降至2030年的0.75万元,医保谈判与带量采购的常态化推进显著降低了药价,虽提升了患者可负担性,但直接影响了市场规模的数值增长;
(2)产品迭代与竞争,随着三代EGFR-TKI、ADC药物等新一代疗法的商业化落地,传统靶向药的市场份额受到挤压,同时核心品种专利到期后仿制药涌入进一步加剧了价格竞争,行业进入新旧产品的更替调整期;
(3)支付端约束强化,DRG/DIP医保支付方式改革的深化,使得医疗机构在用药选择上更注重成本效益,进一步抑制了高价传统靶向药的市场空间。
三、乳腺癌靶向治疗药物市场分析
1. 乳腺癌疾病概述
乳腺癌(Breast Cancer)是源于乳腺导管上皮或小叶上皮的恶性肿 瘤,其发病与女性激素水平、遗传因素、生活方式等密切相关,核心病理机制为乳腺细胞的增殖失控与恶性转化。
激素调控异常是乳腺癌重要驱动因素。雌激素尤其是雌二醇可通过结合乳腺细胞内的雌激素受体ER,激活下游信号通路促进细胞增殖,当ER基因突变或表达异常时,会导致细胞对激素的敏感性异常升高,引发无序增殖。孕激素受体PR与ER协同作用,进一步调控细胞生长。遗传因素中,BRCA1/2基因突变是明确的高风险因素,携带该突变的女性乳腺癌发病风险显著升高,此类基因突变会导致DNA损伤修复功能缺陷,增加细胞癌变概率。此外,长期饮酒、肥胖、晚婚晚育、未哺乳、长期服用雌激素类药物等生活因素,会通过影响激素平衡或增加细胞损伤风险,间接促进乳腺癌发生。
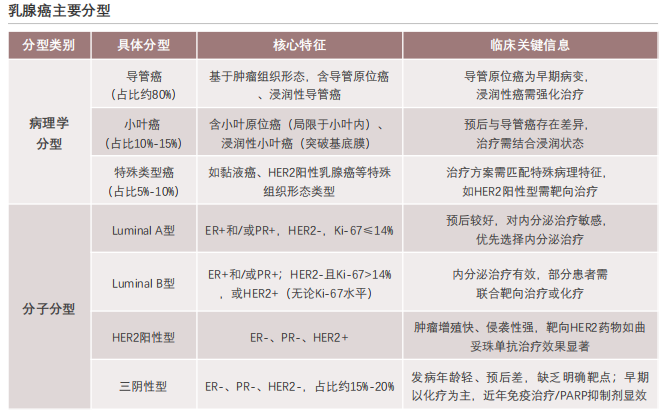
乳腺癌分型以分子分型为核心,直接指导治疗方案选择,是临床诊疗的关键依据。病理学分型主要基于肿瘤组织形态,分为导管癌、小叶癌、特殊类型癌。分子分型基于免疫组化检测ER、PR、HER2及Ki-67的表达情况分为四种类型。
2. 乳腺癌临床分期与诊疗方案
乳腺癌治疗策略逐级递进,治疗方案高度依赖分子分型如HER2、Luminal等,靶向药物贯穿各期,尤其在晚期治疗中发挥关键作用,体现精准医疗的全程应用。
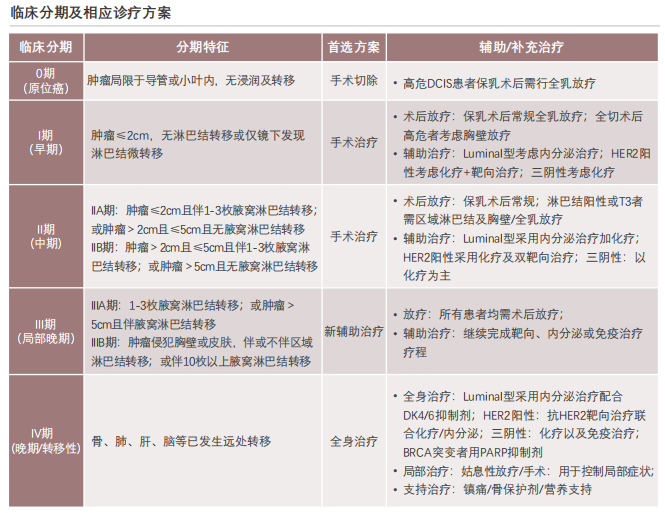
各分期靶向药适配方案:肺癌不同分期的靶向药应用各有侧重。Ⅰ至Ⅱ期高风险患者中,HER2阳性者术后使用曲妥珠单抗1年,联合帕妥珠单抗可降低复发风险,BRCA突变的Luminal型可加用奥拉帕利。Ⅲ期HER2阳性术前使用曲妥珠单抗+帕妥珠单抗+化疗进行缩瘤,术后继续双靶治疗,PD-L1高表达的三阴性患者可联合PD-1抑制剂。Ⅳ期HER2阳性一线选择T-DM1或DS-8201,Luminal型PIK3CA突变者使用阿培利司+氟维司群,多线耐药后可尝试ADC药物或参与新药临床试验。
3. 中国乳腺癌靶向治疗领域宏观环境分析
中国乳腺癌靶向治疗宏观环境向好,政策与技术双驱动,乳腺癌发病率居女性恶性肿瘤首位且呈年轻化,分子分型以HR阳性为主,靶向治疗市场潜力大。
乳腺癌是我国女性发病率最高的恶性肿瘤,且发病率呈逐年上升趋势。2024年,全国乳腺癌新发病例数已攀升至41.6万例,占女性全部恶性肿瘤新发病例的19.8%,相当于每五名女性癌症患者中约有一名为乳腺癌,凸显其作为女性健康主要威胁的严峻形势。目前,我国乳腺癌存量患者总数已突破300万人,庞大的患者群体对社会医疗资源及长期健康管理提出了持续且巨大的需求。从发病年龄结构分析,乳腺癌发病高峰明显集中在45至60岁的中年女性群体,该年龄段新发病例占比高达65%,是防治工作的重点人群。值得关注的是,40岁以下的年轻患者虽占比约为12%,但其发病率增长速度略高于整体人群,提示乳腺癌发病呈现一定的年轻化趋势,需引起公众与卫生部门的高度重视。
患者呈现"城市化、老龄化、年轻化"特征。城市化特征方面,城市女性乳腺癌发病率每10万人约68例,显著高于农村地区每10万人约32例,这与城市女性生活压力大、肥胖率高、晚婚晚育比例高、激素暴露时间长等因素相关。老龄化特征方面,60岁以上老年患者占比从2015年的28%升至2024年的35%,该群体因基础疾病多、身体耐受度低,对靶向治疗的安全性和耐受性要求更高。年轻化特征方面,40岁以下年轻患者占比逐步提升,且多表现为HER2阳性型或三阴性型,恶性程度高、预后较差,对创新靶向治疗需求迫切。
乳腺定期体检意识提升,筛查覆盖率扩大。2024年的统计数据显示,在25至65岁的核心适检女性中,坚持每年至少接受一次规范乳腺体检的比例已达到45%,相较于十年前的水平大幅提升了20个百分点,其中年龄介于35至55岁间且具备乳腺癌高危因素的女性群体中年度体检参与率高达68%,表明风险感知有效地转化为积极的预防行动。此外,得益于国家层面持续推动的癌症早诊早治等公共卫生项目,乳腺筛查服务的可及性得到了实质性改善,乳腺筛查渗透率已从2015年的22%增长至2024年的48%。这一拓展不仅体现了公共卫生服务的均等化进步,更有力地扩大了早期乳腺癌的发现网络,为提升整体治疗效果和患者生存率奠定重要基础。
乳腺疾病检出率:良性疾病占比高,早期乳腺癌检出率提升。乳腺体检中,良性疾病如乳腺增生、乳腺纤维瘤等检出率约为35%至40%,恶性肿瘤检出率约为1.2%至1.5%。值得关注的是,早期乳腺癌0期、I期检出率从2015年的38%提升至2024年的62%,这一变化得益于乳腺超声、乳腺X线钼靶、乳腺MRI等筛查技术的普及,以及居民对乳腺健康的重视。早期病例的增加为手术治疗、靶向辅助治疗提供了更多机会,显著改善患者预后。
4. 中国乳腺癌靶向治疗药物——在研管线靶点覆盖
乳腺癌在研靶点管线中多集中于I/Ⅱ期,靶向治疗仍处于“靶点拓展与机制验证”的阶段,后期管线的研发门槛仍较高,其中HER2的后期管线优势源于其靶点价值与临床数据积累的双重结果。
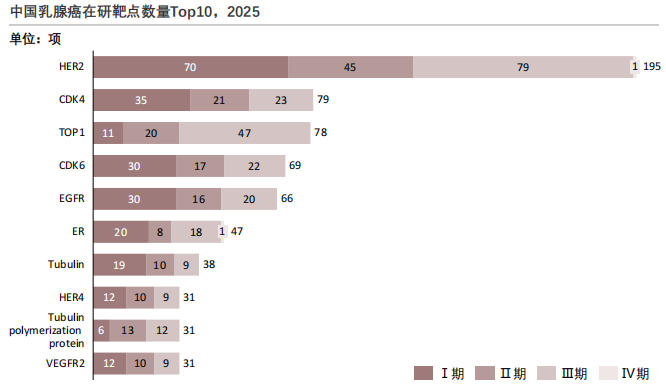
2025年中国乳腺癌在研靶点数量Top10
查数据,找摩熵!数据来源:摩熵医药数据库
- HER2:热门靶点的全周期研发垄断
HER2是乳腺癌靶向治疗的热门靶点。目前在研管线涵盖了单克隆抗体、小分子抑制剂、ADC药物等多种类型。HER2在研管线覆盖I-IV全研发阶段,这一布局源于乳腺癌中约20%患者存在HER2过表达,也得益于已有药物的临床验证基础:早期管线聚焦新机制如ADC药物迭代,后期管线则拓展适应症如晚期后线治疗,形成"迭代升级+场景延伸"的双轮驱动,凸显其在乳腺癌靶向治疗中的核心地位。
- CDK4/6、TOP1:新兴热点靶点的早期研发集中
CDK4(79个)、TOP1(78个)、CDK6(69个)等在研靶点构成第二研发梯队,但管线高度集中于I/Ⅱ期,其中CDK4的I/Ⅱ期占比超70%、TOP1达46%。这一特征与靶点的临床价值阶段相关:CDK4/6是HR+乳腺癌的关键靶点,但现有药物存在耐药问题,早期管线聚焦耐药后新机制。TOP1抑制剂则是化疗联合靶向的潜力方向,处于临床价值验证的早期阶段,反映出"成熟靶点补短板、潜力靶点探价值"的研发逻辑。
- ER、VEGFR2等:小众靶点的差异化布局
ER(47个)、VEGFR2(31个)等靶点管线规模较小,但呈现差异化特征:ER包含Ⅳ期管线,是基于其在HR+乳腺癌中的基础地位,布局方向为联合治疗或耐药后方案。VEGFR2则聚焦抗血管生成与靶向治疗的协同,虽处于早期阶段,但契合乳腺癌"多靶点联合"的治疗趋势。
5. 中国乳腺癌靶向治疗药物——企业在研管线分析
乳腺癌在研企业呈现出“头部高度集中、第二梯队加速追赶、跨国药企占据后期优势”的格局。未来2–3年,随着恒瑞、罗氏、阿斯利康等企业Ⅲ期项目陆续完成,乳腺癌领域有望迎来新药上市高峰。
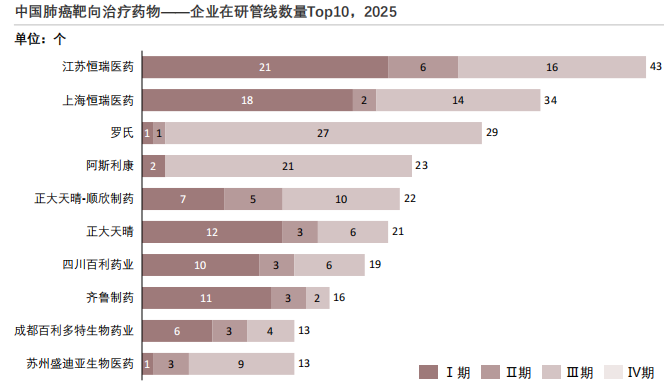
2025年中国肺癌靶向治疗药物——企业在研管线数量Top10
查数据,找摩熵!数据来源:摩熵医药数据库
本土头部企业优势明显,恒瑞医药(江苏及上海恒瑞)在研项目数量显著领先。江苏恒瑞在Ⅰ期(21项)和Ⅲ期(16项)均保持高位,显示其在乳腺癌领域具备"早期持续造血+后期重点突破"的完整研发体系。上海恒瑞同样在Ⅰ期(18项)和Ⅲ期(14项)形成梯队化布局,体现集团层面在乳腺癌适应症上的系统性投入。两家恒瑞系企业合计覆盖大量早期与关键临床项目,巩固了其在中国乳腺癌创新药研发中的龙头地位。
跨国药企以Ⅲ期项目为主,罗氏和阿斯利康的项目明显集中在Ⅲ期,Ⅰ期和Ⅱ期项目数量较少。跨国药企在中国乳腺癌领域更多承担全球同步或区域性关键临床研究角色,其产品多已在海外完成早期开发,中国临床主要服务于注册和适应症拓展。相比之下,其在国内原创早期管线布局相对有限。
本土企业呈现多层级梯队。正大天晴(集团及南京顺欣)、四川百利药业、齐鲁制药、成都百利多特及苏州盛迪亚等企业构成第二梯队与潜力梯队。正大天晴体系在Ⅰ期、Ⅱ期和Ⅲ期均有较为均衡的分布,体现其持续推进创新与改良型新药并行的策略。四川百利药业、齐鲁制药在Ⅰ期项目占比较高,显示其研发重点仍偏向早期创新或仿创结合阶段。苏州盛迪亚和成都百利多特虽总体项目数较少,但Ⅲ期项目占比相对突出,显示其可能聚焦少数核心品种进行突破。
6. 中国乳腺癌热门靶点药物年度销售额变化趋势
靶点结构看,乳腺癌药物市场呈现“HER绝对领先、ER次之、TOP稳定托底”的格局。未来HER靶点仍将是创新研发和商业化竞争的核心,ER靶点的增长则更多依赖差异化创新和联合治疗策略。
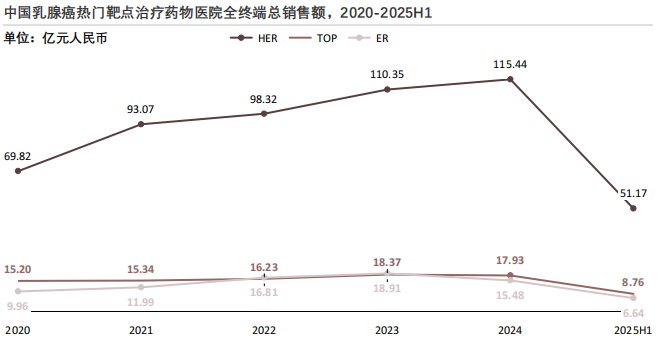
HER靶点药物始终占据销售额首位,且规模优势明显。2020至2024年,HER靶点代表药物医院端总销售额由69.82亿元增长至115.44亿元,复合增长趋势清晰。增长动力主要来自HER2阳性乳腺癌治疗中单抗、ADC等创新药物的持续放量,以及治疗线数前移带来的用药人群扩大。2025年上半年已实现51.17亿元,若下半年维持相近节奏,全年仍有望保持高位增长。目前,HER靶点已成为乳腺癌药物市场的"基本盘",短期内其主导地位难以被撼动。
TOP靶点药物销售额整体规模明显低于HER,但保持相对稳定。2020至2023年TOP靶点药物医院端总销售额由15.20亿元小幅增长至18.37亿元,2024年略回落至17.93亿元。究其原因,该靶点以传统化疗及相关改良制剂为主,临床应用成熟,但创新程度和价格弹性有限,导致增长空间受限。2025年上半年销售额为8.76亿元,预计全年表现以平稳为主,更多承担"基础治疗"角色。
ER靶点:弹性较大,受创新驱动明显。ER靶点药物在2020至2023年表现出较快增长,由9.96亿元提升至18.91亿元,显示内分泌治疗联合新机制药物(如CDK4/6抑制剂等)带来的显著放量效应。2024年回落至15.48亿元,提示市场竞争加剧、医保谈判及价格调整对销售额产生一定影响。2025年上半年为6.64亿元,若考虑政策与竞争因素,全年增速可能趋于温和。
从2020年至2024年,HER、TOP、ER三大热门靶点药物整体销售额呈持续增长态势。该趋势反映出乳腺癌治疗市场在患者基数扩大、诊疗规范完善及创新药渗透率提升等因素驱动下保持稳健扩容。2025年数据为上半年数据表现,其中HER销售额为51.17亿元,TOP销售额为8.76亿元,ER销售额为6.64亿元,在未覆盖全年情况下仍维持较高体量,显示市场需求具备较强韧性。
7. 中国乳腺癌热门靶点代表药物累计销售额结构分析(1/3)
乳腺癌热门靶点代表药物2020-2025H1医院端累计销售额为709.79亿元,其中靶向治疗药物市场呈现出明显的“头部集中”特征,HER2靶向治疗在乳腺癌药物市场中处于核心地位。
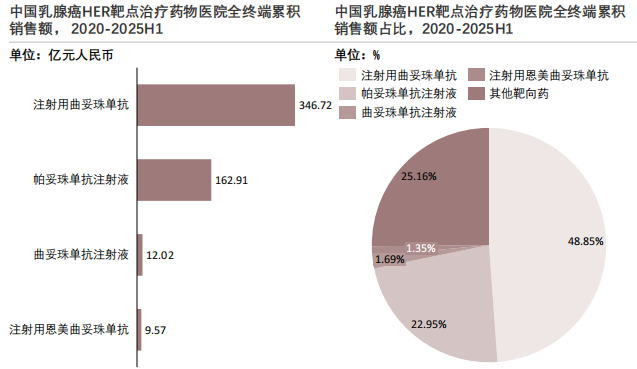
从销售结构看,HER2靶向药已成为乳腺癌用药市场的绝对核心板块。HER2靶点是中国乳腺癌靶向治疗的核心领域,在2020至2025年上半年的医院端市场中,其代表药物呈现出高度集中的竞争格局,头部品种的优势十分突出。注射用曲妥珠单抗以346.72亿元的累计销售额位居榜首,在HER2靶点药物中占比达48.85%,是驱动该市场的绝对核心品种。帕妥珠单抗注射液以162.91亿元的销售额紧随其后,占比22.95%,两者合计贡献了超过七成的市场份额,体现出头部效应极为显著的特征。此外,曲妥珠单抗注射液和注射用恩美曲妥珠单抗等产品形成了补充梯队,覆盖了不同治疗阶段的患者需求,为HER2阳性乳腺癌患者提供了从新辅助、辅助到晚期治疗的完整用药选择。这一格局的形成,主要得益于曲妥珠单抗等核心品种成熟的临床证据、广泛的患者人群基础,以及医保政策推动下用药可及性的大幅提升,使更多患者能够负担并获得规范化治疗。
未来,随着新一代HER2靶向疗法的商业化落地,该靶点市场将在保持头部集中的同时,迎来产品结构的迭代升级。新一代药物凭借其在晚期耐药患者中的卓越疗效,将逐步渗透后线治疗场景,并推动联合治疗方案的优化,为临床提供更多精准有效的治疗策略。不过,短期内这些创新产品难以撼动曲妥珠单抗等核心品种在一线治疗中的基石地位。因此,HER2靶点市场将呈现"核心品种稳固、创新产品补充"的双轨发展态势,整体市场规模将在产品迭代与需求释放的双重驱动下持续扩容,为乳腺癌治疗带来更丰富的选择和更广阔的增长空间。
8. 中国乳腺癌热门靶点代表药物累计销售额结构分析(2/3)
TOP靶点是中国乳腺癌治疗领域的重要组成部分,在2020年至2025年上半年的医院端市场中,其代表药物呈现出“头部集中、整体规模有限”的特征,与HER2等核心靶点的市场体量存在差距。
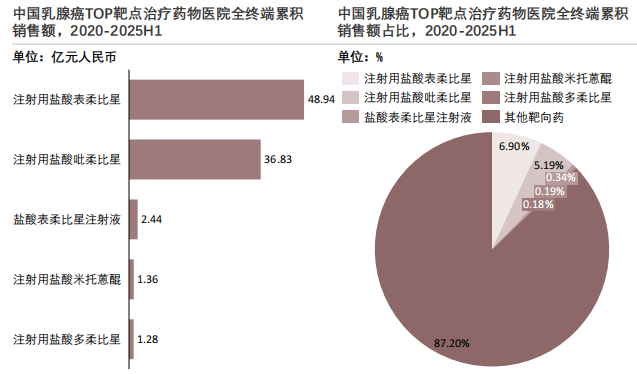
TOP靶点是中国乳腺癌治疗领域中以传统细胞毒类药物为核心的细分赛道。从市场占比来看,TOP靶点药物在乳腺癌整体靶向治疗市场中的占比不足13%,其中核心品种注射用盐酸表柔比星占比仅为6.90%,反映出该靶点并非乳腺癌治疗的主流选择,更多作为特定场景下的补充方案。这一市场格局的形成,是临床定位、技术迭代与政策环境共同作用的结果。
TOP靶点药物以蒽环类等传统化疗药物为主,其临床定位更多集中在早期乳腺癌的辅助治疗或新辅助治疗联合方案中,或适用于无法耐受新型靶向药物的患者人群。随着HER2靶向治疗、CDK4/6抑制剂联合内分泌治疗以及免疫疗法等新型方案的普及,TOP靶点药物的一线治疗场景持续被压缩,仅在局部晚期或复发转移患者的后线治疗中保留稳定需求。其次,这类药物的研发成熟度较高,缺乏突破性的临床数据支撑,难以通过医保谈判等政策工具获得价格与销量的双重突破,导致市场规模长期维持在稳定但有限的水平。
未来,随着ADC药物、新一代SERD抑制剂以及双特异性抗体等创新方案的持续落地,TOP靶点药物的市场份额可能进一步收窄。但在特定患者人群和治疗场景中,如早期乳腺癌的标准化疗方案、部分基层医疗机构的临床实践,以及作为新型疗法的联合用药选择,这类药物仍将保持稳定的临床需求,维持其补充性治疗的地位。整体而言,TOP靶点市场已进入成熟稳定期,未来增长将主要依赖患者人群的自然增长与基层市场的渗透,而非突破性的产品创新或政策驱动。
9. 中国乳腺癌热门靶点代表药物累计销售额结构分析(3/3)
靶向药已成为乳腺癌治疗市场的核心驱动力,随着联合用药和ADC等创新靶向药物持续放量,市场正由基础用药向高价值、精准治疗加速升级。
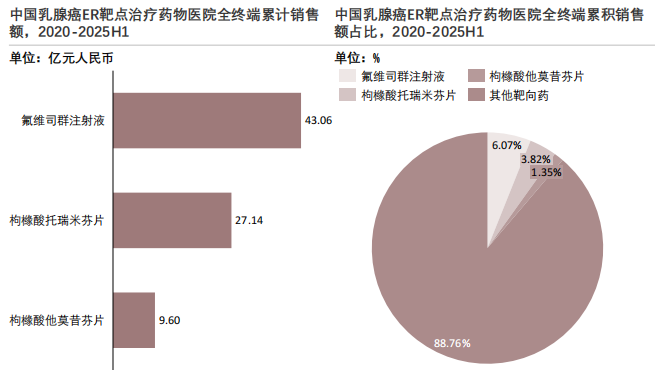
ER靶点代表药物展现出"以成熟品类为主、依赖联合治疗、市场增速平缓"的独特发展轨迹,与HER2等靶向治疗靶点的增长逻辑形成鲜明差异。在产品表现上,氟维司群注射液以43.06亿元的累计销售额成为ER靶点的核心单品,在该细分市场中占比6.07%,枸橼酸托瑞米芬片以37.14亿元的销售额紧随其后,占比5.22%,枸橼酸氯米芬片以9.60亿元的销售额形成补充梯队。三者合计占据了ER靶点药物的绝大多数市场份额,头部效应极为突出。从整体市场占比来看,ER靶点药物在乳腺癌全终端治疗市场中的占比仅约11.29%,这一数据既体现了其作为内分泌治疗核心的稳固地位,也反映出其在整个乳腺癌治疗体系中仍属于"基础性、非爆发性"的赛道,市场规模与增长动能均不及HER2等靶向治疗靶点。
未来,ER靶点市场的增长动力将主要来自创新药物的商业化落地以及乳腺癌早期筛查率提升带来的需求释放。一方面,新一代SERD抑制剂、PROTAC等创新药物的商业化落地,将在耐药患者后线治疗场景中打开新的增长空间,并推动联合治疗方案的优化升级。另一方面,随着乳腺癌早期筛查的普及和基层诊疗能力的提升,内分泌治疗的患者渗透率将进一步提高,为传统药物带来持续的增量需求。整体而言,ER靶点市场将呈现"基础盘稳固、创新点突破"的发展态势,其作为乳腺癌治疗体系中"压舱石"的作用将愈发凸显,但短期内难以改变其作为补充性赛道的市场定位。
10. 中国乳腺癌靶向治疗药物市场规模分析
从2020-2030年的预测数据来看,中国乳腺癌靶向治疗药物市场呈现结构性分化特征,不同亚型的市场规模走势差异显著,整体行业正经历从规模扩张到结构优化的转型。
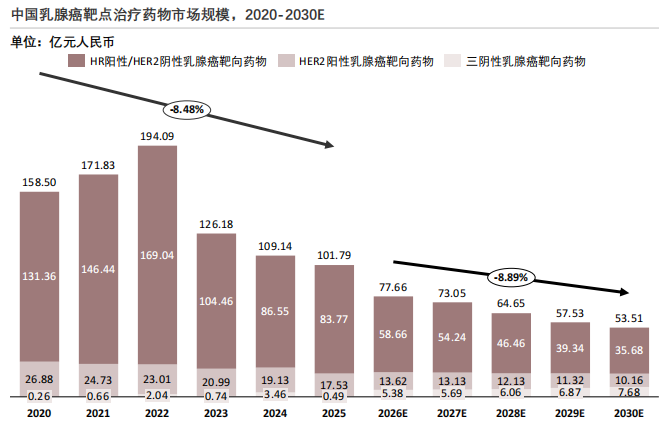
HER2阳性乳腺癌靶向药市场:政策驱动下的规模收缩。HER2阳性乳腺癌靶向药市场在2020至2022年呈现阶段性增长,规模从158.50亿元攀升至194.09亿元,这主要得益于早期曲妥珠单抗等核心药物的放量以及帕妥珠单抗等联合疗法的临床推广。2022年之后,市场进入持续下行通道,预计到2030年将萎缩至53.51亿元,较峰值下降约72%。其中,变化的核心原因在于医保谈判与带量采购的常态化推进,价格下探直接压缩了市场规模的数值增长。
HR阳性/HER2阴性乳腺癌靶向药市场:快速增长后的持续调整。HR阳性/HER2阴性乳腺癌靶向药市场在2020至2022年处于高速成长期,这一阶段的增长主要依赖CDK4/6抑制剂等新型药物的上市与医保准入。2022年后市场规模持续下滑,预计2030年将降至35.68亿元。这一趋势主要由价格因素主导,同时,新一代SERD、PROTAC等药物的研发突破对现有CDK4/6抑制剂市场形成冲击,行业进入新旧产品的快速更替期,进一步抑制了传统靶向药的市场空间。
三阴性乳腺癌靶向药市场:创新驱动下的波动增长。三阴性乳腺癌靶向药市场规模虽整体偏小,但波动最为剧烈,2020至2030年间多次出现规模跳升与回落,预计2030年将增长至7.68亿元,是唯一呈现长期增长趋势的亚型。这一增长主要由创新突破驱动,TROP2-ADC、PD-1/PD-L1抑制剂等新型疗法的商业化,带动市场规模阶段性扩张。
四、结直肠癌靶向治疗药物市场分析
1. 结直肠癌疾病概述
结直肠癌(Colorectal Cancer,CRC)是源于乳腺导管上皮或小叶上皮的恶性肿瘤,其发病与女性激素水平、遗传因素、生活方式等密切相关,核心病理机制为乳腺细胞的增殖失控与恶性转化。
结直肠癌发病率稳步上升,晚期病例占比仍较高。结直肠癌是我国发病率第三、死亡率第五的恶性肿瘤,2024年全国新发病例达38.3万,占所有恶性肿瘤新发病例的8.0%,存量患者超过250万。与其他癌种相比,结直肠癌早期症状不明显,约40%的患者确诊时已处于Ⅲ期或Ⅳ期,晚期病例治疗难度大、预后差,对靶向治疗和免疫治疗需求迫切。
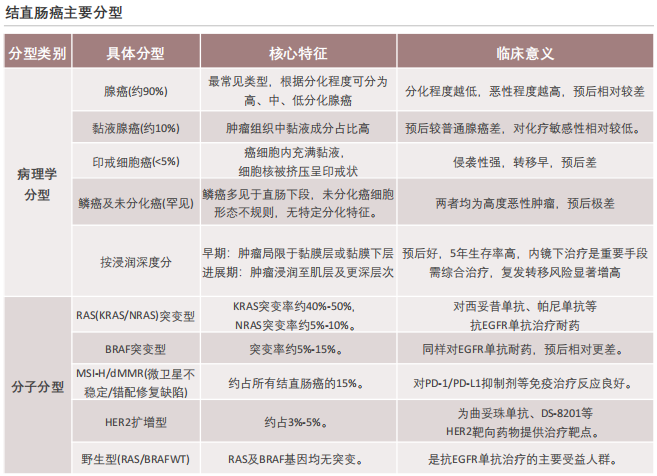
分子分型与治疗需求高度相关。结直肠癌分子分型中,RAS/BRAF野生型占比约40%至50%,RAS突变型占比约40%至50%,BRAF突变型占比约5%至15%,MSI/dMMR型占比约15%,HER2扩增型占比约3%至5%。不同分子分型的治疗方案差异显著:RAS/BRAF野生型对西妥昔单抗等抗EGFR单抗靶向药物敏感,是靶向治疗的主要受益人群;RAS/BRAF突变型对EGFR单抗耐药,需采用化疗联合抗VEGF单抗如贝伐珠单抗治疗;MSI/dMMR型对免疫检查点抑制剂反应良好,免疫治疗已成为该类患者的重要治疗选择;HER2扩增型抗HER2靶向药物如曲妥珠单抗治疗效果显著,为该类患者提供了新的治疗方向。
2. 结直肠癌临床分期与诊疗方案
结直肠癌靶向药治疗前主要用于Ⅳ期患者,需根据RAS/BRAF、MSI、HER2等基因检测结果选择对应的靶向治疗方案,对于0期、I期、Ⅱ期及绝大多数IⅡ期患者,手术和化疗仍是标准治疗手段。
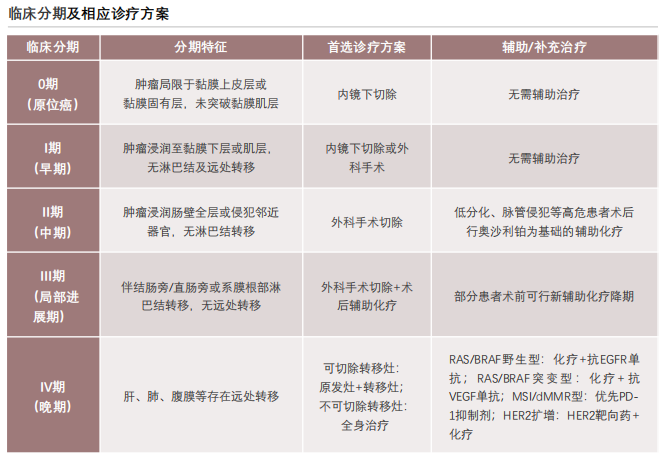
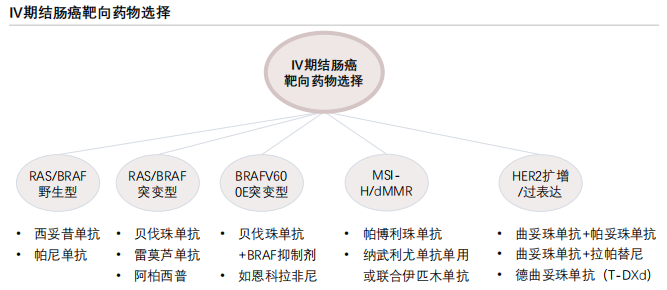
3. 中国结直肠癌靶向治疗领域宏观环境分析
当前我国结直肠癌防控面临多重挑战,部分人群仍保持高脂低纤的饮食偏好,叠加缺乏运动的生活方式,推高了发病风险,疾病呈现“老龄化、城市化”特征。
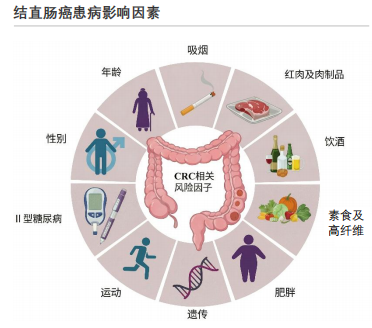
遗传因素在结直肠癌发病中占据重要地位。家族性腺瘤性息肉病(FAP)与遗传性非息肉病性结直肠癌(Lynch综合征)是典型的遗传性疾病。FAP由APC基因突变引起,患者肠道会出现大量腺瘤,若未及时干预,几乎100%会发展为癌。Lynch综合征则因MLH1、MSH2等DNA错配修复基因缺陷,导致细胞DNA复制错误无法修正,引发肿瘤易感性。
环境与生活方式因素中,高脂肪、低纤维饮食会改变肠道菌群结构,增加次级胆汁酸生成,刺激肠黏膜细胞增殖。肥胖、饮酒、吸烟会通过氧化应激损伤DNA,慢性炎症如溃疡性结肠炎、克罗恩病长期刺激肠黏膜,也会提高癌变风险。分子层面,除APC、DNA错配修复基因外,KRAS、BRAF、PI3K等基因突变及微卫星不稳定MSI、染色体不稳定CIN等分子异常,共同驱动肿瘤细胞增殖、凋亡抑制及侵袭转移。
饮食习惯:高脂肪、低纤维饮食仍较普遍,增加发病风险。中国居民饮食习惯虽逐步向健康化转变,但部分人群仍保持高脂肪、低纤维的饮食特征。2024年数据显示,城市居民日常饮食中肉蛋禽鱼占比约35%,蔬菜、水果、粗粮占比约45%。农村居民肉蛋禽鱼占比约28%,蔬菜、水果、粗粮占比约40%。与推荐的"蔬菜、水果、粗粮占比50%以上"相比仍有差距。此外,我国居民饮酒率约为25%,吸烟率约为28%,肥胖率约为18%,这些因素均会通过不同机制增加结直肠癌发病风险,为疾病预防和治疗带来挑战。
运动时长:缺乏运动人群占比高,健康生活方式待普及。随着城市化进程加快,我国居民久坐时间延长,缺乏运动成为普遍现象。2024年数据显示,18至65岁居民中,每周运动时长≥150分钟的比例仅为32%,45%的居民每周运动时长不足60分钟,23%的居民几乎不运动。缺乏运动可导致肥胖、肠道蠕动减慢,增加结直肠癌发病风险,而健康的生活方式如规律运动、均衡饮食有助于降低发病风险。
4. 中国结直肠癌靶向治疗药物——在研管线靶点覆盖
结直肠癌在研管线研发方向高度聚集研发管线呈现出多靶点并行、经典靶点主导、免疫与血管生成靶点长期占优的整体特征,研发重心正由单一机制向组合化和精细化方向演进。
2025年中国结直肠癌在研靶点数量Top10
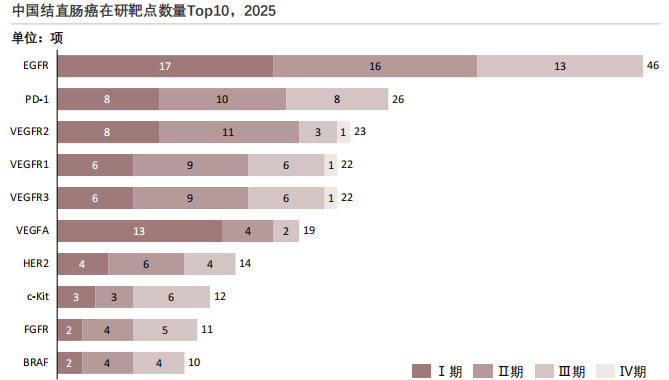
查数据,找摩熵!数据来源:摩熵医药数据库
EGFR靶点研发资源高度集中,免疫治疗已从探索期逐步进入验证和优化阶段。热门靶点EGFR(累计46项)研发成熟度最高,VEGFR2(23项)、VEGFR1(22项)、VEGFR3(22项)三项靶点累计研究数量接近,且Ⅱ期研究占比均为各阶段最高,表明该家族靶点正处于临床疗效验证关键期,是抗血管生成治疗的核心布局方向。在免疫治疗靶点方面,PD-1相关在研项目在各阶段分布相对均衡(Ⅰ期8项、Ⅱ期10项、Ⅲ期8项),考虑到PD-1单药在微卫星稳定型(MSS)结直肠癌中的疗效限制,当前研发更多聚焦于联合治疗方案和适应症细分。
血管生成相关靶点整体呈现出项目数量多、技术路径成熟的特点。VEGFR2、VEGFR1和VEGFR3在Ⅰ期和Ⅱ期均保持较高数量,且均已有Ⅳ期项目(各1项),显示部分产品已进入上市后研究或真实世界阶段。其中VEGFR2在Ⅱ期项目数量达到11项,但Ⅲ期仅3项,提示该领域竞争激烈、淘汰率较高,企业更多在早中期进行差异化验证。VEGFA靶点则呈现"前高后低"的特征,Ⅰ期项目多达13项,但Ⅲ期仅2项,反映传统VEGF通路创新空间逐步收窄,研发重心正在向受体或联合靶点转移。
HER2及其他驱动基因靶点在结直肠癌特定人群中的精准治疗价值逐步受到重视。HER2在研项目数量适中,但总体仍属于小众亚型驱动。BRAF和FGFR靶点在Ⅱ期和Ⅲ期项目数量相对均衡,表明针对特定分子分型的靶向治疗正在稳步推进,但整体规模仍受限于患者人群占比。此外,c-Kit靶点在Ⅲ期项目数量达到6项,高于其Ⅰ期和Ⅱ期,说明部分传统靶点已积累较成熟的临床证据,正集中向注册阶段推进,更多体现为存量优化型研发,而非大规模早期创新。
5. 中国结直肠癌靶向治疗药物——企业在研管线分析
中国结直肠癌在研企业的研发格局呈现出本土企业与跨国药企并存、管线规模分化明显、后期项目向少数企业集中的特征,整体仍处于由早中期向关键性临床推进的阶段。
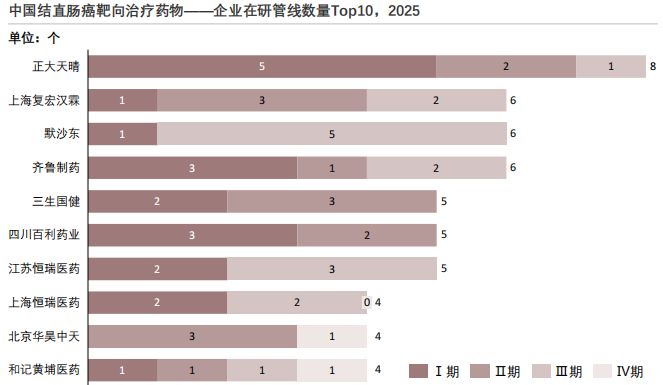
2025年中国结直肠癌靶向治疗药物——企业在研管线数量Top10
查数据,找摩熵!数据来源:摩熵医药数据库
早期管线规模型企业:正大天晴为代表。正大天晴在研项目数量最多,Ⅰ期、Ⅱ期和Ⅲ期分别为5项、2项和1项,体现其通过多早期项目并行布局来分散研发风险、提升成功概率的策略。但其后期项目占比较低,短期内更多体现为管线储备优势,中长期仍需加快核心品种向Ⅲ期转化。
中后期推进型企业:复宏汉霖与恒瑞体系。上海复宏汉霖在Ⅱ期和Ⅲ期项目上布局均衡(Ⅱ期3项、Ⅲ期2项),研发路径相对清晰,聚焦具备明确临床定位的生物药产品。江苏恒瑞医药和上海恒瑞医药的Ⅲ期项目分别达到3项和2项,显示其在结直肠癌领域已有重点品种进入注册关键阶段,研发策略偏向集中资源实现突破。
跨国药企策略:默沙东后期优势突出。默沙东的在研项目几乎全部集中在Ⅲ期(5项),早期项目布局极少,反映其在中国结直肠癌领域主要依托全球成熟管线推进关键性临床和注册,具备明显的后期竞争优势,但本土早期创新参与度较低。
探索与培育型企业:三生国健与四川百利。三生国健和四川百利药业的项目主要分布在Ⅰ期和Ⅱ期,尚未进入Ⅲ期,说明其仍处于早期探索和临床验证阶段。未来能否实现突破,取决于靶点差异化程度及联合治疗策略的临床验证结果。
6. 中国结直肠癌热门靶点药物年度销售额变化趋势
中国结直肠癌靶向药市场中,EGFR类药物靠临床需求扩容持续增长,VEGFR类因产品周期与替代风险呈收缩且被拜耳垄断,未来前者将迎生物类似药冲击、后者待新药与国产替代破局。
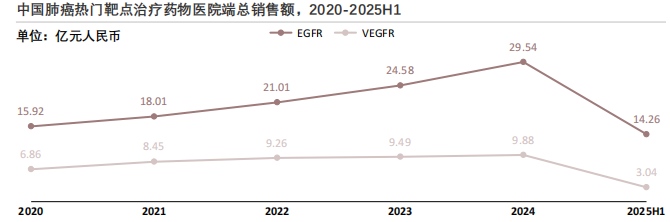
EGFR类持续增长。2020至2024年,EGFR靶向药物西妥昔单抗注射液的医院端销售额呈持续上升趋势,从2020年的15.92亿元增至2024年的29.54亿元,年复合增速约16.8%。2025H1仍保持14.26亿元的较高规模,销售额的持续走高,受结直肠癌患者人群基数快速增长以及临床适应症拓展的双重驱动。目前,西妥昔单抗的原研专利已逐步到期,未来市场3至5年内将受到生物类似药的上市冲击。
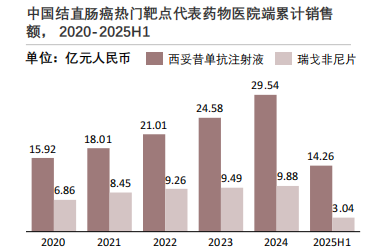
VEGFR类高位回落。VEGFR靶向药物瑞戈非尼片的销售额呈稳中小幅波动后下滑趋势,2020至2024年销售额维持在6.86亿至9.88亿元区间,2025H1销售额为3.04亿元,预计2025年全年销售额在7亿至8亿元之间,或受市场竞争、用药结构调整等因素影响。
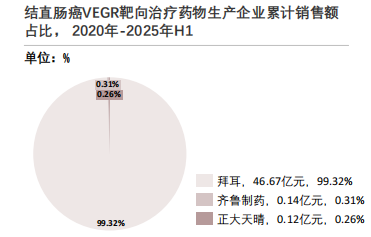
VEGFR药物市场格局拜耳一家独大。瑞戈非尼作为拜耳原研产品,早年通过专利壁垒占据先发优势,2020至2025H1,VEGFR靶点治疗药物的总销售额中,拜耳占比高达99.19%,齐鲁制药、正大天晴的份额极低,呈现"单企业垄断"的市场结构。
7. 中国结直肠癌靶向治疗药物市场规模分析
中国结直肠癌靶向治疗药物市场在2020-2030年间呈现规模持续收缩、患者人数波动增长的分化特征,反映出政策调控、技术迭代与患者需求之间的复杂平衡。
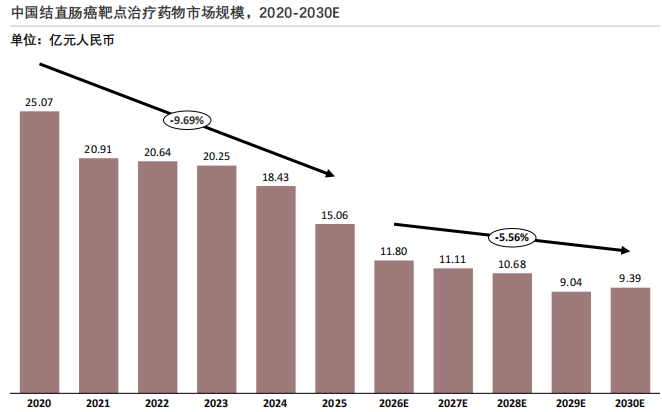
受医保谈判、集采改革影响,结直肠癌传统靶向药价量齐跌,叠加新一代药物及仿制药竞争,市场规模预计逐年收缩。结直肠癌靶向药物市场规模从2020年的25.07亿元持续收缩,预计到2030年将降至9.39亿元,较峰值下降约63%。这一趋势主要由多个因素驱动,其中,价格下探是核心因素。单个患者年均花费从2020年的3.90万元降至2030年的0.90万元,医保谈判与带量采购的常态化大幅降低了药价。虽然"以价换量"提升了患者可及性,但直接压缩了市场规模的数值增长。同时,产品迭代与竞争分流,随着新一代靶向药如TKI抑制剂、ADC药物的商业化落地,传统靶向药的市场份额受到挤压,而核心品种专利到期后,仿制药涌入进一步加剧了价格竞争。此外,DRG/DIP医保支付方式改革的深化,使得医疗机构在用药选择上更注重成本效益,进一步抑制了高价传统靶向药的市场空间。
结直肠癌临床需求仍在,未来行业将从规模扩张转向高质量发展,原研创新药及补充支付完善将成长期增长关键。尽管市场规模持续收缩,但患者人数的增长表明临床需求依然存在。未来行业将从单纯的规模扩张,转向以创新突破、精准分层、支付优化为核心的高质量发展阶段。具有临床价值的原研创新药,尤其是针对耐药机制和罕见靶点的药物,以及商保、惠民保等补充支付方式的完善,将成为推动市场长期增长的关键。
五、实体瘤治疗领域典型企业案例分析
1. 中国实体瘤研发领域典型企业分析
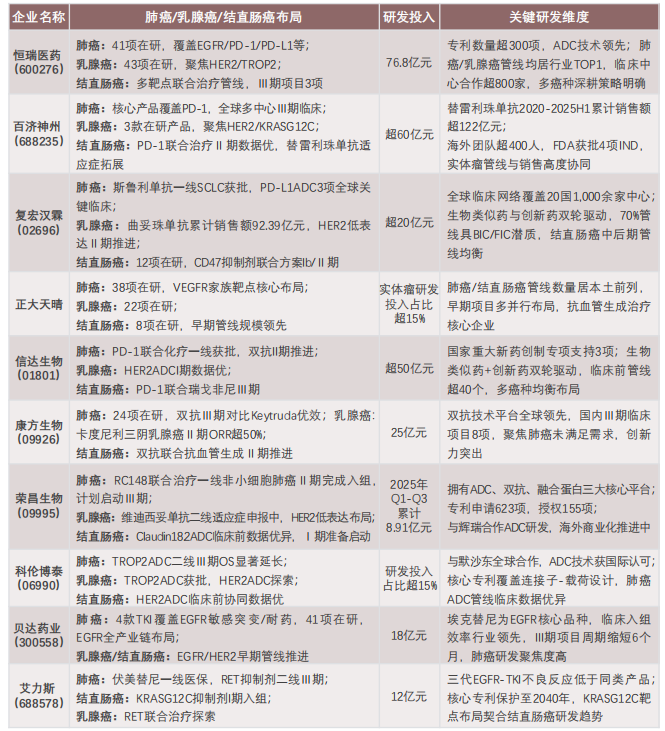
TOP10企业占据国内三大癌种靶向药在研管线的62%,恒瑞、百济神州、复宏汉霖凭借“全癌种+全靶点”布局稳居第一梯队,复宏汉霖、信达生物等企业以技术平台差异化突围。
2025年中国实体瘤靶向治疗药物代表生产企业研发实力对比
2. 中国实体瘤靶向治疗领域核心药企研发能力——恒瑞医药
恒瑞医药研发策略呈现“多癌种覆盖+重点癌种深耕”的特点,形成了研发驱动与商业兑现相辅相成的战略格局,兼具现有现金流支撑和未来增长潜力。
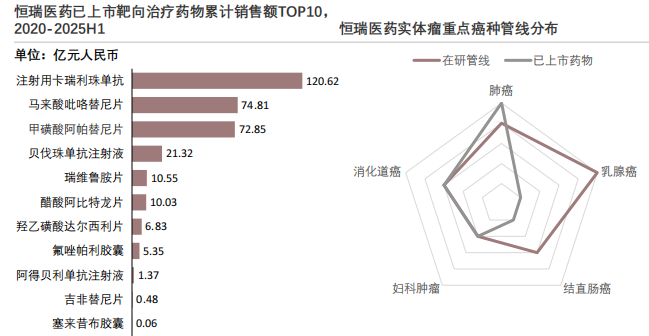
恒瑞医药的研发策略呈现多癌种覆盖的特点。注射用卡瑞利珠单抗和甲磺酸阿帕替尼片等药物均在多癌种开展临床试验,且晚期数量较多,说明企业在广泛适应症探索的同时,注重商业化潜力较高的晚期临床布局。此外,乳腺癌和卵巢癌为研发重点,相关药物如SHR-A1811、马来酸吡咯替尼片和氟唑帕利胶囊在各临床阶段均有较大投入,体现企业在核心癌种市场的深耕策略,同时也具备一定早期创新能力。
查数据,找摩熵!数据来源:摩熵医药数据库
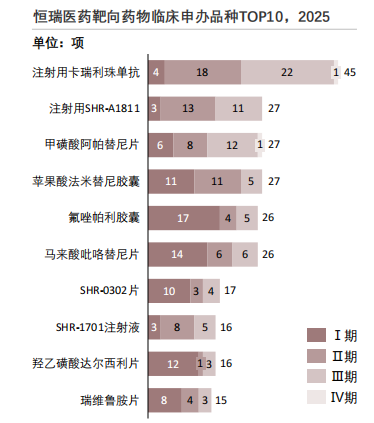
恒瑞医药的研发技术储备全面。卡瑞利珠单抗和马来酸吡咯替尼片临床阶段覆盖广且晚期数量多,说明企业具有将研发成果高效推进至上市的能力;氟唑帕利胶囊、SHR-A1811等早期在研药品显示企业在新适应症和早期创新上具备潜力。总体来看,企业能够实现研发管线的多元化布局,兼顾商业化收益与创新能力,技术平台成熟且临床推进体系完整,具备持续竞争优势。
3. 中国实体瘤靶向治疗领域核心药企研发能力——复宏汉霖
复宏汉霖构建了覆盖乳腺癌、肺癌等多个高发实体瘤病种的全维度管线,形成“生物类似药筑牢基础、创新药引领突破、联合疗法拓展边界”的三层布局。
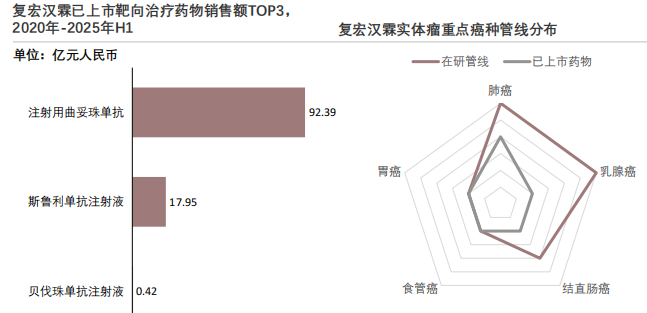
中后期管线稳步推进,核心产品具备商业化潜力。斯鲁利单抗注射液以及重组抗EGFR人源化单抗注射液等关键产品,在临床开发阶段中,Ⅱ期及Ⅲ期临床试验项目数量占据显著比例,标志着企业在免疫检查点抑制剂和经典靶向抗体这两大重要治疗领域的研发已进入收获在即的中后期,为未来的市场上市和商业化放量奠定了坚实基础。同时,企业也在积极拓展下一代创新疗法,多款双特异性抗体及联合制剂均已进入临床研究阶段,可见企业不仅深耕现有成熟靶点,更在创新药物开发上进行了前瞻性的积极探索,旨在覆盖当前尚未被满足的、更为广泛的肿瘤临床治疗需求。
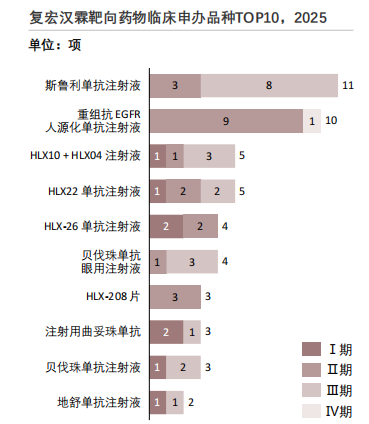
具备高效的临床转化与精准的价值挖掘能力。以复宏汉霖核心产品斯鲁利单抗为例,其通过涵盖11项临床研究的庞大开发计划,成功在小细胞肺癌这一治疗难题领域确立了突破性免疫治疗药物的地位。此外,企业还通过策略性探索联合疗法以及开发差异化新剂型等手段,系统性拓展药物的应用边界,实现单一药物产品临床价值与市场潜力的最大化,展现了企业具备覆盖药物研发全链条的深厚实力与清晰战略思维。
4. 中国实体瘤靶向治疗领域核心药企研发能力——百济神州
百济神州实体瘤领域布局呈现一超多强的竞争格局,替雷利珠单抗贡献主要销售额,同时在肺癌、乳腺癌、卵巢癌等实体瘤领域布局多款靶向药,预计未来2~3年将有多个潜在上市产品。
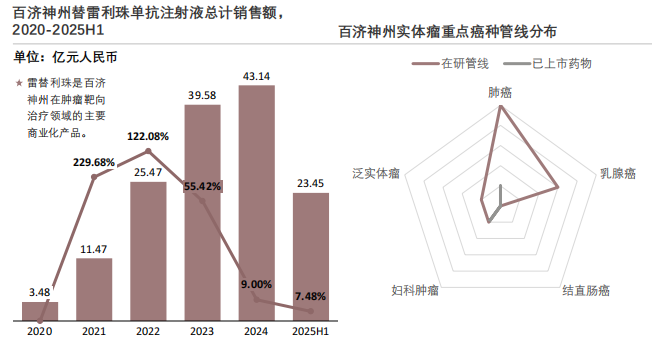
替雷利珠单抗是企业实体瘤靶向药商业化的核心支柱。替雷利珠单抗作为PD-1抑制剂是企业商业化体系的核心支柱。2020至2025H1期间,该产品销售额从3.48亿元增长至2024年的43.14亿元,2025H1达到23.45亿元。尽管销售增速从早期的百余个百分点逐步回落至个位数,但其在肺癌、乳腺癌等主要适应症的市场渗透率已形成显著优势,为企业提供了稳健的现金流和研发投入基础。
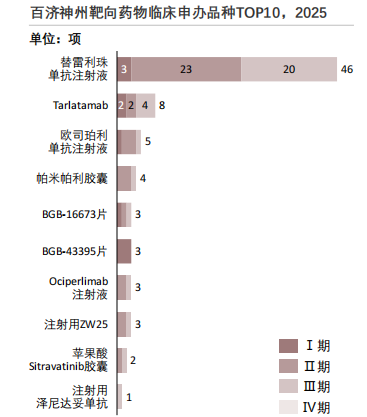
百济神州在研管线完全聚焦实体瘤,呈现出核心癌种集中、研发与销售高度协同的特征。在核心癌种层面,肺癌布局5款产品,乳腺癌布局3款,覆盖PD-1、HER2、KRASG12C等主流及前沿靶点,在研管线的重点适应症与已上市产品覆盖高度重合,实现"上市即对接成熟渠道"的市场转化效率最大化。
六、实体瘤靶向治疗行业前景与挑战分析
1. 生物类似药冲击风险
生物类似药的快速崛起正深刻改变中国实体瘤靶向治疗药物市场格局,核心品种专利到期引发的市场竞争重构,将成为未来3-5年行业发展的关键变量。
实体瘤靶向治疗代表药物原研及生物类似药市场竞争
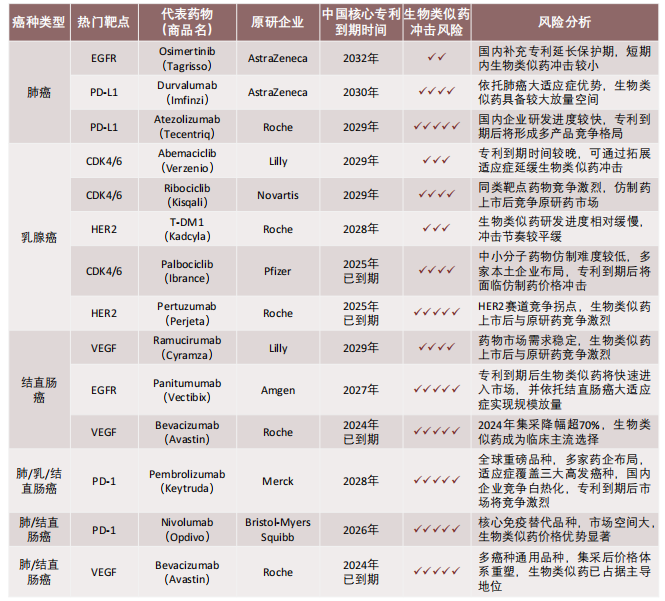
肺癌、乳腺癌和结直肠癌领域的生物类似药冲击风险将在专利到期与政策放量的共同作用下集中释放。HER2抗体和VEGF抗体已率先跨过中国核心专利到期节点,在集采和医保政策推动下,生物类似药快速放量,重塑价格体系并持续挤压原研药市场空间。同时,PD-1/PD-L1免疫检查点抑制剂预计将在2028年前后集中迎来中国专利到期窗口,相关品种覆盖三大高发癌种、市场体量庞大,一旦专利失效,生物类似药有望凭借价格优势迅速下沉至基层及联合治疗场景,对原研产品形成显著竞争压力。
2. 高发癌种未来产品技术展望
肺癌、乳腺癌、结直肠癌靶向治疗已形成成熟的核心靶点布局体系,未来产品技术将聚焦罕见靶点突破、耐药机制攻克、剂型创新升级三大方向,通过精准化、多元化的研发策略,填补临床未满足需求。
肺癌靶向治疗将以拓展靶点广度、攻克耐药深度、丰富治疗维度为核心,全面拓宽精准治疗的覆盖人群与应用场景。针对EGFR exon20插入、MET扩增/外显子14跳跃、RET融合、NTRK融合等罕见驱动事件,高选择性抑制剂及双抗将成为研发重点,并依托NGS检测体系实现靶点检出与精准用药的闭环管理。围绕EGFR-TKI、ALK抑制剂获得性耐药,三代及新一代靶向药、EGFR/c-MET双抗有望构建更加合理的序贯治疗策略,联合抗血管生成等方案用于延缓耐药发生。同时,TROP2-ADC等新型偶联药物为无明确驱动突变或经多线治疗失败患者提供新的治疗可能。
乳腺癌靶向治疗将以分型精准化、靶点多元化及剂型创新化为核心,覆盖不同分子亚型及获得性耐药场景,逐步构建全周期精准治疗体系。当前研发与临床实践主要聚焦于三阴性乳腺癌、HER2低表达及HR阳性耐药三大方向:三阴性乳腺癌以TROP2-ADC为代表的新型偶联药物为核心,联合免疫治疗提升疗效,PARP抑制剂逐步向BRCA突变早期治疗拓展,Claudin18.2等新靶点仍处于探索阶段。HER2低表达乳腺癌以ADC为主要突破口,新一代HER2靶向药物及免疫重定向双抗正处于临床研究中。HR阳性耐药治疗策略则围绕CDK4/6抑制剂联合新型SERD展开,并通过PI3KCA、AKT等通路抑制剂及PROTAC等新机制药物不断丰富治疗选择。
结直肠癌治疗将以罕见靶点突破、免疫治疗联合升级及局部-全身协同为核心,逐步构建覆盖多分子分型与不同病程阶段的精准治疗体系。针对KRAS G12C、BRAF V600E等驱动突变,通过靶向药物联合EGFR抑制剂等方案优化疗效,HER2扩增靶向治疗进一步填补小众分型的治疗空白。在免疫治疗方面,MSI-H/dMMR人群免疫治疗逐步向早期治疗阶段前移,而MSS型结直肠癌则通过联合抗血管生成药物、化疗或多靶点药物探索提高免疫响应率。同时,靶向或免疫治疗联合手术、消融等局部治疗手段,有助于实现转移灶控制与疾病长期管理,肠道微生物组调控等新策略仍处于探索阶段。
以上内容均来自头豹研究院{ 2026年中国实体瘤流行病学趋势及热门靶点药物市场表现洞察 },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论