作者:不二
- 2020.11.01-2020.11.08期间药审中心受理总量为220个,涉及品种142个。
- 12个1类新药申请获CDE受理。
- 新增11个按仿制药质量和疗效一致性评价品种申报的受理号。
1. 在审评阶段
根据健数科技中国药品审评数据,11月1号-11月8号期间共142个(按品种计,下同)药品获CDE承办,包括化药93个,生物制品33个,中药11个,以及体外诊断试剂1个。
近期CDE承办的申报临床新药,共计14个品种,其中化药8个,治疗用生物制品6个。另有9个品种提交一致性评价。
数据来源:健数科技中国药品审评数据库 (备注:按品种统计)
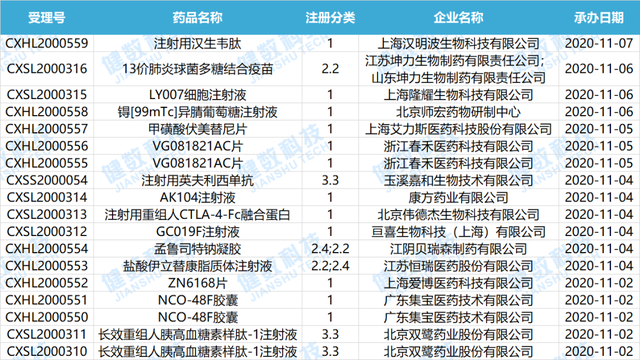
近期受理国产新药共计18个受理号,涉及15个品种15家企业。
下表为2020.11.01-2020.11.08新承办的新药药物情况。
数据来源:健数科技中国药品审评数据库
中国生物科技服务(08037.HK)控股下属公司上海隆耀生物科技提交LY007细胞注射液临床申请。LY007细胞注射液是一种嵌合抗原受体T细胞(CAR-T)注射液,主要用于治疗复发难治的CD20阳性的B细胞型非霍奇金淋巴瘤,包括弥漫大B细胞淋巴瘤和转化型滤泡性淋巴瘤。该产品由上海隆耀自主研发并具有知识产权的OX40共刺激信号设计,实验证明该设计在保障安全性的前提下,提高了产品的功效。该产品目前是中国第一个也是唯一一个获得注册临床申请受理的CD20靶点的CAR-T产品。
嘉和生物英夫利西单抗申报上市。注射用英夫利西单抗(GB242)是嘉和生物开发的一款生物类似药,拟用于治疗自身免疫性疾病。根据CDE官网信息,除强生的原研药类克(英夫利西单抗)外,中国尚无英夫利西单抗生物类似药获批上市。
AK104注射液是PD-1/CTLA-4双抗,在10月9日被纳入拟突破性治疗品种公示名单,AK104 是康方生物利用康方独特的Tetrabody双抗平台自主研发的新型的、潜在下一代首创PD-1/CTLA-4 双特异性肿瘤免疫治疗骨干药物,也是全球首个进入临床试验的PD-1/CTLA-4双特异抗体,旨在实现与肿瘤浸润淋巴细胞,而不是正常外周组织淋巴细胞的优先结合。本试验的适应症是晚期实体瘤(非小细胞肺癌、黑色素瘤、鼻咽癌、胃癌、三阴乳腺癌、尿路上皮癌和高度微卫星不稳定型实体瘤)。
2. 在审批阶段
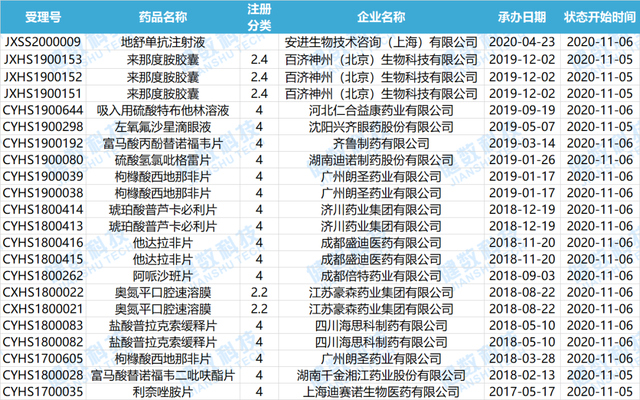
近期共有14个品种(22个受理号)进入审批阶段。
2020.11.01-2020.11.08在审批阶段药物情况
数据来源:健数科技中国药品审评数据库
地舒单抗注射液:本品是由安进公司开发的一种新型RANKL抑制剂,是RANKL的全人化单克隆IgG2抗体,对可溶性、跨膜形式的人RANKL具有高度亲和力和特异性。2019年5月,NMPA有条件批准地舒单抗注射液(英文名:Denosumab Injection)进口注册申请,用于骨巨细胞瘤不可手术切除或者手术切除可能导致严重功能障碍的成人和骨骼发育成熟的青少年患者治疗。2020年6月又获批进口新适应症,可能为用于治疗有增加骨折危险的绝经后妇女的骨质疏松(有骨质疏松史或多发性骨折危险因素)或不能耐受现有其它骨质疏松治疗药的患者。
迪赛诺利奈唑胺片即将获批。迪赛诺利奈唑胺片4类上市申请进入行政审批阶段,有望近日获批上市。利奈唑胺是一种恶唑烷酮类抗生素,主要用于治疗革兰阳性球菌引起的感染,包括由耐甲氧西林金黄色葡萄球菌引起的院内获得性肺炎、社区获得性肺炎、复杂性皮肤或皮肤软组织感染以及耐万古霉素肠球菌感染。该品种国内仅有原研辉瑞及华邦制药、豪森药业等3家药企获批。
3. 审批完毕
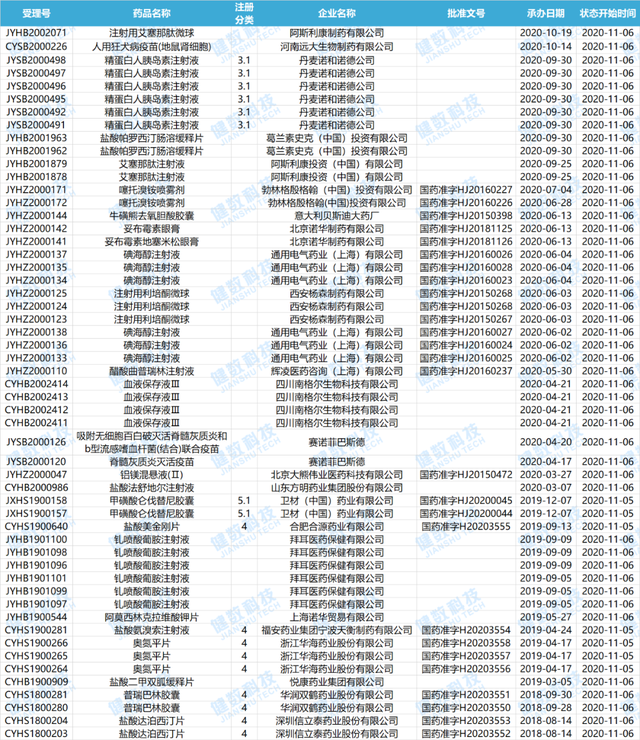
近期共计26个品种(涉及受理号54个)处于审批完毕-待制证。下表是审批完毕的药物情况。
2020.11.01-2020.11.08审批完毕药物情况
数据来源:健数科技中国药品审评数据库
4. 制证完毕-待发批件
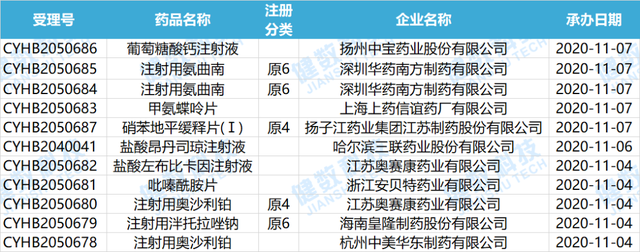
本周共计27个品种(涉及受理号33个)制证完毕-待发批件,有3个品种通过一致性评价,6个品种视同通过一致性评价。下表是制证完毕的药物情况。
2020.11.01-2020.11.08制证完毕药物情况
数据来源:健数科技中国药品审评数据库
5. 已发件
近期共计42个品种(涉及受理号72个)已发件,其中有11个品种通过一致性评价,8个品种视同通过一致性评价。下表是已发件的药物情况。
2020.11.01-2020.11.08已发件药物情况
数据来源:健数科技中国药品审评数据库
华纳大药厂枸橼酸铋钾胶囊首家通过一致性评价:湖南华纳大药厂枸橼酸铋钾胶囊获药监局批准通过一致性评价,为该品种首家通过一致性评价的仿制药。枸橼酸铋钾胶囊用于慢性胃炎及缓解胃酸过多引起的胃痛、胃灼热感(烧心)和反酸。
联环药业硫酸氢氯吡格雷片通过一致性评价。联环药业4类仿制药硫酸氢氯吡格雷片获国家药监局批准并视同通过一致性评价。硫酸氢氯吡格雷片是一种血小板聚集抑制剂,是抗血栓形成药市场的明星品种,已纳入第一批国采。目前国内共有9家企业获得该品种生产批文,分别为原研厂家赛诺菲、信立泰、乐普药业、石药欧意等。
正大天晴注射用艾司奥美拉唑钠首家过评。正大天晴注射用艾司奥美拉唑钠获NMPA批准通过一致性评价,为该品种首家通过一致性评价的注射剂。艾司奥美拉唑是奥美拉唑的单一左旋异构体,属于质子泵抑制剂,由阿斯利康原研,用于治疗胃食管反流性疾病、糜烂性反流性食管炎等。
6. 一致性评价申请
近期有9个品种提交一致性评价申请。
2020.11.01-2020.11.08药审中心一致性评价承办情况
数据来源:健数科技中国药品审评数据库
【声明】本文为原创文章,首发于微信公众号:健数科技(ID:drugeyes),如需转载请联系授权

























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论