长期以来,我国化学药品制剂产品频现“出海”难题,出口主力仍以原料药为主。直到最近几年,在国家政策引导下,我国化学药品制剂生产技术已取得突飞猛进。2019年,我国化学药品制剂出口额41.1亿美元,同比增长0.23%,其中,对美西药制剂出口4.21亿美元,同比增长8.78%;对非洲出口5.5亿美元,同比增长5.7%;对欧盟西药制剂出口额为10.1亿美元,同比下降16.4%。比如安徽华益、恒瑞医药、丽珠集团、药明康德、海普瑞、九州药业等,越来越多的本土药企跨越国际规范市场准入门槛,实现制剂出海。但与国际队伍相比,欧美地区占据CRO市场九成份额,中国比重依然有限,未来还需进一步提高国际竞争力。
化学药品制剂已”跋山涉水”走出国门,但要想站稳国际舞台,未来任重而道远…
获得国外药监认可GMP时间长。由于化学药品制剂直接作用于患者,对其质量标准、准入门槛要求更高,而且注册手续繁琐。整个注册程序下来通常需要3-4年时间,甚至更久,导致企业面临风险较大,出口意愿不高。
科学研发能力不足。我国出口的化学药品制剂绝大部分是仿制药,产品附加值低,难以打造出国际品牌。归咎其因,在于企业研发投入不足、新药研究资源匮乏。
出口品种单一。我国是全球原料药生产大国,但由于技术限制,能出口的产品品种有限,集中于青蒿素类、头孢类、维生素类、激素类等药品。
对于化学药品制剂走向国际舞台,华益药业科技(安徽)有限公司(以下简称“华益药业)董事长高煜博士表示,“在2006年的时候,一位欧洲客户将我们具有CEP证书的原料药从中国卖到欧洲市场,欧洲药企再将这些原料药转运到印度做成制剂,最后回到欧盟市场去销售。我们团队当即意识到,我们为什么不将原料药在中国直接做成制剂卖到欧洲?这在当时对我们来说是不可想象的,甚至是疯狂的。然而,欧洲客户对此却很感兴趣,并提出了极高的要求。”
在当时艰难的医药环境下,正是高煜和他的团队这种大胆的、不可思议的想法,才打造了华益药业这所安徽省首家通过欧盟认证的化学药品制剂的出海基地。
2021年5月11-12日,由药融圈主办的“生物医药创新者峰会”在广州召开。安徽华益专注于为中国和欧盟市场提供片剂、胶囊、口服液体制剂的研发生产服务型企业。其利用在制剂及早期临床方面过硬的技术和创新的手段打造了中国从原料药转型到化学药品制剂的出海生产基地。欢迎大家前往展位号13A号垂询,共同探索中国化学药品制剂如何与欧美”接轨”!

据公开数据显示,华益成立20年来,进出口额累计约35亿美元,其中出口约30亿美元,进口约5亿美元;净资产增长近40倍。在制造板块,医药制剂生产和研发基地——华益药业通过以数字化车间建设为主线实现产能扩大和质量提升,现已成长为中国医药制剂国际化先导企业、国家高新技术企业、中国CDMO企业20强、中国外包服务百强、安徽省服务外包KPO(知识流程外包)10强。
华益药业很好地解决了化学药品制剂出海困局
中美双报途径
公司拥有专业的欧盟和国内研发和注册团队,同时拥有专业系统的欧盟法规和强大的文件顾问资源,自成立至今已成功为欧盟客户获得超过10个仿制药研发注册批件,并实现商业化生产。
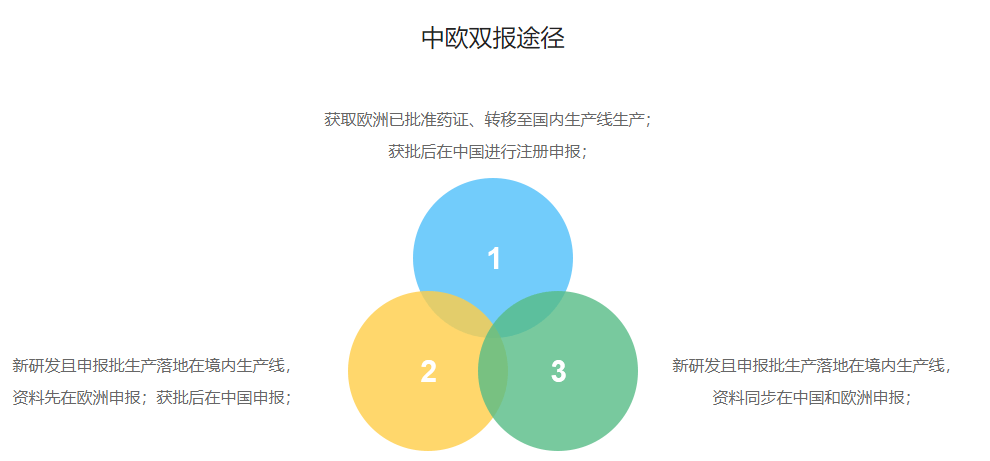
华益药业自2018年起与合肥市诗泰特医药科技有限公司、合肥市开凡检测科技有限公司建立战略合作关系,建成符合中欧双标准的药学研发-临床研究-第三方检测-注册申报-商业化生产-商务服务一站式医药制剂开发CDMO平台,实现研发CRO、商业生产CMO以及商务服务CSO的无缝对接。

研发技术过硬
公司下设药物研究院,拥有一支专业药品研发队伍,核心成员平均工作年限10年以上,已成功为客户研发50多个品规,年产量逾20亿片。同时,华益在专业技术上,通过欧盟正式BE的产品为0.1毫克的某种糖皮质激素,由于规格极小,技术难度大,欧盟仅有一家企业的产品获准上市,华益药业生产的验证批以近乎完美的数据一次性通过BE试验,使得华益有望成为欧盟第二家能够上市该产品的企业,展现了华益药业在研发和生产方面过硬的技术能力。
出口品种丰富
华益药业可生产、研发多种剂型和包装的固体制剂和液体制剂产品,在骨架缓释、极小规格、泡腾片等特殊剂型上拥有较强的独特技术优势。在医药制剂产品与技术方面,华益药业已完成50多个仿制药品种或剂型的研发和技术转移,目前正在研发的项目有56个,其中,欧盟技术转移项目14个以及委托研发项目26个、中国委托研发项目11个、欧盟自主持证项目4个、世界卫生组织WHO抗结核复方制剂项目1个。
如果用发展阶段来形容全球化学制剂市场,那么欧美国家化学药品制剂已进入鼎盛时期,而中国正处于对万物抱有好奇,仍在探索中前行的发展中时期。发展中的中国早晚会强大,需要有像华益医药这样敢于突破自我,冲出国门的企业做标杆,为中国化学药品制剂市场之崛起而拼搏。
<END>



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)


















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论