近日8家外资制药巨头发布Q1业绩:强生、罗氏、雅培、诺华、赛诺菲、BMS、GSK和安进。从营收来看,5家增长,3家小幅度下滑。
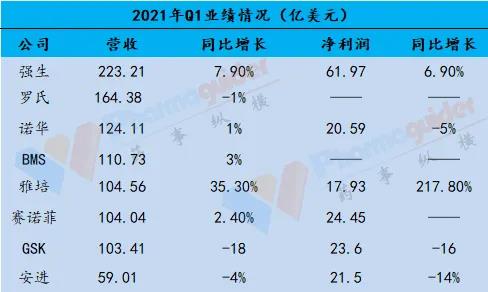
资料来源:财报
01

诺华一季度营收124.11亿美元,同比增长1%,净利润20.59亿美元,下滑5%。主要由于covid-19对需求产生了负面影响,特别是:皮肤病学、眼科、乳腺癌产品组合、Sandoz零售和抗感染药物。
制药事业部与前一年(0%cc、4%美元)一致,从Entresto(34%cc)、Zolgensma(81%cc)和Cosentyx(11%cc)持续强劲增长,Kesimpta的销售额达到了5000万美元。
肿瘤事业部增长了1%(cc、4%美元),主要由Kymriah(55%cc)、Promacta/Revolade(13%cc)、Kisqali和Jakava(8%cc)推动。Adakveo的销售额达到了3700万美元。
Sandoz销售额下降13%,(cc、-9%),零售下降18%,生物制药增长7%。
2021年十大创新药物产品的净销售额
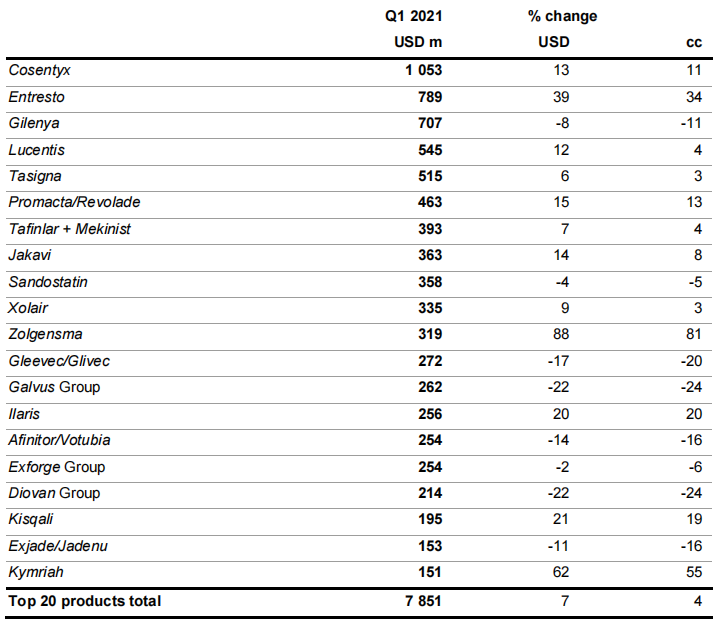
资料来源:诺华Q1财报
02

赛诺菲21年Q1营收85.91亿欧元,同比增长2.4%;其中一季度Dupixent销量大增46%,达到10.47亿欧元,去年全年Dupixent销量35.34亿欧元,大幅增长73.19%;疫苗板块增长5.3%,达到9.15亿欧元。
Dupixent是一款靶向IL-4R的单克隆抗体药物,可以结合IL‑4和IL-13共同的受体模块IL‑4Rα,同时阻断IL-4和IL-13信号,对多种2型免疫相关的炎性疾病具有很好的控制作用。Dupixent一于2017年3月首次获得FDA批准,Dupixent已经获批3项适应症,分别为哮喘、慢性鼻-鼻窦炎伴鼻息肉和特应性皮炎。在特应性皮炎领域,Dupixent目前已经逐步覆盖了年龄在6岁以上的所有患者。2020年6月19日,赛诺菲Dupilumab注射液(英文商品名:Dupixent)在中国获批上市,用于治疗中至重度特应性皮炎。
其他业务中罕见病板块一季度营收7.7亿欧元,增长4%;神经病学和风湿病学板块营收5.81亿欧元,罕见的血液功能障碍板块营收2.72亿欧元,抗肿瘤板块营收2.21亿欧元,增长26%。
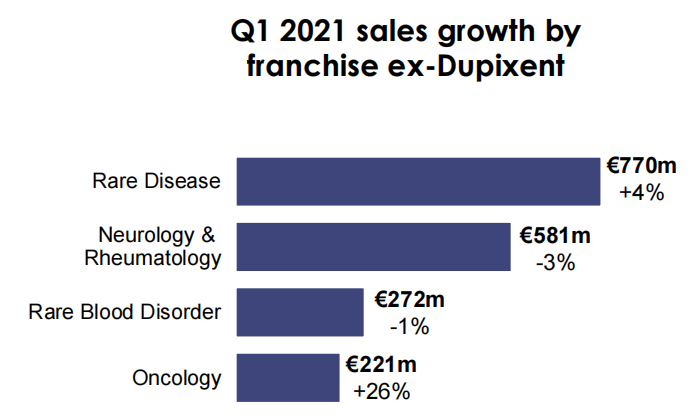
资料来源:赛诺菲财报
第三阶段的研发管线如下
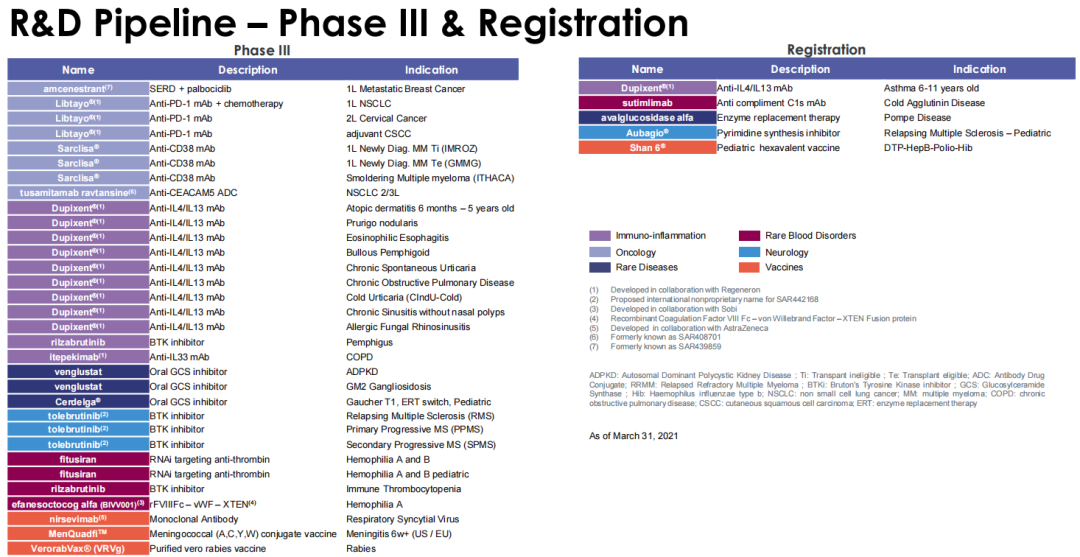
资料来源:赛诺菲财报
03

强生2021年第一季度$销售额223亿,增长7.9%;净利润为61.97亿美元,同比增长6.9%。美国区销售额为111.11亿美元,同比增长3.9%;
按业务板块:消费者健康业务销售额35.43亿美元,同比下降2.3%;制药业务销售额121.99亿美元,同比增长9.6%,其中新冠疫苗销售额为1亿美元;医疗器械业务销售额65.79亿美元,同比增长10.9%。
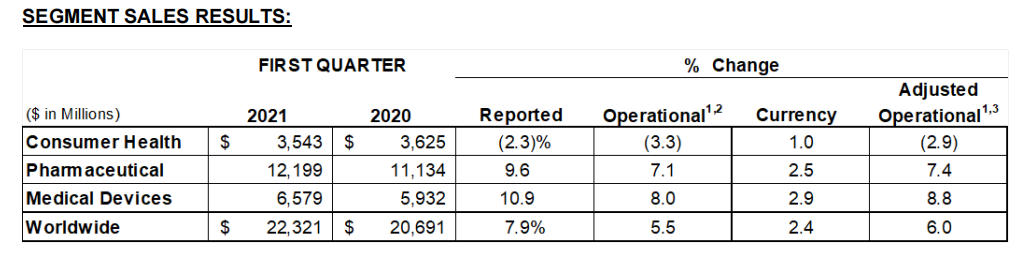
资料来源:强生财报
强生公司将2021年全年指引的调整运营销售增长增至9.3%,并在中点调整运营EPS增长至16.8%。以下是强生的部分研发管线。
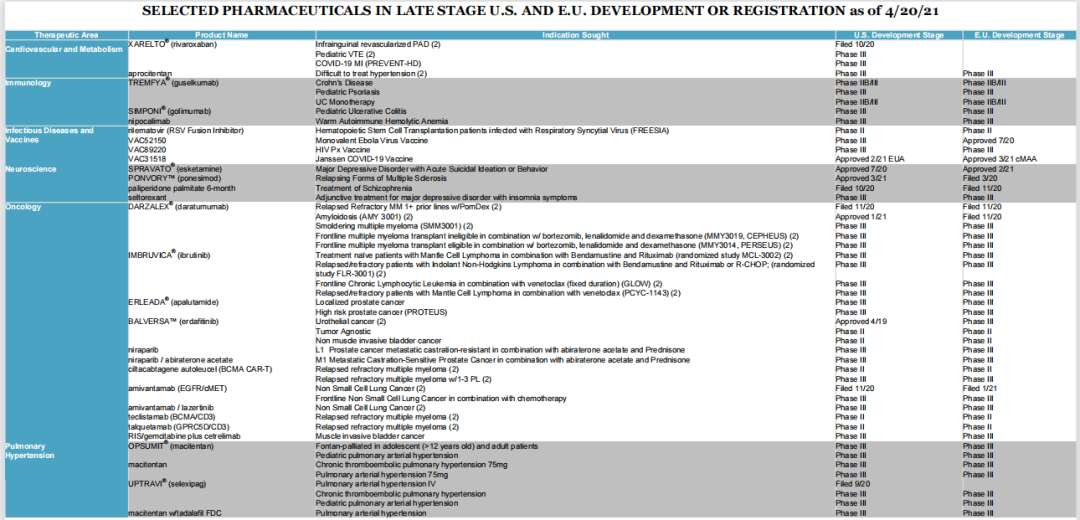
资料来源:强生财报
04

罗氏21年Q1营收14.9亿瑞士法郎,同比下降1%。药品部门的销售销售仍然受到covid-19和生物仿制品的影响。其中抗肿瘤板块受到生物类似药和COVID-19影响营收下降19%。
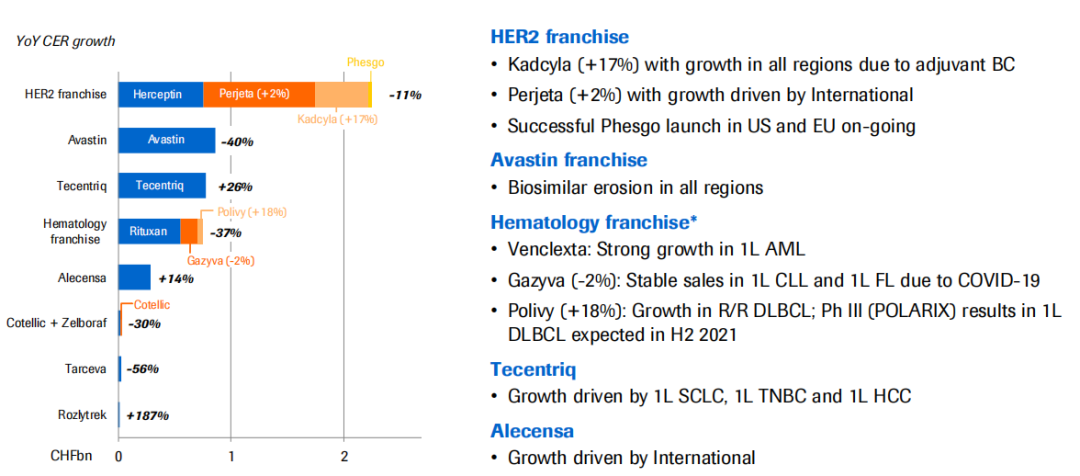
Kadcyla增长17%。恩美曲妥珠单抗(Kadcyla),是由抗HER2靶向药物曲妥珠单抗与抑制微管聚集的化疗药物美坦新(DM1)通过硫醚连接子连接而成的抗体偶联物(即ADC药物),具有「生物导弹」靶向肿瘤细胞的杀伤特点。该药由罗氏和ImmunoGen共同研发,于2013年被FDA批准用于治疗已经接受过曲妥珠单抗和紫杉醇化疗失败的HER2阳性晚期乳腺癌患者。
Tecentriq增长26%。2020年2月13日,中国药监局正式批准了罗氏PD-L1单抗Tecentriq(atezolizumab,阿替利珠单抗),具体适应症为:Tecentriq联合化疗用于一线治疗广泛期的小细胞肺癌(SCLC)。值得注意的是,阿替利珠单抗联合化疗是全球第一个,且目前中国唯一一个获批用于一线治疗广泛期小细胞肺癌的肿瘤免疫疗法,阿替利珠单抗也是继阿斯利康的Imfinzi(durvalumab,度伐利尤单抗)之后,中国批准的第二款PD-L1肿瘤免疫疗法。
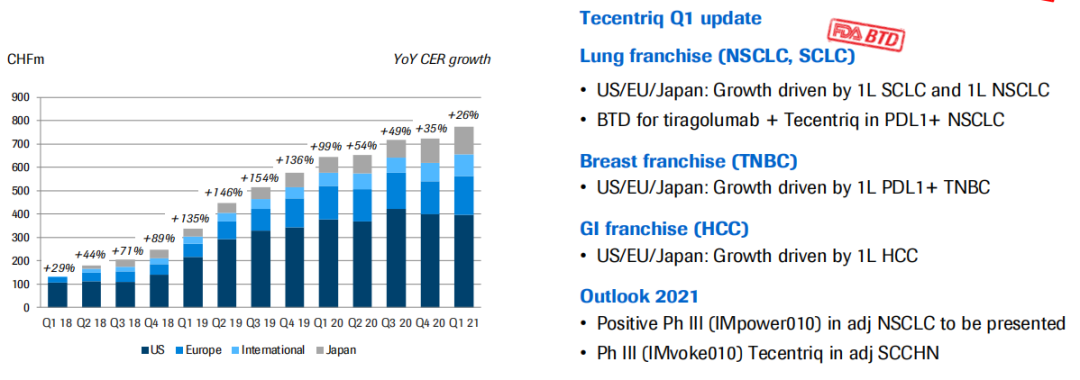
罗氏目前进入到3期临床的研发管线
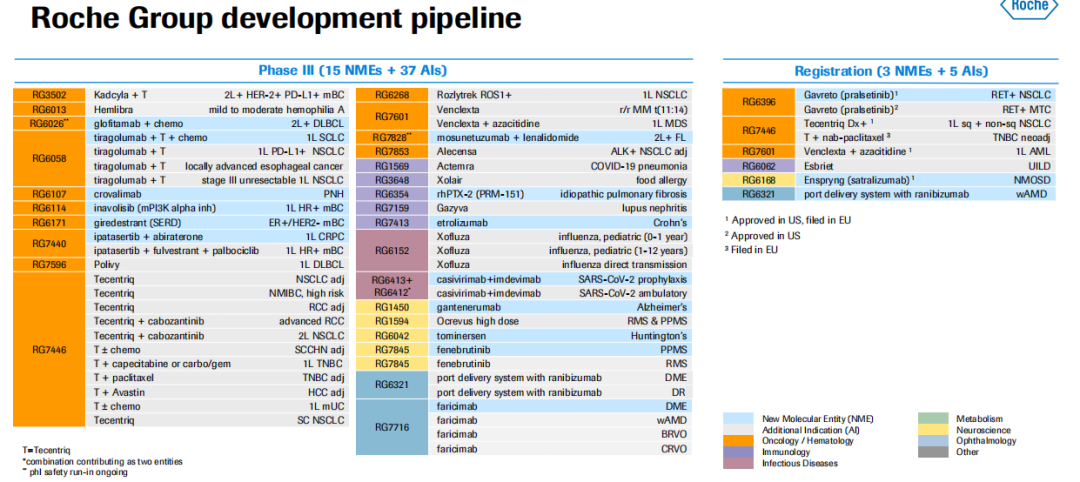
05

安进21年Q1营收59.01亿美元,增长4%,净利润21.50亿元,下降14%。其中Prolia销量6.54亿美元,同比增长16%,该药在2018年5月FDA获批上市,治疗骨质疏松。
Enbrel一季度销量11.53亿美元,下降20%。Enbrel是世界上首个应用于类风湿性关节炎和强直性脊柱炎的TNF抑制剂,原研公司为安进和辉瑞,目前已获得至少五个炎症相关适应症的批准,该药在2010年就在中国获批上市。诺华山德士曾在19年8月挑战两项Enbrel的专利,以失败告终。安进在美国上诉法院取得了Enbrel专利官司的胜利,法院支持Enbrel专利期延长至2029年。依据判决,这一抗炎药物将在美国市场上享有长达31年的市场优势。
Evaluate Pharma估计到2024年,Enbrel的终身销售额或达1400亿美元。这将使它在重磅药物传奇榜上跃居第3,仅次于艾伯维的Humira和辉瑞的Lipitor。
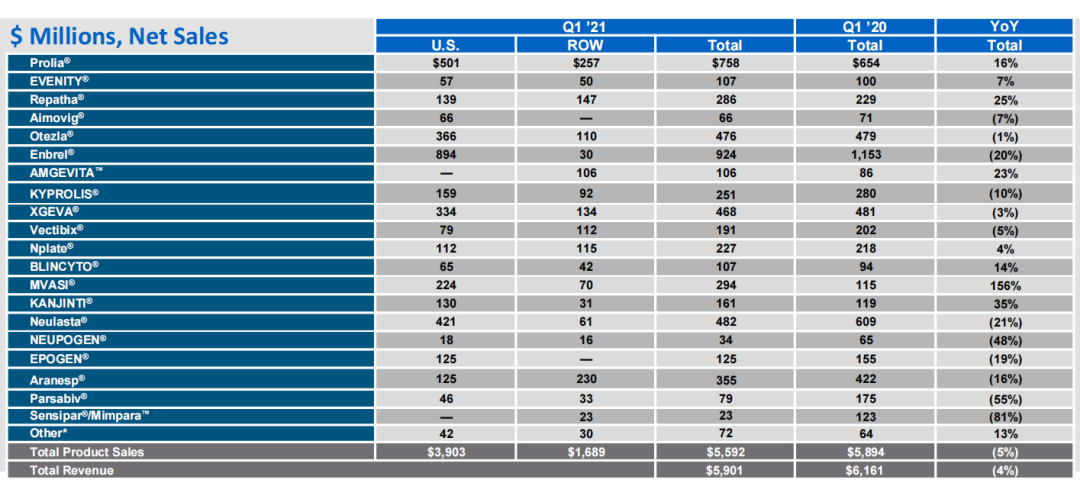
数据来源:安进财报
安进研发管线更新
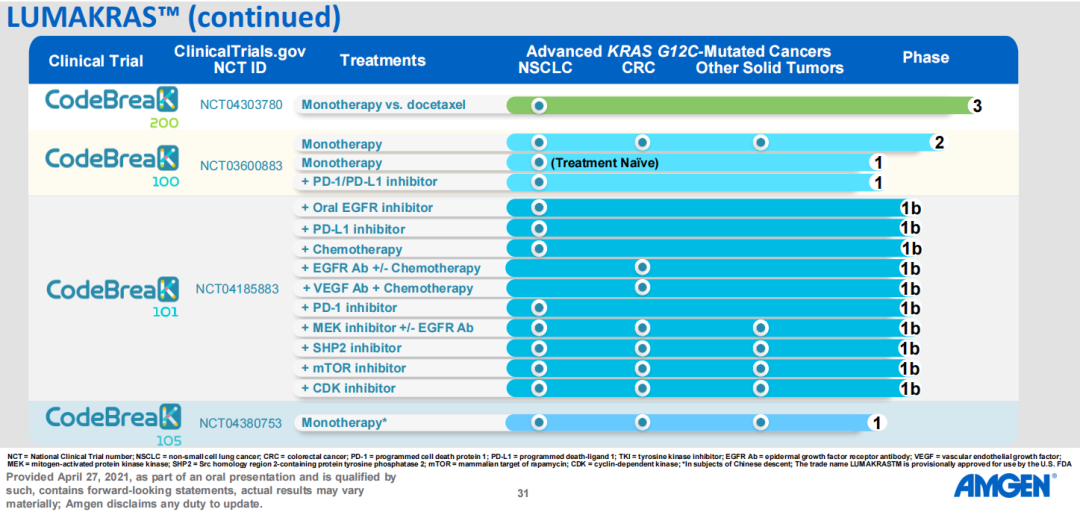
数据来源:安进财报
06

GSK21年Q1营收74亿英镑,同比下降18%。其中制药板块营收39亿英镑,下降12%,新产品和专业产品类增长3%,其中包括呼吸类增长24%,免疫炎症类增长26%,抗肿瘤产品增长38%。
抗肿瘤板块:PARP抑制剂的销售为8800万英镑,增长9%。美国的销售额为5100万英镑,欧洲为3600万英镑。复发或难治性多发性骨髓瘤患者的治疗公司于2020年第三季度在美国和欧洲获得批准和推出,本季度销售额为2100万英镑。
疫苗板块:一季度营收12.24亿英镑,下降32%,,主要来自covid-19大流行对鞘状疱疹、肝炎疫苗、含dtpa疫苗和贝塞洛的不良影响。但中国市场表现较好,抵消了部分下滑。
公司的研发侧重于免疫系统的科学、遗传学和先进的技术。该管道目前包括59种疫苗和药物,其中主要分布在传染病、肿瘤学和免疫介导的疾病等领域。
07

BMS第一季度营收111亿美元,同比增长3%。经外汇因素调整后增长1%。剔除上年同期与COVID-19相关的购买模式后,第一季度收入增长了8%。分区域来看,美国营收增长4%,至70亿美元,国际营收增长1%,达到41亿美元,研发支出22亿美元。
Opdivo药一季度销量17.6亿美元,下降3%。
BMS产品一季度销量
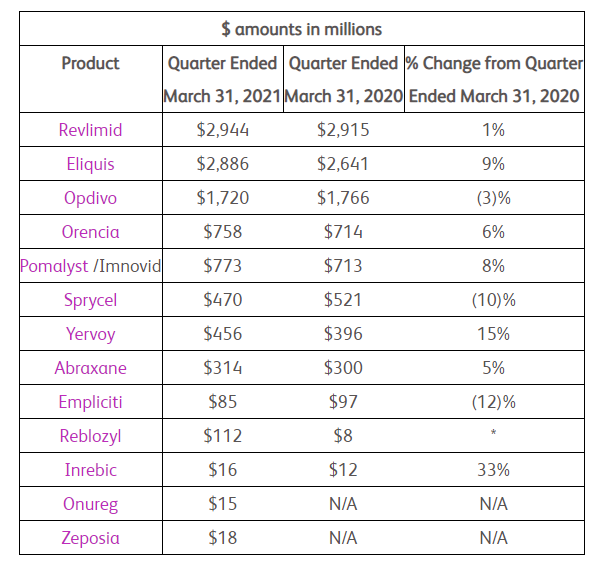
资料来源:BMS财报
08

雅培第一季营收为105亿美元,较上年同期增长35.3%。今年第一季度,全球COVID-19检测相关销售额为22亿美元,雅培的BinaxNOW、Panbio和IDNOW快速检测平台的总销售额为18亿美元。
今年1月,美国医疗保险中心(U.S.Centers for Medicare &医疗补助服务(Medicaid Services)扩大了雅培革命性的MitraClip设备的报销范围,这大大增加了能够从这种市场领先的微创心脏设备中受益的人数。今年3月,雅培宣布在美国推出NeuroSphere虚拟诊所,这是一项首创的技术,允许患者与医生沟通,确保适当的设置和功能,并根据需要远程接受新的治疗设置。今年4月,雅培宣布了FDA(FDA)对其BinaxNOW COVID-19 Ag自检的紧急使用授权(EUA),适用于有或无症状且不需要处方的个人。
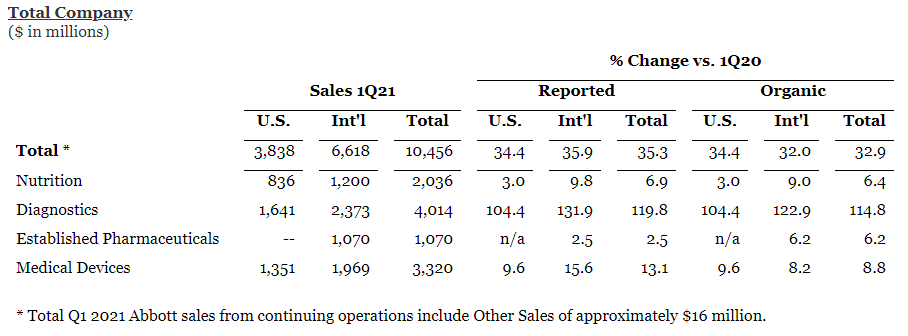
资料来源:雅培
总结
从一季报来看,尽管受到新冠疫情影响,但跨国制药企业大部分业绩保持平稳,创新药/抗肿瘤产品大都保持良好增长,中国区业务增长速度一定程度上抵消了其他区域的下滑。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论