
据CDE官网显示,广州必贝特医药的1类新药BEBT-209胶囊再次获批临床,适应症为三阴性乳腺癌。
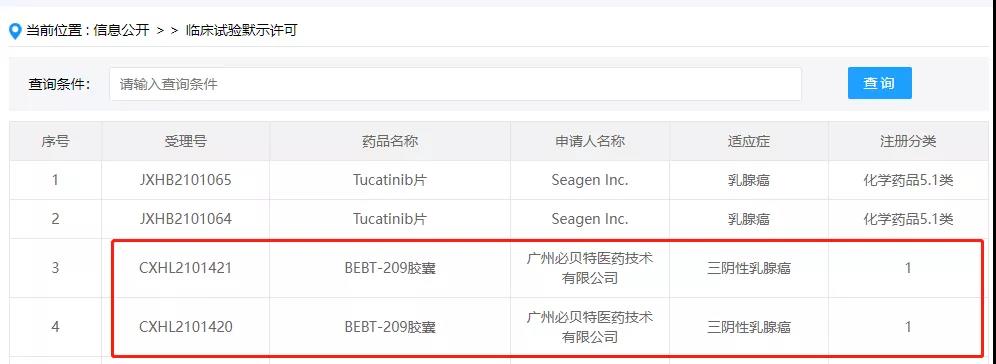
图片来源:CDE官网
BEBT-209是一种对CDK4选择性高的CDK4/6抑制剂,该药此前已有多个适应症获批临床,包括:
- 复发或转移性HR+/HER2-晚期乳腺癌
- 联合氟维司群治疗既往接受内分泌治疗后疾病进展的激素受体阳性(HR+)及人表皮生长因子受体阴性(HER2-)的晚期乳腺癌
- 绝经后女性患者激素受体阳性(HR+)及人表皮生长因子受体阴性(HER2-)的晚期乳腺癌
对标辉瑞帕博西尼,BEBT-209有望成为Best-in-class CDK4/6抑制剂
CDK4/6抑制剂已成为乳腺癌治疗的一类重要靶向药物,其中的先行者和佼佼者便是辉瑞的Palbociclib(Ibrance,帕博西尼)。
2015年2月,辉瑞Ibrance通过加快审评在美国获FDA 批准上市,成为全球上市的首个CDK4/6抑制剂;2018年7月获NMAP批准在国内上市。凭借其先发优势,上市后其全球销售额每年均呈稳定增长,为辉瑞带来相当丰厚的收益,在2020年Ibrance销售额更是突破50亿美元大关,达到53.92亿美元。
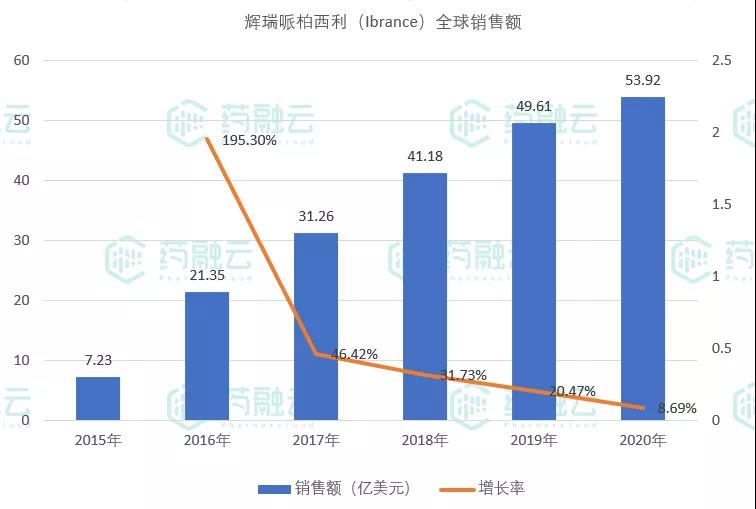
来源:据公开数据,药融云整理
而针对帕博西尼(Palbociclib)药代动力学口服暴露量低和血液系统毒性等缺陷,BEBT-209通过降低CDK6抑制活性和提高CDK4的选择活性,减少CDK6抑制导致的血液系统和免疫抑制毒性,使药物可能更加安全有效。
BEBT-209的I/II期临床试验初步结果表明,与帕博西尼比较,BEBT-209暴露量更高,安全性和疗效更佳,极有潜力成为Best-in-class CDK4/6抑制剂。必贝特医药已提交开展BEBT-209联合氟维司群≥1线治疗HER+/HER2- MBC III期临床试验的CDE沟通交流会议申请。
随着CDK4/6抑制剂广泛用于HR+/HER2-晚期乳腺癌的一线和二线治疗,超过30%的患者在接受CDK4/6抑制剂治疗后的两年内复发(N.Engl.J.Med.375:1925-1936),而CDK4/6抑制剂和内分泌治疗疾病进展是乳腺癌相关死亡的一个新原因,克服CDK4/6耐药是一个亟待解决的问题。
利用BEBT-209治疗晚期乳腺癌安全性高、疗效显著的优势以及BEBT-908阻断CDK4/6抑制剂耐药机制相关PI3K通路和HDAC激活的作用,公司正在启动的BEBT-209联合EBT-908治疗接受过内分泌治疗和CDK4/6治疗后耐药的ER+/HER2-晚期乳腺癌临床研究,极有望突破晚期乳腺癌患者对CDK4/6抑制剂和内分泌治疗耐药后无有效治疗药物的难题。
CDK4/6市场近70亿美元,恒瑞医药有望成国产首家
在《中国临床肿瘤学会(CSCO)乳腺诊疗指南(2020版)》、《中国晚期乳腺癌规范诊疗指南(2020版)》和最新版NCCN指南中,CDK4/6抑制剂联合内分泌治疗已成为HR阳性/HER2阴性晚期乳腺癌患者的首选治疗推荐。
目前全球共有4款CDK4/6抑制剂获批上市,实现商业化,即辉瑞的Palbociclib(Ibrance,帕博西尼)、诺华的Ribociclib(Kisqali,瑞波西利)、礼来的Abemaciclib(Verzenio,阿贝西利)及G1 Therapeutics的Trilaciclib(Cosela),2020年全球市场规模为69.92亿美元。国内目前已获批的CDK4/6抑制剂为哌柏西利和阿贝西利。
有机构预计,到2029年,CDK4/6抑制剂销售额将达到200亿美元,占乳腺癌药物销售市场份额的42%。
全球已上市CDK4/6抑制剂
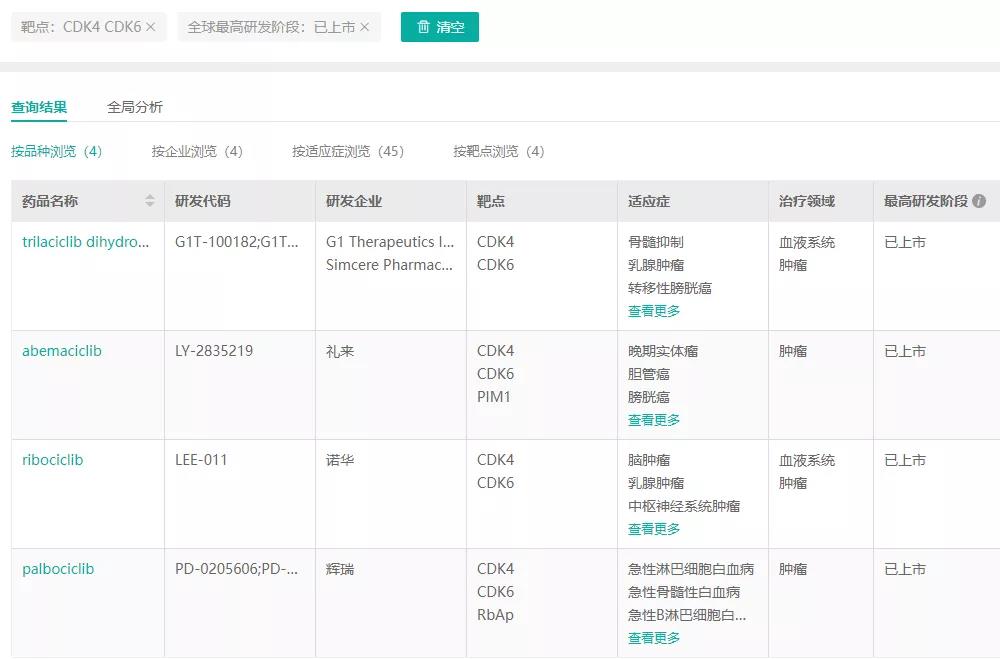
图片来源:药融云全球药物研发数据库
据统计,全球已有近40款在研CDK4/6抑制剂。国内已有恒瑞医药、四环医药、甘李药业、复星医药、豪森药业等多家药企布局,其中恒瑞医药进展最快,其自主研发的SHR6390片已递交上市申请,并于今年5月纳入优先审评程序,有望成为国产首款、国内第3款CDK4/6抑制剂。
国产在研CDK4/6抑制剂
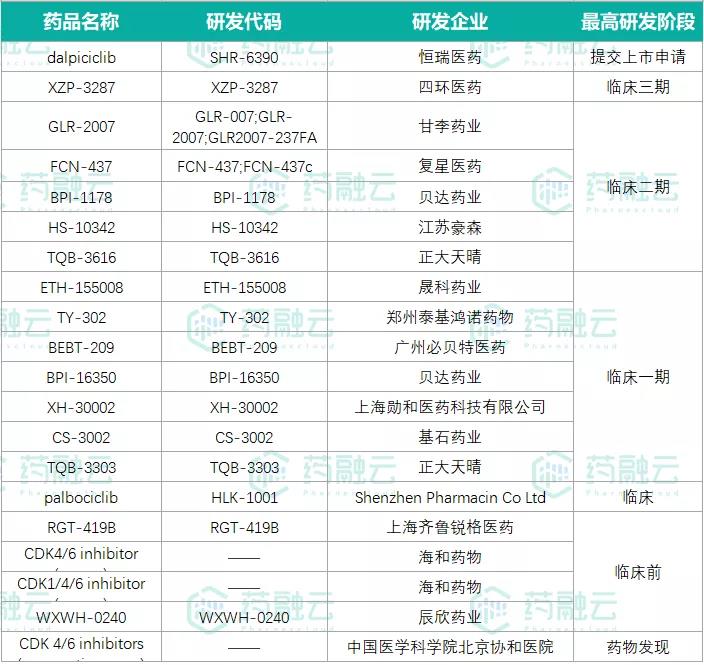
数据来源:药融云全球药物研发数据库
四环医药的XZP-3287进展在国产企业中也属前列,已进入临床III期试验。
四环医药XZP-3287公示临床试验
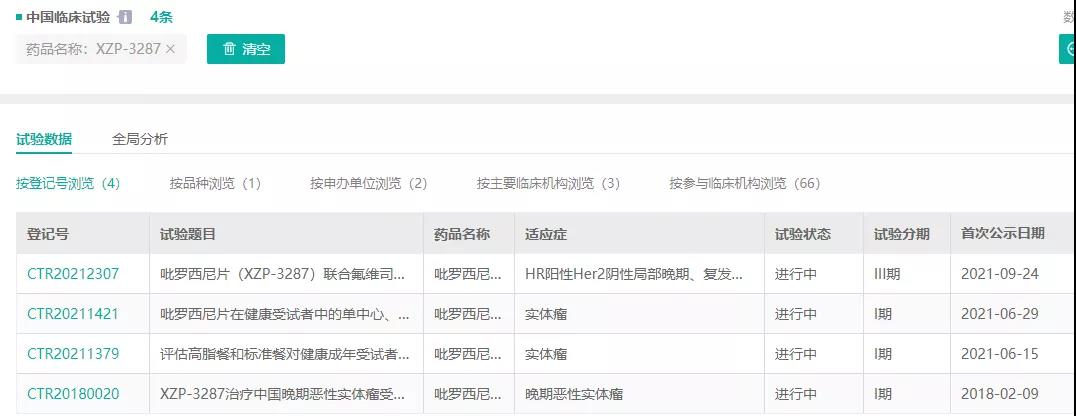
数据来源:药融云中国临床试验数据库
乳腺癌为全球最高发的恶性肿瘤之一,据世界卫生组织国际癌症研究机构(IARC)发布的最新数据显示,2020年乳腺癌新发患者达到226万,超过肺癌成为全球最高发的恶性肿瘤,也是全球女性发病率最高的恶性肿瘤,约68万患者死于乳腺癌。2020年,中国乳腺癌新发患者约42万,死亡患者约12万,是女性最常见的恶性肿瘤死亡原因之一。期待更多高效、安全的药物获批上市,乳腺癌患者也将拥有更合适的选择和更“亲民”的价格。
—END—


































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论