
2025年04月14日,日本兴和制药的佩玛贝特片在中国获批上市,用于治疗高脂血症(包括家族性高脂血症)。摩熵医药曾预测该品种仿制跟进速度会极其快,(详见相关扩展阅读:降脂新药佩玛贝特片中国获批!21家仿制企业“围剿”,首仿之争一触即发)
但没想到,这速度远比想象中还要快。仅一天后,4月23日,南京正大天晴首家提交仿制上市申请,随后七天内,又接连有4家企业提交了上市申请。短短一周多,已有五家提交了上市申请:

首家仿制上市申请被受理的日期与NMPA发布原研批准件日期相差仅9天。
这个时间差创造了新纪录,首次有企业仿制上市受理日期与原研获批日期相隔在10天以内,加上中间双休日,受理等待等,实际准备注册资料时间预计只有5天,这个速度真的是吓人。
目前国内对于首仿药品的政策倾斜力度其实并不大,抢仿更多还是用来体现企业的综合实力和宣传作用,毕竟业内会记得品种的首仿企业,但很难记得二仿、三仿企业。
不过首家提交上市申请也不一定就是首仿企业,后来者抢占首仿可能性不小。
比如近日同样被“围剿”的品种瑞舒伐他汀依折麦布片首仿已出现。赛诺菲的瑞舒伐他汀依折麦布片24年1月2日在国内上市,24年1月12日石家庄四药上市申请被受理,是首家上报,但首家过评企业却是第二家提交上市的福元医药(24年2月6日提交),目前石家庄四药的上市申请在尚在发补阶段。
福元医药顺利抢走了石四药的首仿。
由此看来,企业要想顺利抢到首仿,提交速度不是关键,资料及数据准备完全才是关键。
再说回佩玛贝特片,这个确实是个好品种。有业内人士称,佩玛贝特是个非常被看好的品种,抗血脂市场极大,国内对非核心专利的无效申请已经得心应手,花一千万左右的CMC费用获得一个强势品种非常划算,前期成功案例挺多。
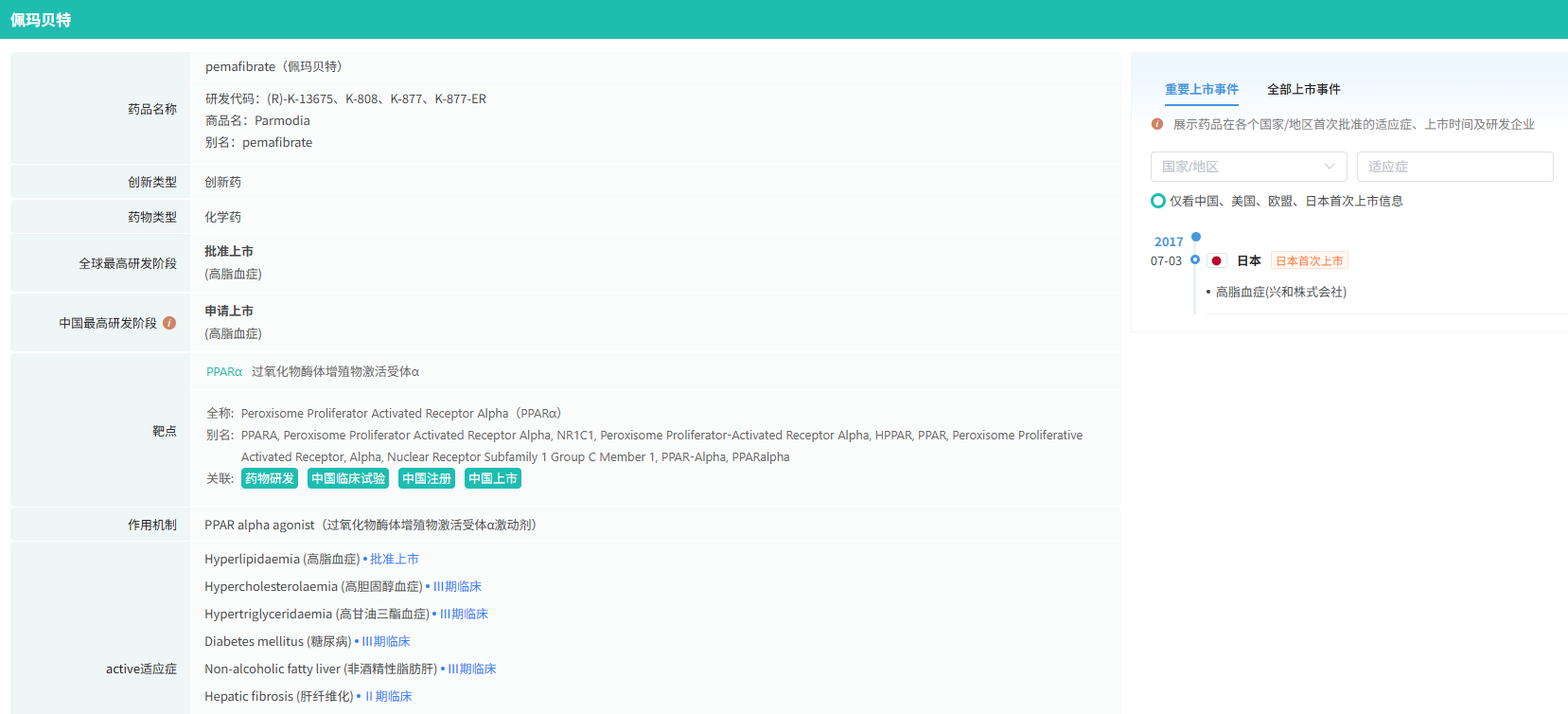
截图来源:摩熵医药数据库-全球药物研发数据库























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论