
8月18日,CDE官网显示,石家庄四药/河北爱尔海泰制药递交的注射用尼可地尔上市申请获受理。这是国内第10家以新注册分类申报该品种上市的企业,预估近两年这个年售超12亿元心血管注射剂大品种将迎来仿制药井喷,竞争愈发激烈。

截图来源:CDE官网
尼可地尔为心血管系统用药,具有三重作用靶点,不仅作用于冠状动脉,还作用于微血管和心肌线粒体。可用于急性冠状动脉综合征、心绞痛、心力衰竭、不稳定型心绞痛、心脏衰竭、高血压等。
目前国内上市的尼可地尔相关制剂仅有普通片剂和注射剂。总体来看,注射用尼可地尔占据主要市场(占比超7成)。目前注射用尼可地尔尚未纳入医保,即使如此,其近年院内销售市场依然一路见涨,据药融云统计,注射用尼可地尔2020年销售额突破10亿元大关,2021年达12.8亿元,同比增长了26%。
注射用尼可地尔院内销售情况
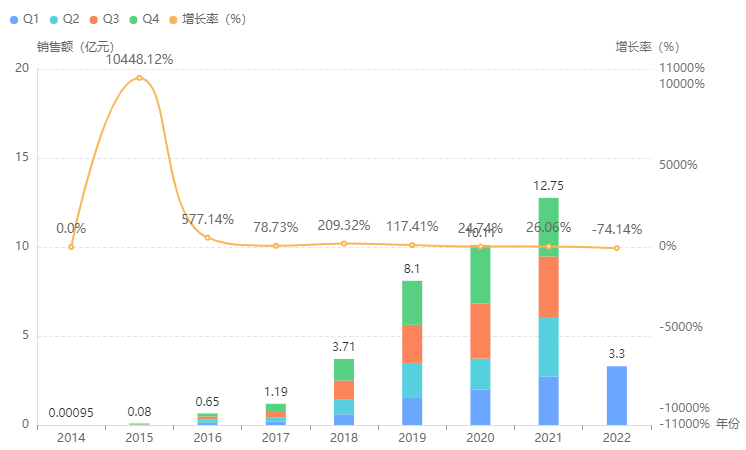
截图来源:药融云全国医院销售数据库
注射用尼可地尔目前仅北京四环科宝制药一家拥有批文,为其独家品种。北京四环科宝已递交了一致性评价补充申请,但暂未过评。
注射用尼可地尔中国批文信息

截图来源:药融云中国药品批文数据库
据药融云数据库查询,扬子江药业、仁合益康、天津天士力之骄药业、成都苑东生物/山西普德药业、南京恒道医药/江苏九旭药业等10家企业相继提交了注射用尼可地尔的仿制3类上市申请,均在审评审批中。若谁能顺利通过,将直接成为国产第二家获批生产该12亿心血管注射剂的企业,究竟花落谁家,让我们拭目以待。
以新注册分类申报注射用尼可地尔的企业
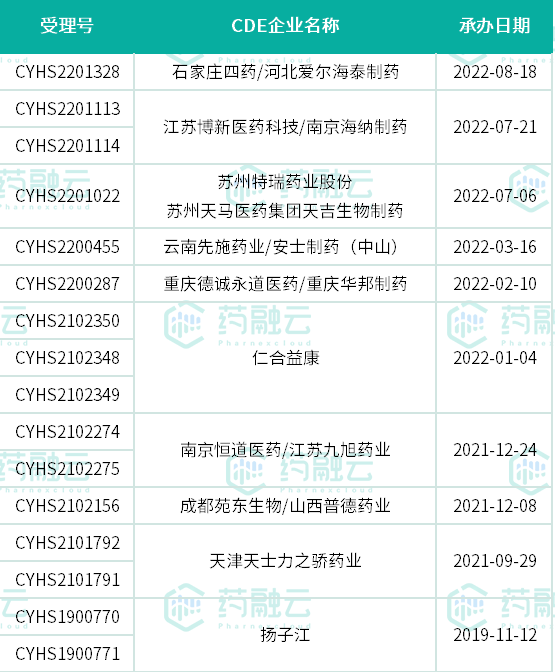
数据来源:药融云中国药品审评数据库
参考来源:
[1] CDE官网
[2] 药融云数据库
想要解锁更多药企仿制药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企仿制药申报情况、审批信息、最新进展、一致性评价、市场竞争格局、销售情况,市场规模与前景,可否投入!注册立享15天免费试用和虎年首份医药数据大礼包!

—END—





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论