
2023年1月10日,从国家药品监督管理局药品审评中心官网公示信息获知,江苏诺泰澳赛诺生物制药股份有限公司(简称诺泰生物)注册申报的司美格鲁肽原料药[登记号:Y20220001086]已获得受理。诺泰生物成为该产品国内首批上市申请获得受理的原料药厂家之一,国内首家由天吉生物申报(《国内首家!司美格鲁肽原料药申报获受理,天吉生物再突破!》)。
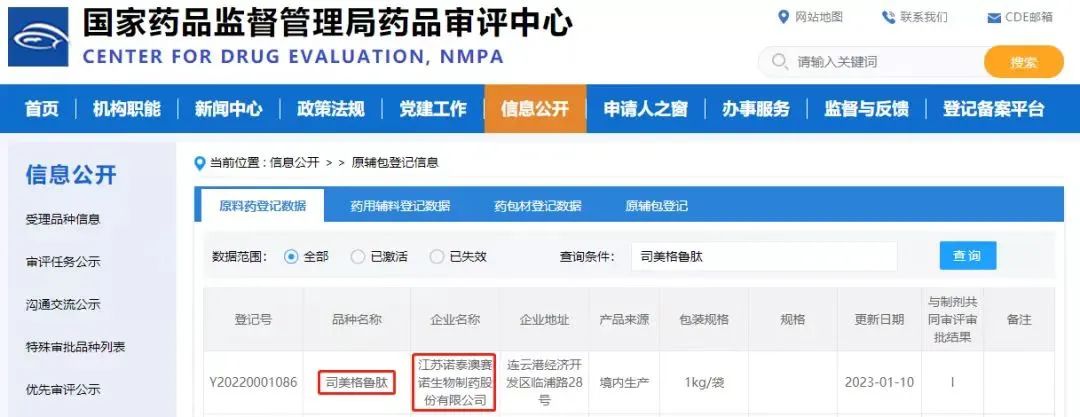
2021年11月诺泰生物向美国食品药品监督管理局(FDA)递交司美格鲁肽原料药的注册申请,并已通过完整性审查,于2022年5月收到FDA技术审评意见,预计2023年1月提交发补答复资料。
2022年8月诺泰生物向印度MoHFW递交了司美格鲁肽原料药的注册申请,并于2022年12月收到技术审评意见,预计2023年2月提交发补答复资料。
另外,司美格鲁肽原料药以EDMF方式在欧洲国家的注册已在诺泰生物2023年的计划中。
历经多年研发,诺泰生物的司美格鲁肽在单批批量和产品质量均处于行业领先地位。
一、关于司美格鲁肽
据药融云数据库显示,司美格鲁肽是由诺和诺德开发的新型长效GLP-1 RA,最早在2017年12月获得FDA批准,用于辅助饮食控制和运动以改善2型糖尿病患者的血糖控制。2021年6月,FDA批准该药物用于肥胖或超重成人的慢性体重管理。诺和诺德2022年三季度财报显示,作为主打产品的司美格鲁肽表现亮眼。其中,用于注射剂销售额约56.8亿美元,增长率69%;片剂销售额约9.62亿美元,两者合计销售约66.42亿美元。
司美格鲁肽适应症研发状态
截图来源:药融云全球药物研发数据库
在中国,司美格鲁肽于2021年4月上市,目前获批的适应症仅为2型糖尿病。据诺和诺德公开信息,该药2021年的销售额一举突破亿元,达到约3.12亿人民币。2022年前三季度,司美格鲁肽在中国市场继续强势增长,实现15.36亿人民币的销售额。
司美格鲁肽中国批文信息
截图来源:药融云中国药品批文数据库
为了进一步改善患者的用药便利性和依从性,诺和诺德公司又研发了首个可口服的司美格鲁肽片剂,成为FDA批准使用的第一个口服GLP-1 RA,为全球糖尿病患者带来福音。

除了降糖、减重作用显著外,司美格鲁肽还可从多方面实现对心脑血管的保护,包括保护血管内皮、降低血压、改善血脂、减轻炎症、改善微循环等,且耐受性良好。同时,司美格鲁肽还能降低2型糖尿病患者的白蛋白尿、保护肾脏、降低肾脏复合终点事件发生风险,可用于糖尿病肾脏病的防治。司美格鲁肽还具有改善肝脏和大脑中的胰岛素抵抗,发挥保护肝脏、减少肝脏中的脂肪含量以及提高认知能力、保护神经的作用,亦是非酒精性脂肪性肝病和神经退行性疾病的治疗选择。
诺泰生物深耕多肽类药物10余年,经过多年研发积累,其自主选择的多个原料药品种的单批批量和整体产能均处于行业领先,多肽原料药已CDE登记备案或美国FDA进行DMF/VMF备案登记,包括司美格鲁肽、比伐芦定、依替巴肽、胸腺法新、利拉鲁肽、醋酸兰瑞肽、醋酸奥曲肽、醋酸西曲瑞克等多个品种,其中部分品种为全球首仿的独家原料药供应商。
诺泰生物获批原料药(部分)
截图来源:药融云原料药供应商数据库
依托十余年小分子和多肽从临床前到商业化的一站式工艺开发服务的成功经验,诺泰生物寡核苷酸技术平台可以为客户提供从临床前样品制备到符合国内外法规要求的寡核苷酸原料药和制剂GMP生产服务。工艺、分析、制剂和注册法规团队的协同合作,可为客户提供寡核苷酸开发全流程的快捷、高效、专业、灵活的一体化解决方案。

图 | 连云港工厂

图 | 浙江建德工厂
二、关于诺泰生物
江苏诺泰澳赛诺生物制药股份有限公司成立于2009年,是一家聚焦多肽药物及小分子化药自主研发与定制研发相结合的企业。公司是国家高新技术企业和省级科技型企业,致力于通过技术创新,突破药物研发及生产的技术瓶颈,构建从医药高级中间体、原料药到制剂的全产业链,为全球伙伴提供绿色、低成本、优质、高效的医药相关产品和技术服务。
截图来源:药融云投融资数据库
诺泰生物围绕高级医药中间体及原料药的生产工艺研究(包括合成路线设计、工艺条件选择、起始原料和试剂选择、工艺优化与中试放大、杂质分析、三废处理等),制剂剂型和处方工艺研究、质量研究、稳定性研究等药学基础研究,结合多肽药物与小分子化药各自特点,解决了多肽药物及小分子化药研发及合成生产过程中的一系列全球性技术难题,建立了多肽规模化生产技术平台、手性药物技术平台、绿色工艺技术平台、制剂给药技术平台、多肽类新药研发技术平台等五大行业领先的核心技术平台。

2022年,诺泰生物荣获药智网“2022中国医药CDMO企业20强”,SK Pharmateco首选合作伙伴奖,2022浙江省A级“守合同重信用”企业,连云港市“最具成长力创业企业”。江苏诺泰澳赛诺生物制药股份有限公司第三次通过国家高新技术企业复审认定,江苏省多肽类药物工程技术研究中心验收通过。
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论