
PDC整合了多肽的优势,与ADC相比,其分子量更小,不易引起自身免疫反应;与抗体生产的复杂工艺过程相比,PDC更易合成与纯化,有效降低大规模生产的成本,有望成为继小分子药物、单克隆抗体、ADC药物之后新一代靶向抗癌药物。PDC由三个部分组成:靶向肽、连接子、细胞毒性药物,通过一个连接子将特定的多肽序列与细胞毒素共价结合。
PDC 和 ADC 的对比

资料来源:广发证券
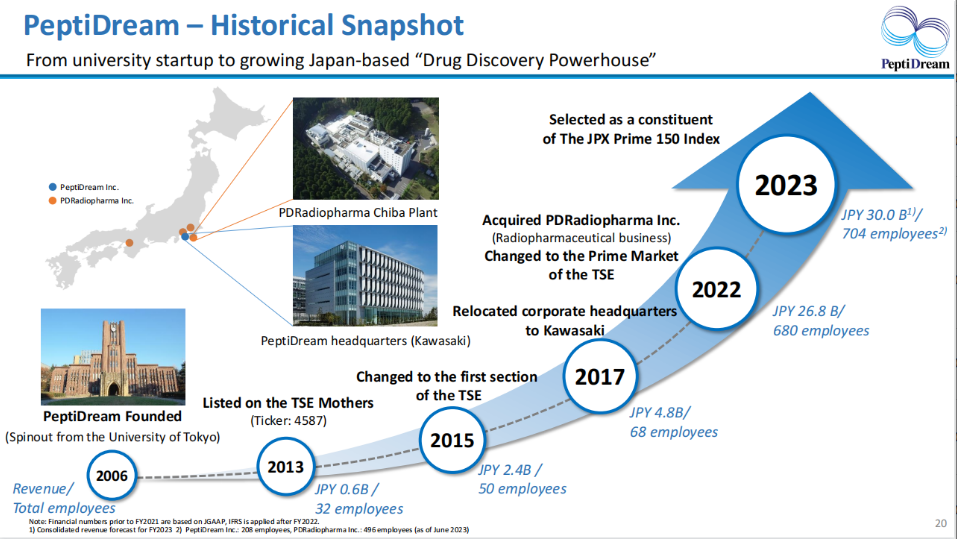
除了第一三共的ADC全球闻名以外,日本在肽药物偶联物(PDC)药物也走在前列。PeptiDream是一家位于日本的生物制药公司,成立于2006年。PeptiDream的独特之处在于公司专有的多肽发现平台系统(PDPS)能以高效率生产高度多样化的非标准多肽库,用以鉴定高效和选择性命中候选物。
近日,PeptiDream发布2023年中报:上半年实现营收94.26亿日元(0.64亿美元),同比增长87.6%;净利润为-7.29亿日元;研发费用为15.06亿日元,同比增长29%。目前PeptiDream主营构成主要是药物发现和开发业务和放射性制药业务。公司预计2023年营收为300亿日元,员工将达704人。(1 日元 =0.0068 美元)
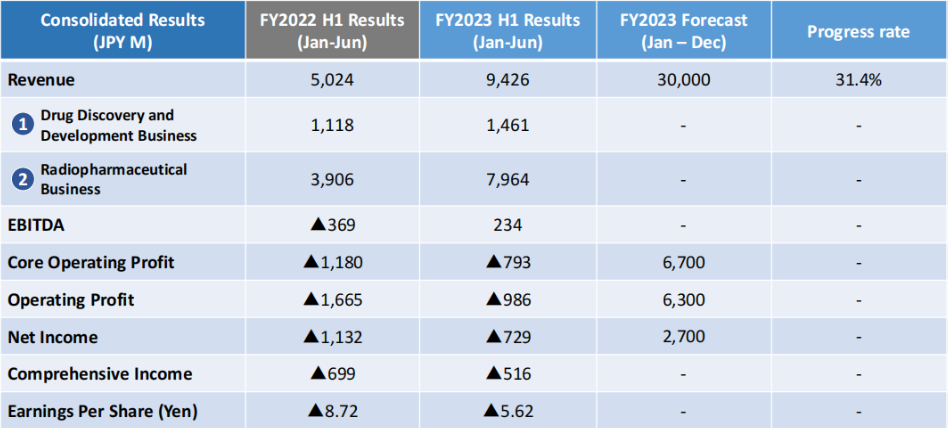
上半年药物发现和开发业务营收15.61亿日元,公司表示有望接近2023财年的预测,尽管最初预计的交易延迟将在上半年完成;放射性制药业务营收79.64亿日元,公司表示尽管市场存在“阻力”,但在保持盈利能力和实现未来增长方面的努力取得稳步进展。
截至2022年12月31日,该公司已将其PDPS技术非独家授权给11家公司:百时美施贵宝(2013年)、诺华(2015年)、礼来(2016年)、基因泰克(2016年)、盐野木(2017)、MSD(美国- merck & Co. Kenilworth, NJ, USA)(2018)、MiraBiologics(2018)、Taiho Pharmaceutical(2020)、Janssen(2020)、Ono Pharmaceutical(2021)和Fujirebio(2022)。
在对外授权合作方面,近两年PeptiDream合作金额超80亿美元。
在2021年7月分别和武田、Alnylam达成合计高达57亿美元的PDC药物开发合作,2022年12月26日,又与礼来达成高达12.35亿美元的PDC药物的创建和开发达成联合研究和许可协议。2022年12月27日 ,PeptiDream 宣布与MSD就新型肽药物的发现和开发达成最高21亿美元合作和许可协议。
多肽偶联物(PDC)是PeptiDream重点布局方向,目前已经布局了40多个PDC项目,包括蛋白、抗体、核酸(DNA或siRNA)、多肽、小分子和核素等。截至2023年6月30日,公司的管线包括127个发现和开发项目。
目前公司的主要研发管线如下:
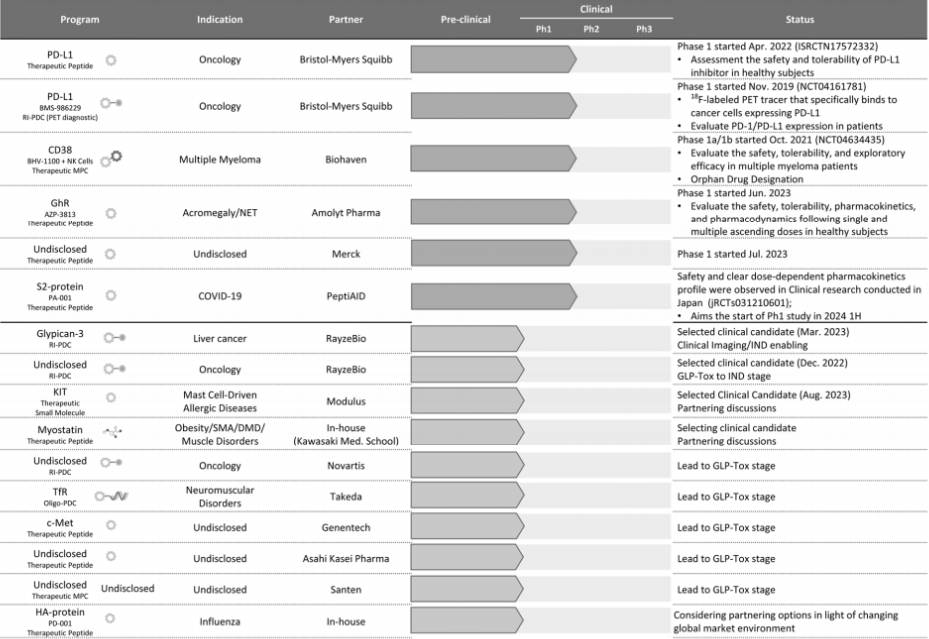
据药融云数据,目前PDC的在研产品以国外公司为主,研发进展较快且活跃的公司有Oncopeptipes、Bicycle Therapeutics、Cybrexa Therapeutics等。国内布局该领域的企业有盛诺基医药、同宜医药、泰尔康生物、汉鼎医药、博瑞生物、智肽生物和主流源生物等。其中盛诺基医药与加拿大公司Angiochem合作开发的SNG1005(paclitaxel trevatide),正在中国开展III期临床试验,是国内进展最快的PDC项目。
SNG1005临床试验研发进展

数据来源:药融云中国临床试验数据库
总结
目前PeptiDream多肽偶联物PDC领域进展最快的还处在临床1期,布局的靶点包括PD-L1、CD38、TfR、c-Met等,PeptiDream是PDC药物领域集大成者,其研发布局非常值得借鉴。目前全球获批的ADC药物已经有15个,目前仅有2个PDC药物获批上市Lutathera和Melflufen。2018年1月,美国FDA批准诺华研发的全球首款PDC药物 Lutathera,用于治疗生长抑素受体阳性的胃肠胰腺神经内分泌肿瘤(GEP-NETs)成人患者;2022年和2023H1分别实现销售额4.71亿美元和2.99亿美元。
2022年8月19日,Oncopeptides宣布欧盟委员会授予其药物Pepaxti(melphalan flufenamide,又称为melflufen)上市许可,与地塞米松(dexamethasone)联用,以治疗多发性骨髓瘤成人患者。不过2021年10月,melflufen在美国上市仅7个月,因为安全性原因被撤回,但不该行业向前发展的大趋势。
总的来说,目前PDC药物领域,行业关注度相对不高、整体处于早期阶段,国内外竞争格局良好。
资料来源:
1.PeptiDream财报
2.药融云数据库
3.广发证券
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论