5月24日,CDE公开征求《关于无参比制剂品种仿制研究的公告(征求意见稿)》意见。
核心在于,临床价值,详情见下:

为积极做好无参比制剂品种仿制研究工作,药审中心在前期调研的基础上,起草了《关于无参比制剂品种仿制研究的公告(征求意见稿)》。经请示国家药监局同意,现在中心网站予以公示,以广泛听取各界意见和建议。
我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。
您的反馈意见请发到以下联系人的邮箱:
联系人:王佳、汪小燕
邮箱:wangjia@CDE.org.cn,wangxiaoyan@CDE.org.cn
感谢您的参与和大力支持!
附件:
1. 《关于无参比制剂品种仿制研究的公告(征求意见稿)》
2. 《关于无参比制剂品种仿制研究的公告(征求意见稿)》起草说明
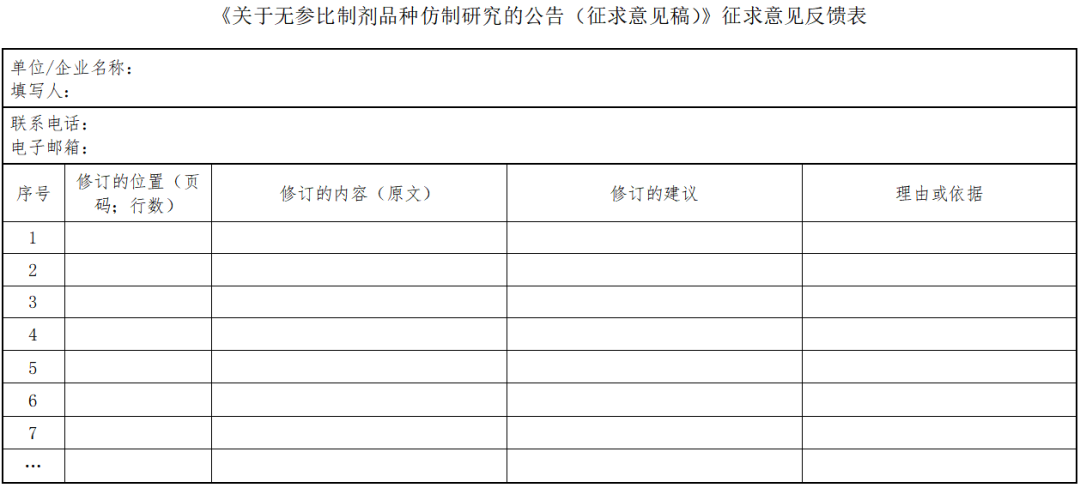
3. 《关于无参比制剂品种仿制研究的公告(征求意见稿)》征求意见反馈表
药品审评中心
2023年5月24日










<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论