
近日(10月24日),健达九州(北京)生物科技有限公司(以下简称“健达九州”)自主研发的基因治疗药物GA001注射液,获美国食品药品监督管理局(FDA)授予快速通道资格(Fast Track Designation, FTD),用于治疗由视网膜色素变性(RP)导致的晚期盲症。该资格的获得将有助于加速药物的临床试验与上市注册进程,显著缩短其上市周期。
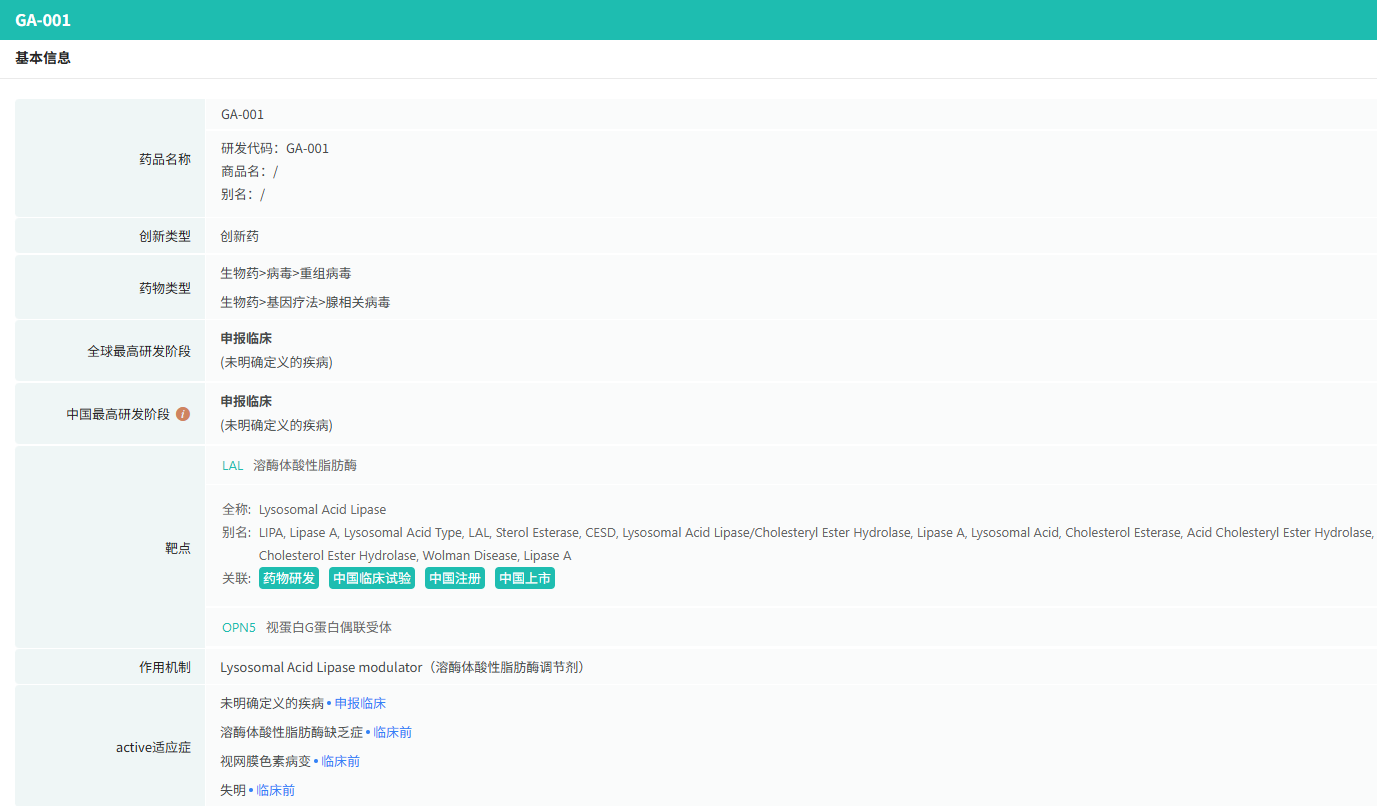
截图来源:摩熵医药数据库-全球药物研发数据库
此次GA001注射液针对RP适应症获得FTD认定,是继今年3月取得孤儿药资格(ODD)以及近期获得FDA II期临床试验许可之后,该药物的又一重要里程碑。这一进展表明其临床价值与研发潜力获得了国际监管机构的认可,并将进一步增强健达九州在基因治疗领域的核心竞争力。
未来,健达九州将继续秉持“改善人类健康,让每个生命拥有更好的现在与未来”的企业愿景,加快推进GA001注射液的临床试验进程,力争早日为全球患者提供更优质的治疗方案。
关于快速通道资格(FTD)
FTD是FDA为加速针对严重疾病且存在未满足临床需求的新药研发而设立的资格认定。获得认定的药物可在研发全周期中与FDA开展更频繁的早期沟通,及时解决研发过程中遇到的问题;在提交新药上市申请(NDA/BLA)时,还可采用滚动递交模式提交研究资料,为药物的快速获批提供多重保障。
参考来源:
[1] NMPA/CDE/FDA官网
[2] 摩熵医药(原药融云)数据库
[3] 公司官网/官方披露
扩展阅读:
1. 百济神州靶向BTK CDAC药物获FDA快速通道资格,挑战难治性白血病
2. FDA上半年新药批准创下3个“新高” 代表了药物研发的哪些趋势
3. 第一三共/阿斯利康合作,研发ADC新药Dato-DXd获FDA批准
4. 翰宇药业利拉鲁肽注射液FDA获批,解决2型糖尿病患者用药难题
5. 芳拓生物:FT-002获FDA批准成为国内首个rAAV基因治疗药物在美国开展II期临床
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论