
12月11日,葛兰素史克(GSK)宣布,口服疗法Gepotidacin获美国FDA批准补充新药申请,用于治疗12岁及以上(体重≥45kg)单纯性泌尿生殖系统淋病患者,该申请此前获FDA优先审查。这是三十多年来首个获批治疗淋病的新型抗生素。

截图来源:GSK官网
Gepotidacin是一款first-in-class新型口服抗生素,具有独特的药物特性与作用机制,其结构属于三氮杂苊烯类,不同于现有喹诺酮类抗生素。和喹诺酮类仅单一抑制拓扑异构酶II(Top II)或拓扑异构酶IV(Top IV)不同,Gepotidacin可选择性且均衡抑制细菌 DNA 回旋酶(Top II 的亚型)与 Top IV,通过双重作用阻断细菌DNA复制。
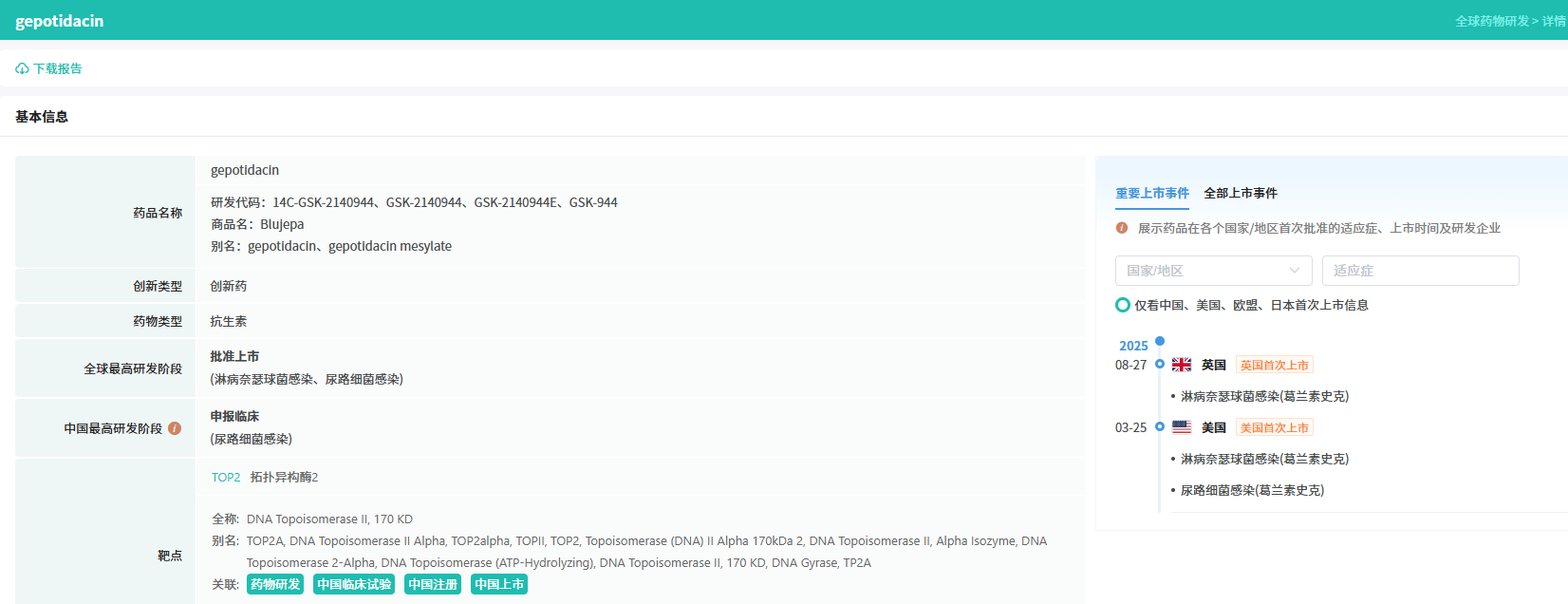
截图来源:摩熵医药数据库-全球药物研发数据库
今年3月25日,Gepotidacin(商品名:Blujepa)首次获FDA批准,用于治疗单纯性尿路感染(uUTI)的成人女性患者(≥40 kg)及12岁以上青少年患者(≥40 kg),这也是30多年来首个获批治疗uUTI的新型口服抗生素。
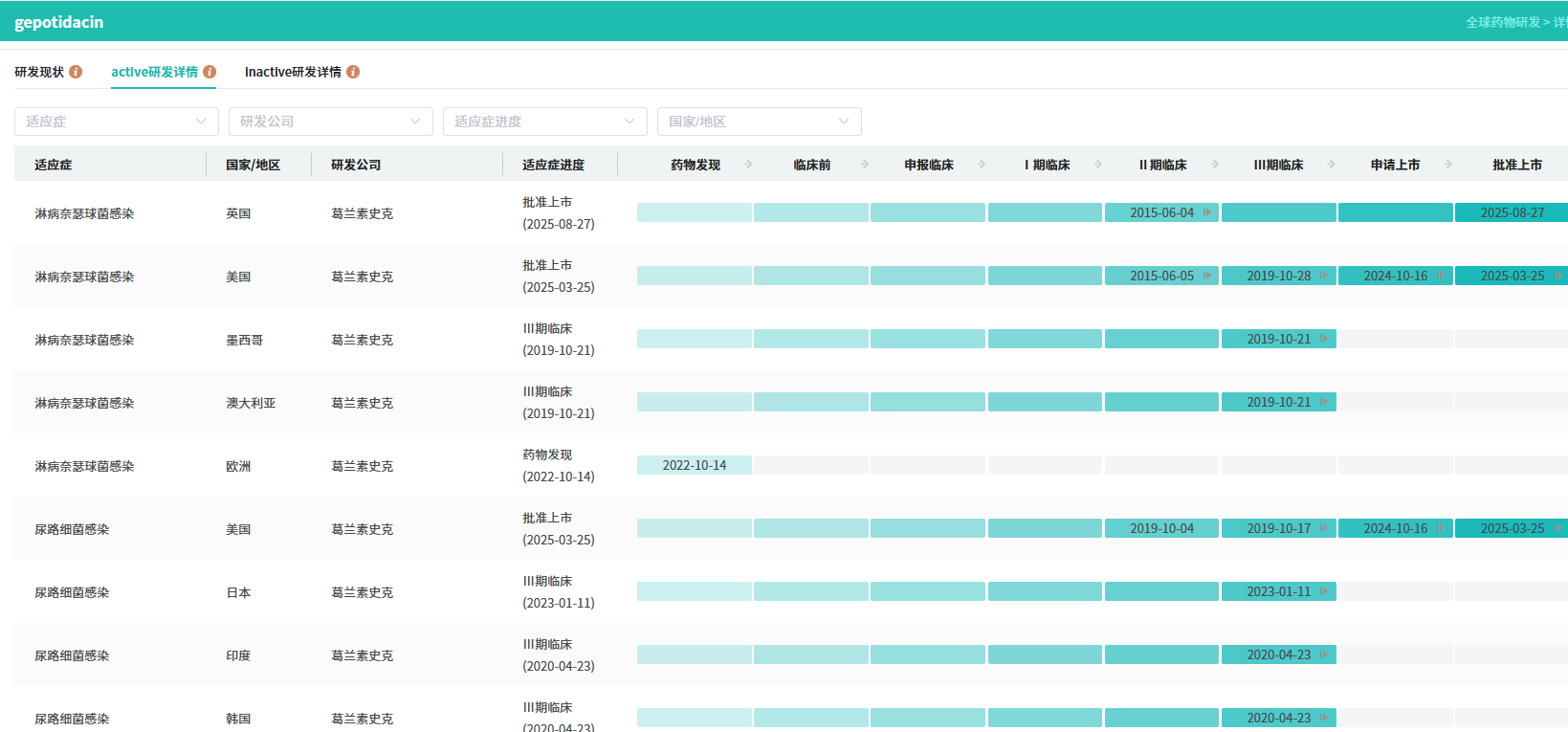
截图来源:摩熵医药全球药物研发数据库
Gepotidacin新适应症获批基于EAGLE-1 III期试验(NCT04010539,属全球性III期综合项目,结果2025年4月发表于《柳叶刀》)。该非劣效性试验纳入约600例单纯性泌尿生殖系统淋病患者,对比口服两剂Gepotidacin(3000毫克/次)与肌注头孢曲松(500毫克)联合口服阿奇霉素(1000毫克)的疗效与安全性。
结果显示,Gepotidacin组治疗成功率92.6%,头孢曲松联合组91.2%,均无因淋球菌持续感染致治疗失败案例,且安全性良好,无严重不良事件,常见不良反应为轻至中度胃肠道反应。淋病是公共卫生重要挑战,2023年美国报告超60万例,居性传播感染报告数第二位,尚无预防疫苗,临床对口服治疗需求迫切。Gepotidacin的获批填补了这一空白,为患者提供便捷新选择。
参考来源:
[1] GSK官网/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. GSK2023年业绩:RSV疫苗破15亿美元,继续领先辉瑞!
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论