
4月12日,在2026年美国妇科肿瘤学会(SGO)年会上,艾伯维以口头报告形式公布了FRα ADC药物Mirvetuximab Soravtansine(MIRV)联合卡铂治疗铂敏感卵巢癌(PSOC)的II期临床(IMGN853-0420)数据。结果显示,该联合方案客观缓解率(ORR)达68%,成为首个证实ADC与卡铂在卵巢癌中可联合使用的临床试验,为铂敏感卵巢癌治疗带来新突破。

一、突破治疗瓶颈,ORR达68%印证联合方案潜力
据摩熵医药数据库显示,MIRV是艾伯维自ImmunoGen收购的全球首款获批上市的FRα ADC药物,采用SPDB连接子、DM4毒素,DAR值为4,现用于治疗FRα阳性铂耐药上皮性卵巢癌等成年患者,此次新数据探索了其在铂敏感卵巢癌领域的应用前景。MIRV在2022年11月14日在美国首次上市,2024年11月22日在中国首次上市。
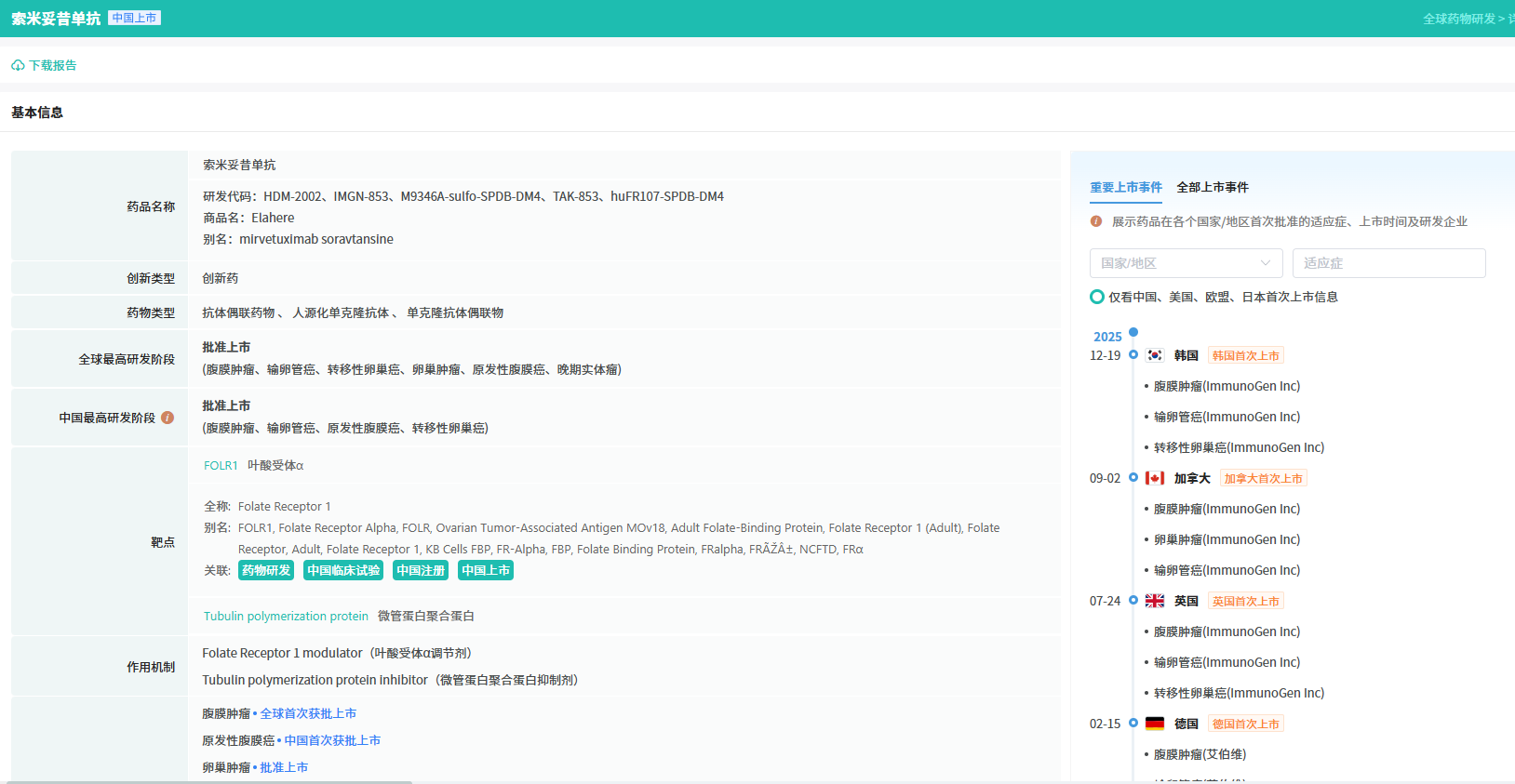
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
本次公布的IMGN853-0420是一项多中心、开放标签II期试验,共纳入125名FRα表达≥25%的铂敏感卵巢癌患者,其中48.8%既往接受过PARP抑制剂(PARPi)治疗。
试验采用“联合诱导+单药维持”模式:患者首先接受MIRV联合卡铂治疗6-8个周期,未进展者继续接受MIRV单药维持治疗。
有效性数据显示:
- 整体ORR达68%,显著高于临床试验预设假设;
- 91%患者(112/123)出现靶病灶缩小,81%患者在联合治疗后未进展并进入维持治疗阶段,且疗效持续或加深;
- 中位无进展生存期(PFS)为11个月,与PARPi治疗历史数据(8-12个月)基本持平;
- 亚组分析显示,PARPi初治患者ORR更高(72.6% vs 63.9%),但PARPi经治患者仍保持较高缓解率,验证了该方案在“临床代表性人群”中的价值。
二、安全性可控,毒性谱呈“化疗特征”
安全性方面,MIRV联合方案的主要不良事件呈现明确的化疗相关性特征,且整体可控:
- 眼部事件:为主要不良事件,但多为低级别、可逆性角膜事件;≥3级眼部治疗相关不良事件(TRAE)导致MIRV减量、延迟给药及停药的比例均为4.0%。
- 骨髓抑制:联合期 vs 维持期对比显示显著改善——血小板减少(50%→10%,降幅80%)、中性粒细胞减少(46%→22%,降幅52%);无出血性血小板减少或发热性中性粒细胞减少报告。
- 其他风险:≥3级血小板减少及中性粒细胞减少导致减量/延迟给药比例分别为5.6%和11.2%;2例药物相关肺炎死亡(已知风险,需主动监测),肺炎多为低级别且可缓解。
此外,≥3级TRAE导致卡铂停药4.8%、MIRV停药4.0%,整体安全性特征与已知风险一致。
三、拓展应用边界,布局新辅助化疗
MIRV作为全球首款获批的FRα ADC药物,此前已获批用于FRα阳性、铂耐药上皮性卵巢癌等适应症。此次II期数据的公布,进一步拓展了其在铂敏感卵巢癌领域的应用前景,尤其为PARPi经治患者提供了有潜力的后续治疗选择。
目前艾伯维正在评估MIRV联合卡铂作为新辅助化疗(NACT)的应用,相关GOG-3115试验正在进行中,有望进一步丰富该药物的临床应用场景。
参考来源:
[1] 企业官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 艾伯维乌帕替尼缓释片新适应症获受理,优先审评开启白癜风治疗新篇!
2. 艾伯维与Genmab合作新突破:CD3×CD20双抗Epkinly在R/R DLBCL III期试验中PFS显著改善
3. 荣昌生物与艾伯维达成56亿美元BD合作,RC148双抗“出海”加速全球化
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论