随着“优先审评”“快速通道”“突破性疗法”“有条件批准”等特殊审评审批通道的开通,创新药的审评审批速度得以大幅提高。截至6月30日,2021年国家药品监督管理局(NMPA)已经批准了36个新药(含化药和治疗用生物制品,不含中药、蛋白、疫苗、血液制品和细胞制品)上市,这些产品的上市将大幅改善我国的用药需求,尤其是在肿瘤和罕见病两大领域。
在2021年获批上市的36个新药中,进口新药有22个,国产新药有14个。就治疗领域而言,这些产品主要集中在六大治疗领域,其中肿瘤和免疫领域达15个,几乎占到总数的一半。在进口新药中,有5个产品为2020年在欧美日刚刚首次获批上市的产品,而国产新药中,有11个为全球首次获批上市的新分子实体。
值得一提的是,相比2020年同期,2021年获批上市的国产新药数量有明显增加的趋势,我国创新药的发展已到集中爆发阶段。为了方便广大同仁了解行情,笔者对2021年上半年获批上市的14个本土创新药进行简要介绍。
伏美替尼(Furmonertinib)
2021年3月2日,NMPA优先审评并附条件批准了上海艾力斯医药的第三代表皮生长因子受体(EGFR)激酶抑制剂伏美替尼(商品名:艾弗沙),用于经检测确认存在EGFR T790M突变阳性的局部晚期或转移性非小细胞性肺癌(NSCLC)成人患者的治疗。截止目前,伏美替尼尚没有完成三期临床研究,一项开放性的单臂2b期临床试(NCT03452592)验数据显示,220名EGFR T790M突变阳性的患者接受了本品80mg治疗,163名患者出现缓解,总缓解率(ORR)为74%[i]。我国2015年新发肺癌病例数高达73.3万例[ii],治疗需求巨大,其中约40%的NSCLC患者是EGFR 阳性,而EGFR敏感患者在经过一二代EGFR抑制剂治疗后,通常会出现进展,其中一半以上是T790M突变。尽管NMPA此前已经批准了奥西替尼和阿美替尼,但本品的上市将进一步丰富患者的治疗选择,降低治疗成本。

泰它西普(Telitacicept)
2021年3月9日,NMPA优先审评并附条件批准了荣昌生物的泰它西普(商品名:泰爱),与常规治疗联合,适用于在常规治疗基础上仍具有高疾病活动的活动性、自身抗体阳性的系统性红斑狼疮(SLE)成年患者。本品是B淋巴细胞刺激因子(BLyS)受体跨膜蛋白活化物(TACI)的融合蛋白,可通过抑制BLyS和增殖诱导配体(APRIL)的活性而发挥生理学作用。一项公开发表在美国风湿病学会(ACR/ARP)2019年年会上的2期临床试验(NCT02885610)数据显示,249 名患者随机接受本品80 mg (n=62)、160 mg (n=63)、240 mg (n=62) 或安慰剂 (n=62)治疗,第48周的SRI4(SLE应答指数)应答率分别为71.0%、68.3%、75.8%和33.9%,SELENA-SLEDAI(SLE疾病活动指数)评分下降超过4分的患者比例分别为75.8%、77.8%、79.0%和50.0%,而不良反应发生率分别为93.5%、92.1%、90.3%和82.3%[iii]。《2020中国系统性红斑狼疮诊疗指南》数据显示,我国SLE患病率约为30~70/10万,具有巨大的治疗需求,而本品的上市将为患者带来全新的治疗选择。
优替德隆(Utidelone)
2021年3月11日,NMPA优先审评批准了成都华昊中天药业的优替德隆(商品名:优替帝),与卡培他滨联合,用于既往接受过至少一种化疗方案的复发或转移性乳腺癌患者治疗。优替德隆为埃坡霉素类衍生物,可促进微管蛋白聚合并稳定微管结构,诱导细胞凋亡。在一项开放性的3期临床试验(NCT02253459)中,405名转移性乳腺癌患者按2:1的比例分别接受本品+卡培他滨或卡培他滨单药治疗,本品+卡培他滨治疗组患者中位无进展生存期(PFS)为8.4个月,总生存期(OS,意向人群分析)为19.8个月,而卡培他滨单药治疗组PFS和OS仅分别为4.3个月和16.0个月,以PFS统计风险比为0.46,以OS统计风险比为0.75[iv][v]。流行病学数据显示,我国乳腺癌年新发病例数达27.2万例[vi],治疗需求巨大,本品的上市将为广大患者带来新的希望。

磷丙泊酚(Fospropofol Disodium)
2021年5月19日,NMPA批准了人福的短效静脉全身麻醉药磷丙泊酚。磷丙泊酚为丙泊酚的水溶性前药,早在2008年就已经获得FDA批准上市(商品名Lusedra),用于成人诊断或治疗过程中的监护麻醉(MAC)。Globaldata检索结果显示,磷丙泊酚在中国已经开展了4项临床试验,分别为两项三期试验、一项二期试验和一项一期试验。一项公开在美国麻醉医师协会(ASA)2019年会的三期临床试验(CTR20170405)数据显示,540名中国受试者按2:1的比例分别接受了本品(20mg/kg)或丙泊酚脂肪乳(2mg/kg)治疗,两组患者在给药后5 分钟内 MOAA/S(改良警觉镇静评分量表)评分成功达到 1 级的比例(主要终点)均为97.7%,达到非劣性标准[vii]。本品的获批,满足了脂肪乳不耐受患者的用药需求,但用药剂量比较大,潜在的安全性问题值得长期关注。

帕米帕利(Pamiparib)
2021年4月30日,NMPA优先审评并附条件批准了百济神州的帕米帕利(商品名:百汇泽),用于既往经过二线及以上化疗并伴有胚系乳腺癌易感基因(gBRCA)突变的复发性晚期卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。帕米帕利是一种多聚ADP-核糖聚合酶-1(PARP-1)和PARP-2的选择性、强效抑制剂,可通过抑制癌细胞DNA单链损伤的修复和同源重组修复缺陷,促进癌细胞凋亡[viii]。在一项针对晚期卵巢癌、输卵管癌和原发性腹膜癌或晚期三阴性乳腺癌患者设计的1/2 期临床试验(NCT03333915)中,113名BRCA1/2阳性、既往至少经历过二线治疗的卵巢癌患者接受了本品治疗,中位随访时间为12.2个月。铂敏感的患者亚组(n=90)ORR为64.6%,中位持续缓解时间(DoR)为14.5个月,疾病控制率(DCR)为95.1%,而铂耐药的患者亚组(n=23)ORR为31.6%,中位持续缓解时间(DoR)为14.5个月,疾病控制率(DCR)为94.7%[ix]。尽管已经有多个PARP抑制剂获批上市,但本品的获批有望进一步增加患者的治疗选择,同时降低治疗负担,

康替唑胺(Contezolid)
2021年6月1日,NMPA优先审评批准了上海盟科药业的康替唑胺(商品名:优喜泰),用于治疗对康替唑胺敏感的金黄色葡萄球菌(甲氧西林敏感和耐药的菌株)、化脓性链球菌或无乳链球菌引起的复杂性皮肤和软组织感染。康替唑胺为噁唑烷酮类抗菌药,可抑制70S起始复合体而达到抑菌的作用。Globaldata数据显示,本品已经完成了两项三期临床试验,其中一项是有589名患者参与、以利奈唑胺为对照的头对头试验(GDCT0331531),结果显示本品疗效非劣于利奈唑胺,治愈率分别为93.0% vs 93.4%,不良反应相当。耐甲氧西林的金葡菌和耐万古霉素的肠粪球菌感染是当今医药界的一大难题,治疗手段少,死亡率高。尽管在此之前,FDA已经批准了利奈唑胺和特地唑胺,但两个产品的敏感菌有差异,获批适应症也不相同,本品的获批将为临床新增加一道“防线”。

多纳非尼(Donafenib)
2021年6月8日,NMPA优先审评批准了苏州泽璟生物制药的甲苯磺酸多纳非尼(商品名:泽普生),用于既往未接受过全身系统性治疗的不可切除肝细胞癌患者。多纳非尼是一种血小板衍生生长因子受体(PDGFR)、Raf激酶、血管内皮生长因子受体(VEGFR)的多靶点抑制剂,在一项开放标签的三期临床试验中,668名符合入组条件的肝细胞癌患者(意向治疗),分别接受了本品或索拉菲尼治疗,全样本分析结果显示,本品和索拉菲尼治疗组的中位OS分别为12.1个月(n=328)和10.3个月(n=331),死亡风险下降了17%。在意向人群(ITT)中,结果也几乎类似,中位PFS分别为3.7个月和3.6个月,ORR分别为4.6%和2.7%[x]。由于乙肝病毒感染率高,故肝癌是我国发病率最高的癌症之一,2015年有46.6万新增患者[xi],治疗需求巨大,但是肝癌信息传递通路复杂,近年来药物鲜有实质性突破,本品的上市是众多肝癌患者的福音。

维迪西妥单抗(Disitamab Vedotin)
2021年6月8日,NMPA优先审评并附条件批准了荣昌生物制药的维迪西妥单抗(商品名:爱地希),用于至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃癌(包括胃食管结合部腺癌)患者的治疗。维迪西妥单抗由人表皮生长因子受体-2(HER2)抗体部分、连接子和细胞毒药物单甲基澳瑞他汀E(MMAE)构成。截止目前,维迪西妥单抗尚无三期临床的数据,但在一项开放性、单臂设计的二期临床试验(NCT03556345)中,初步体现出产品对胃癌治疗的安全有效性。该试验共招募了127名患者,其中59名患者既往接受过三线以上治疗,全样本分析下ORR为18.1%,中位PFS为3.8个月,中位总生存期为7.6个月。最常见的不良反应为白细胞减少 (52.0%)、脱发 (51.2%)、中性粒细胞减少 (48.0%) 和疲劳 (42.5%)[xii]。维迪西妥单抗是我国首个自主研发上市的抗体偶联药物(ADC),意义重大。
海曲泊帕(Herombopag)
2021年6月16日,NMPA优先审评批准了江苏恒瑞的海曲泊帕(商品名:恒曲),用于因血小板减少和临床条件导致出血风险增加的既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发免疫性血小板减少症(ITP)成人患者,以及对免疫抑制疗效不佳的重型再生障碍性贫血(SAA)成人患者治疗。在一项针对ITP患者设计的三期临床试验(NCT03222843)中,424名患者以2:2:1的比例分组,分别接受了本品2.5mg、本品5mg或安慰剂治疗,2.5mg治疗组8周应答(血小板计数≥50×109/L)率为58.9%,5mg治疗组为64.3%,而安慰剂组仅为5.9%,最常见的不良反应为上呼吸道感染 (42.2%)、泌尿道感染 (17.1%)、免疫性血小板减少性紫癜 (17.1%) 和血尿 (15%)[xiii]。本品是一种非肽类促血小板生成素受体(TPO-R)激动剂,全球范围内已经有多个产品获批上市,而本品的上市有望降低我国ITP患者的治疗成本。

赛沃替尼(Savolitinib)
2021年6月22日,NMPA优先审评并附条件批准了和记黄埔医药的赛沃替尼(商品名:沃瑞沙/ORPATHYS),用于含铂化疗后疾病进展或不耐受标准含铂化疗的、具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者治疗。赛沃替尼是一种选择性抑制MET激酶抑制剂,对MET 14号外显子跳变的肿瘤细胞增殖有明显的抑制作用。在一项单臂、开放标签设计的二期临床试验(NCT02897479)中,76名患者接受了本品治疗,ORR为49.2%,中位PFS为6.9个月,中位OS为14.0个月[xiv]。MET外显子14跳跃突变发生率约为3%~ 4%[xv],是继EGFR、ALK之后,研发最热门的靶点之一,仅在2020年就有tepotinib和capmatinib两大产品获批上市,本品的国际权益已经授权给了阿斯利康,目前在开展肾细胞癌(RCC)和与奥西替尼联合治疗NSCLC的临床试验,是最有望走出国门的产品之一。

艾米替诺福韦(Tenofovir Amibufenamide)
2021年6月22日,NMPA优先审评批准了江苏豪森的艾米替诺福韦(商品名:恒沐),用于慢性乙型肝炎成人患者的治疗。艾米替诺福韦是替诺福韦的亚磷酰胺药物前体,在2021 亚太肝病学会年会(2021 APASL)上,豪森公布了一项三期临床试验的结果,1005名乙肝患者2:1的比例分别接受本品25mg或替诺福韦二吡呋酯(300mg)48周,乙肝e抗原(HBeAg )阴性亚组中,本品治疗组有90.2%的患者HBV DNA<20 IU/mL,而在HBeAg阳性的中,这一数字为52.8%,均达到非劣性标准。另外,不论在HBeAg阳性还是阴性人群中,试验组的ALT正常化率显著高于对照组[xvi]。我国是乙肝病毒感染率最高的国家之一,《2020年全国法定传染病报告发病死亡统计表》数据显示,2020年我国乙型肝炎新发病例90.2万人,治疗需求巨大。虽然本品并非新分子实体,但剂量仅为替诺福韦二吡呋酯的1/12,与吉利德的丙酚替诺福韦相当,耐受性也有望达到丙酚替诺福韦的同一水平,市场潜力巨大。

海博麦布(Hybutimibe)
2021年6月25日,NMPA优先审评批准了浙江海正药业D 海博麦布(商品名:赛斯美),作为饮食控制以外的辅助治疗,可单独或与HMG-CoA还原酶抑制剂(他汀类)联合用于治疗原发性(杂合子家族性或非家族性)高胆固醇血症。为了获得NMPA的批准,该产品已经完成了两项关键性三期临床试验,其中单独用药试验(CTR20150787)共入组了374名患者,低密度脂蛋白(LDL-C)水平相比基线下降了14.6%,不良反应与安慰剂无统计学差异;而与阿托伐他汀联用试验(CTR20150788)共入组了255名患者,本品联合阿托伐他汀治疗组,LDL-C相比基线下降了16.4%,而阿托伐他汀剂量倍增(对照)组仅下降了6.8%,两组不良反应分别为7.9%%和13.6%[xvii]。本品是继依折麦布之后,在我国获批上市的第二个选择性胆固醇吸收抑制剂,将进一步满足我国高血脂患者的治疗需求。

艾诺韦林(Ainuovirine)
2021年6月25日,NMPA过优先审评批准江苏艾迪药业的非核苷类逆转录酶抑制剂艾诺韦林(商品名:艾邦德),与核苷类抗逆转录病毒药物联用,治疗成人HIV-1感染初治患者。本品与拉米夫定和替诺福韦联合用药的安全有效性在一项有630名HIV感染者参与的临床试验中(CTR20181797)进行了评估,江苏艾迪药业的公告信息显示,在病毒抑制效果方面,ACC007 与对照组依非韦伦方案,相互非劣等效,在不良反应尤其是各类神经系统和精神类不良事件的发生率方面,ACC007 优于对照组[xviii]。在此之前,已有多个非核苷类抗逆转录酶抑制剂获批上市,由于本品尚未公开大型临床试验数据,安全有效性的优劣无法比较,但本品的获批将为我国艾滋病患者提供一种新的治疗选择。
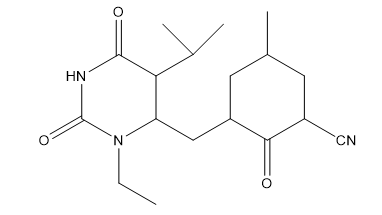
左奥硝唑酯二钠(Levornidazole Disodium)
2021年5月26日,NMPA批准了扬子江的左奥硝唑酯二钠,左奥硝唑酯二钠为硝基咪唑类抗生素左奥硝唑的前体药物,可迅速降解为左奥硝唑发挥治疗作用。在本品获批之前,扬子江已经完成三项药动学和一项安全有效性研究。在安全有效性研究(CTR20180384)中,总计有147人加入了临床试验,该试验在2019年已经完成,详细数据并未公开。

除了以上14个国产新药,值得一提的是,NMPA还批准了第一个CAR-T阿基仑赛,用于复发或难治性大B细胞淋巴瘤治疗。由于阿基仑赛(Axicabtagene Ciloleucel)属于细胞疗法,与传统药物有所不同,故笔者在此不作讨论。
我国上半年批准的国产或进口新药

以上数据仅基于作者个人统计,含化药和治疗用生物制品,不含中药、蛋白、疫苗、血液制品和细胞制品,截止日期为6月30日






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论