一、2021上半年部分国内上市药企研发费用
创新为帆,研发先行。截止2021年8月31日,国内上市药企中期业绩报告基本披露完毕(港股少部分公司还未公开),我们统计了上半年部分药企(含器械企业)研发费用数据,如下图:
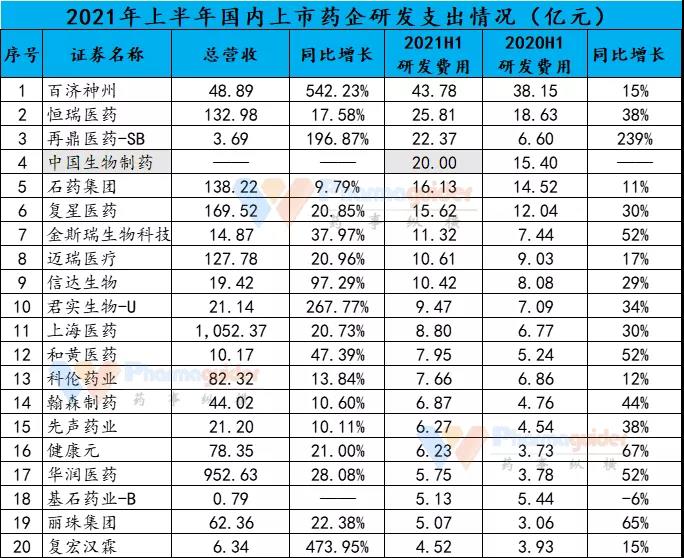
数据来源:上市公司中报 ;药事纵横整理 (中国生物制药此前是预估)
(1港元=0.8308人民币;1美元 ≈ 6.4665人民币)
上半年国内药企研发费用支出呈现以下几个特点:
1、从top20来看,大部分药企研发投入和去年同期相比大幅度增加,其中增长超过30%的有12家。其中再鼎医药今年上半年研发投入22亿元,同比大增2倍多。和黄医药、华润医药、健康元和丽珠集团上半年研发投入同比增长超过50%;
Top20里面研发投入5亿元以上的药企有19家左右,top9研发投入超过10亿元。
2、Big Pharma上半年研发投入大幅增长。其中恒瑞医药上半年研发投入25.81亿元,相比去年同期增长38%,占营收比例19%;报告期内,创新药实现销售收入 52.07 亿元,同比增长 43.80%,占整体销售收入的比重为 39.15%,创新成果的逐步收获对公司业绩增长起到了拉动作用。
翰森制药研发投入6.87亿元,同比大增44%;复星医药投入15.62亿元,同比增长30%;石药上半年研发投入16.13亿元,同比增长11%,按照成药板块112.3亿元营收来看,研发占比14%。中国生物制药在2021年一季度研发投入10.62亿元,上半年研发投入约19亿元。
2021 年上半年,华东医药在医药工业领域研发投入 5.36 亿元,同比增长 6.38%。
3、Biopharma 和Biotech类公司营收和研发投入大幅增长。
百济神州上半年营收48.83亿元,大增5倍,研发费用投入43.72亿元,排名第一,同比增长15%。
信达生物上半年营收暴增97%,达到19.42亿元,研发支出10.42亿元,同比增长29%。
金斯瑞生物上半年营收14.83亿元,同比增长38%,研发费用支出11.32亿元,同比大幅增加52%;
和黄医药和先声药业研发支出也是保持增长,两家公司研发支出分别同比增长52%和38%。复宏汉霖增长15%。
4、医疗器械中迈瑞医疗上半年营收128亿元,同比增长21%,研发费用支出10.61亿元,同比增长17%。
总结
从top20上半年研发支出来看,国内的药企创新力度正在加大。
在医药行业政策持续变革的大背景下,旧的医药市场格局正被打破,新的格局正逐步建立,推动着仿制药高质量发展,鼓励药物研发创新快速提升。未来,我国医药产业结构必将加速升级。
二、2021上半年跨国药企研发费用Top15
创新是穿越时代的主旋律,也是药企保持领先的重要抓手。
搞创新不是简单的请客吃饭,需要持续不断的投入大量的研发费用,跨国药企之所以能长期立于不败之地,除了强大的销售网络以及并购获得新资源以外,最核心的竞争力就是保持创新进化能力,不断的推出满足市场需求的新品。近期跨国药企的中报披露完毕,我们整理相关数据,按照研发费用排名如下:
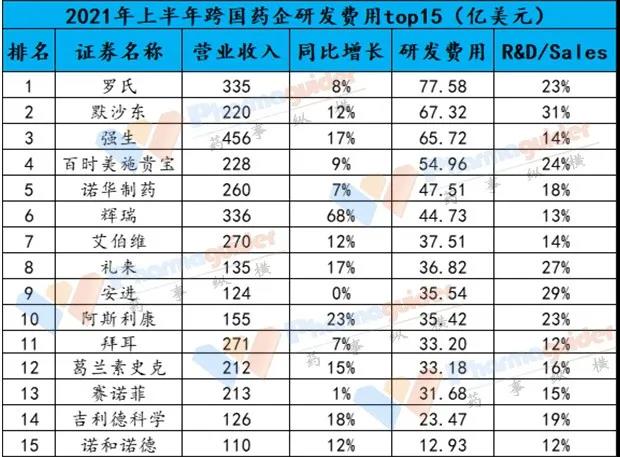
数据来源;公告 药事纵横
(强生R&D占制药业务营收26.5%;1欧元=1.1707美元;1瑞士法郎=1.091美元;1英镑=1.3648美元)
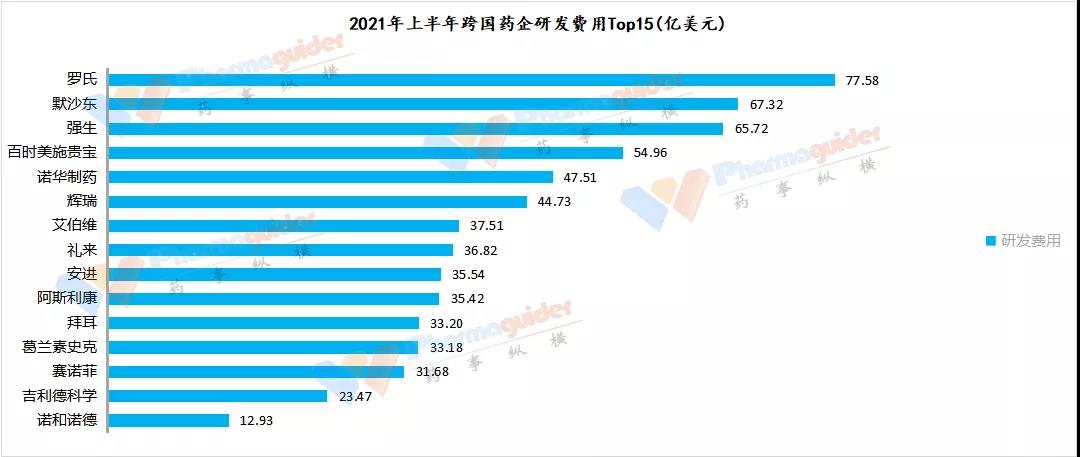
数据来源;公告 药事纵横(武田的财报周期不一致,故不在排名之内)

排名第一的是罗氏,上半年研发费用77.58亿美元,同比增长16%;营收为335亿美元,研发费用占营收比例为23%。
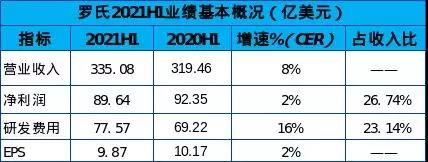
资料来源:罗氏公告 药事纵横 (1瑞士法郎=1.091美元)
据国盛证券统计,今年二季度,罗氏共3项上市申请获批(1NME+2AIs),3项处于申请阶段(1NME+2AIs),启动5项III期临床试验(1NME+4AIs),4项II期临床试验(3NMEs+1AI),2个新分子进入临床I期,进入临床及之后阶段的在研管线数总计达150个。其中上半年罗氏PD-L1单抗Tecentriq(atezolizumab,阿替利珠单抗)获批多个适应症。
图:罗氏2021H1新获批产品或适应症
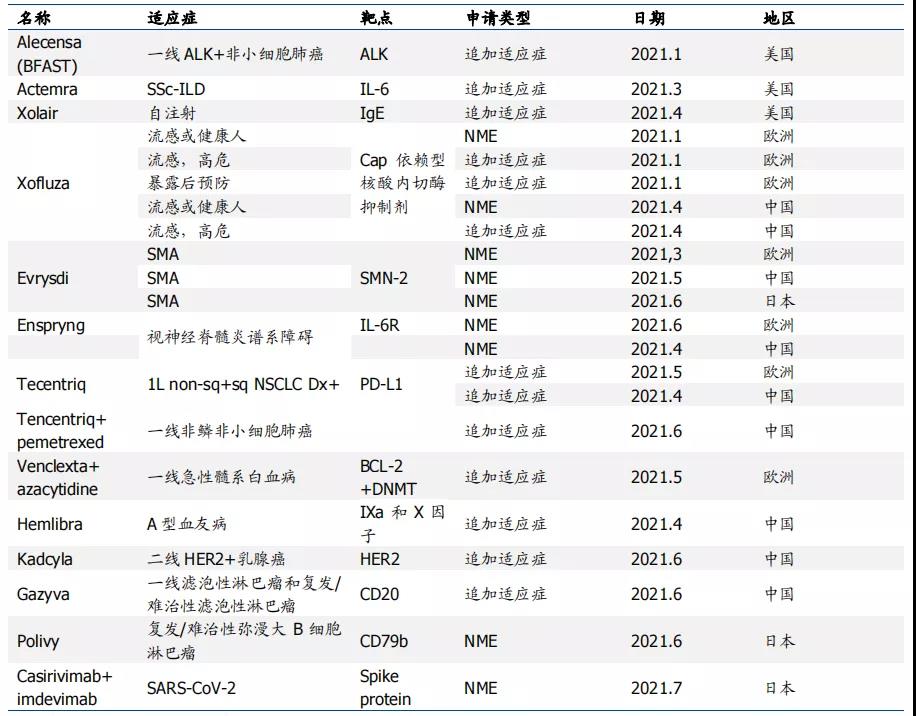
资料来源:罗氏公告 国盛证券研究所
三、默沙东
默沙东2021年上半年公司研发投入67.32亿美元,同比增长58%,其中2021Q2研发费用43.21亿美元。公司研发进展顺利,二期临床管线52个,三期临床管线25个。公司继续推进其肿瘤学产品组合的开发项目,预计到2028 年将有超过90 个潜在的新适应症。
近两月K药获批两个新的适应症:7月美国FDA批准KEYTRUDA用于治疗局部晚期皮肤鳞癌;8月FDA批准Keytruda与口服多受体酪氨酸激酶抑制剂Lenvima联用,一线治疗晚期肾细胞癌(RCC)成人患者。
疫苗方面:7月份,美国FDA批准了默沙东肺炎球菌15价结合疫苗Vaxneuvance上市,用于在18岁以上成人中预防由肺炎链球菌血清型1、3、4、5、6A、6B、7F、9V、14、18C、19A、19F、22F、23F和33F引起的侵袭性疾病。Vaxneuvance通过优先审查程序获得批准。目前,这款疫苗也正在接受欧洲EMA的审查。
COVID-19治疗产品:默沙东正在全力推进口服抗病毒药物molnupiravir(EIDD-2801/MK-4482)的开发。4月,默沙东宣布与印度知名仿药品制造商就Molnupiravir(莫诺匹韦,MK-4482,核糖核苷类似物)签订了非排他性自愿许可协议。6月,公司宣布与美国政府就Molnupiravir签订采购协议。

强生上半年营收456.33亿美元,同比增长16.9%,研发费用65.72亿元,同比增长24%;占营收比例在14.4%。业务收入主要分为制药、医疗器械和大健康三大板块。制药板块2021上半年销售额为247.98亿美元,同比增长13.3%;研发费用占制药业务营收比例为26.5%。
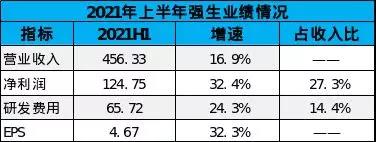
研发项目覆盖肿瘤、免疫、心血管、抗感染、代谢、神经系统、个人护理等领域,处于临床后期阶段产品共53项。
上半年强生在抗肿瘤研发方面成果显著:
2月份针对BCMA靶点的CAR-T疗法Ciltacabtageneautoleucel(cilta-cel)向欧洲药品管理局(EMA)提交了上市申请,用于治疗复发性和/或难治性多发性骨髓瘤(MM)。2019年12月FDA曾授予cilta-cel治疗MM的突破性疗法资格认定。
4月份cilta-cel完成向FDA滚动递交生物制剂许可申请(BLA),用于治疗复发性和/或难治性多发性骨髓瘤(MM)。
5月份DARZALEXSC在欧洲获批,用于治疗新诊断的系统性轻链(AL)淀粉样变性的成年患者,并额外获批用于多发性骨髓瘤二线治疗;
6月份Teclistamab(BCMA,CD3)用于复发或难治性多发性骨髓瘤获FDA突破性疗法
总结
从Top15来看跨国药企的研发费用上半年最低为是13亿美元,换算人民币84亿元左右,相当于百济神州一年的研发投入。就整体而言,和跨国药企研发投入相比,目前国内药企差距还很大,但中国的医药产业已经由仿制为主向创新为主的战略转变,未来的国内药企整体的研发投入会逐渐加大。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论