
12月1日,经药融云查询,华润双鹤药业/南京海鲸递交的阿普斯特片上市申请已进入行政审批阶段,若此次顺利获批,将成为该品种国内首仿。此前,也有兆科药业、齐鲁等多家企业以仿制新3类报产,但均折戟成沙,终未获批。
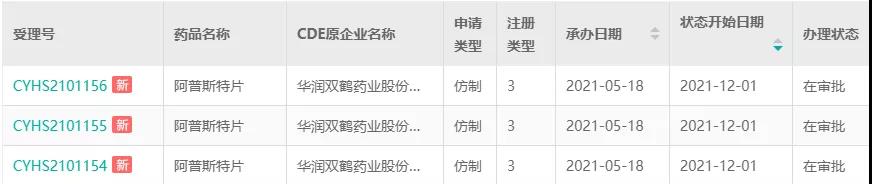
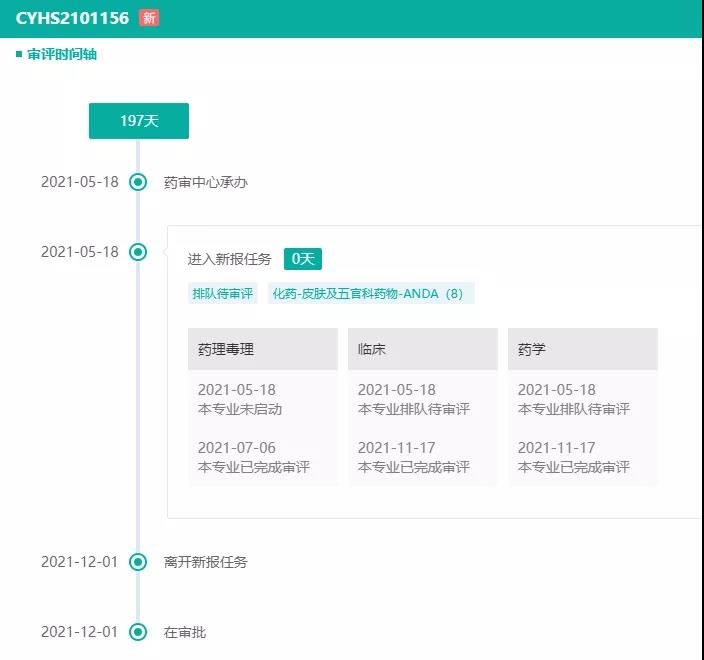
截图来源:药融云中国药品审评数据库
阿普米司特片原研由新基(Celgene)研发,2014年在美国上市(商品名:欧泰乐Otezla)。在全球,阿普米司特片已在50多个国家和市场获批,其在美国获批的适应症包括用于治疗成人活动性银屑病性关节炎、用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者、以及用于治疗与白塞氏病相关的成人口腔溃疡患者。
2019年8月,安进以高达134亿美元的价格获得了阿普米司特的全球权益。2021年2月,安进在中国提交阿普米司特上市申请并被纳入优先审评审批,今年8月获批上市,用于治疗符合接受光疗或系统治疗指征的中度至重度斑块状银屑病的成人患者。这是中国首个获批用于斑块状银屑病治疗的口服磷酸二酯酶4(PDE4)抑制剂。
据药融云全球药物研发数据库显示,这款产品全球销售额已达21.95亿美元。我国约有650万银屑病患者,中重度患者约占57.3%。不言而喻,该产品在我国的销售前景备受看好。因此,国内有多家企业进行积极布局。
目前朱养心药业、华润双鹤、桂林南药、石药欧意、齐鲁、兆科药业、江西青峰药业等均递交了上市申请,但尚未有企业获批。今年8月安进原研获批在中国上市后,其中多家企业以新4类再度报产(详见以下表格)。同时还有多家企业已获批临床、或正在进行BE试验。
阿普米司特片当前报产情况(已筛除未通过审批的受理号;标红为“在审批”状态)
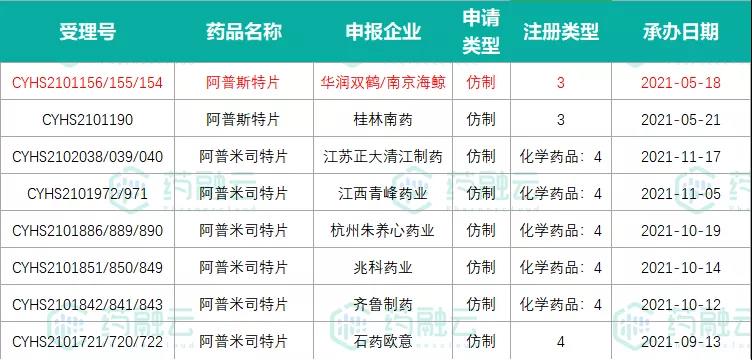
数据来源:药融云中国药品审评数据库
在接下来2-3年内阿普米司特的国产仿制药将迎来获批的井喷期,可以预见其竞争之激烈。
—END—























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论