
逆势上涨的De-SPAC医药股
从2020年开始,以SPAC(特殊目的收购公司)并购上市的模式在全球范围内掀起了一股热潮。SPAC的目的是收购一家私营公司帮助其上市,而标的公司不用通过传统的IPO程序,提供了一种快速且具有成本效益的IPO方式,对于生物技术公司来说极具吸引力。
但是过去两年,全球资本市场充满动荡、波折和不确定性,受美联储激进加息缩表以及SPAC本身交易结构等影响,以SPAC合并上市的股票表现并不尽如人意。
Moonlake Immunotherapeutics(NASDAQ:MLTX)是极少数在上市之后股价表现优异的De-SPAC医药企业,该公司在2022年4月完成与SPAC公司Helix Acquisition(NASDAQ:HLXA)合并上市(HLXA的发起人是华人女性Bihua Chen创办的著名生物医药投资机构Cormorant Asset Management)。此前,Moonlake曾获得BVF、Cormorant、RTW等知名生物医药投资机构的投资。
自上市以来,Moonlake涨幅超过330%,截至2023年10月12日,市值约32.84亿美元。
MLTX股价表现

IL-17新型纳米三抗
值得关注的是,这家尚处于临床阶段的生物技术公司仅凭一条核心管线便撑起了30多亿美元的市值。
其主打药物Sonelokimab(SLK)是一款在研的靶向IL-17A和IL-17F的新型三特异性纳米抗体,已开展针对银屑病、化脓性汗腺炎(HS)以及银屑病关节炎(PsA)的临床试验,这些疾病均是具有重大未满足医疗需求的炎症性疾病。

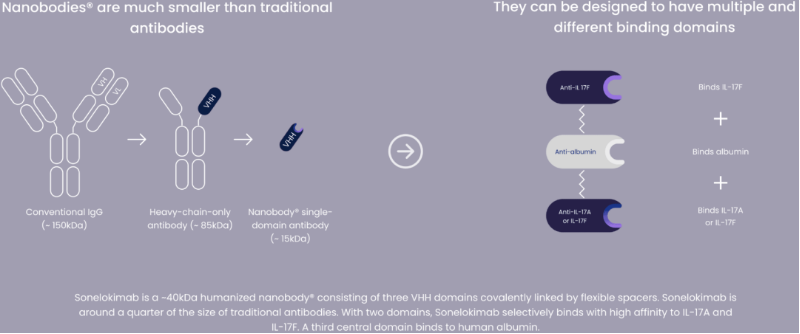
炎症性疾病的特点是药物往往难以到达深层次的组织,纳米抗体相较于传统抗体体积小得多,有望突破这一“瓶颈”,实现深层次的组织渗透。Sonelokimab是一种新型的人源化纳米抗体,由三个VHH结构域组成,由柔性甘氨酸-丝氨酸间隔物共价连接,分子大小约40k Da。通过两个结构域,Sonelokimab选择性地与IL-17A和IL-17F高亲和力结合,从而抑制IL-17A/A、IL-17A/F和IL-17F/F二聚体的形成,这些二聚体是炎症性疾病的核心驱动因素。第三个中心结构域与人白蛋白结合,促进Sonelokimab在炎性水肿部位的进一步富集。
药融云数据库显示,Sonelokimab原研是比利时纳米抗体公司Abylnx,该公司成立于2001年,是全球纳米抗体领军企业和技术佼佼者,在2018年被赛诺菲以39亿欧元收购,该公司拥有纳米抗体(Nanobody®)和纳米克隆(Nanoclone®)的商标权。
2013年,德国默克与Ablynx达成全球开发和商业化协议,获得了抗IL-17A/F纳米抗体Sonelokimab(ALX-0761/M1095)的专有权。2017年3月,CRO公司Avillion与德国默克签订了Sonelokimab的2期和3期开发协议。其中2期临床试验在2020年提前完成(NCT03384745)。
2021年4月,《柳叶刀》在线刊发Sonelokimab治疗中重度斑块型银屑病的2b期临床试验详细数据。该试验在第12周达到了主要终点,所有剂量组与基线相比均具有显著的临床和统计学意义(p <0.001)。次要终点方面,银屑病面积和严重程度指数(PASI 75,PASI 90和PASI 100)在第12周对比基线也具有显著的统计学意义(p≤0.002)。

截图自《柳叶刀》
该研究采用IL-17A抑制剂司库奇尤单抗(Cosentyx)作为阳性对照,与安慰剂相比,Sonelokimab在主要终点方面表现出显著的改善,并且在数值上优于采用现行标准治疗方案(司库奇尤单抗)的阳性对照组,在最高剂量组,57%的患者在24周后实现了PASI 100。同时,Sonelokimab耐受性良好,安全性与司库奇尤单抗组相似,第0~12周总的念珠菌感染率为2.9%,12~52周为6.4%。
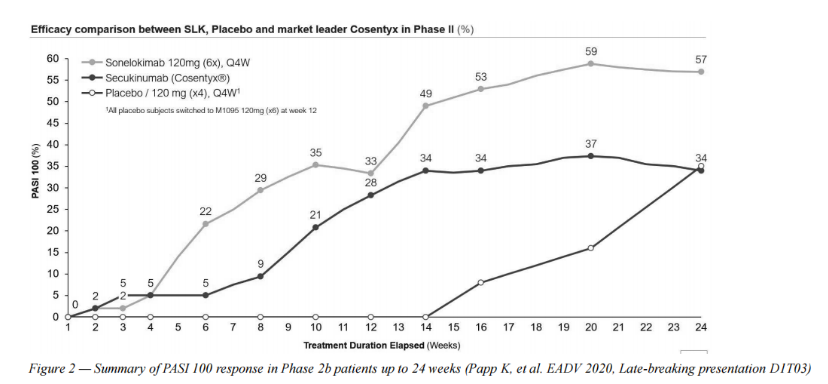
(所有安慰剂组患者在12周时转为Sonelokimab 120mg治疗)
同样在2021年4月,刚成立不久的MoonLake Immunotherapeutics AG(现为MoonLake Immunotherapeutics瑞士子公司)与默克签订许可协议,以2990万美元(包括2500万美元现金以及9.9%的股权)首付款以及未来高达3.071亿欧元的里程碑付款引进Sonelokimab(M1095),Moonlake将全权负责Sonelokimab的研究、开发与商业化。
基于此前的2b期临床数据,Moonlake肯定了Sonelokimab作为炎症性疾病治疗药物的潜力,以及与司库奇尤单抗相比,Sonelokimab显示出差异化的治疗结果。该公司认为细胞因子IL-17A和IL-17F在优化炎症反应和感染防御之间的平衡方面均具有重要性。
财务和运营状况
根据财报披露,Moonlake Immunotherapeutics公司2022年研发费用为4200万美元(+18.3%),一般及行政开支为2300万美元(+27.5%),全年净亏损6450万美元(+20.2%)。
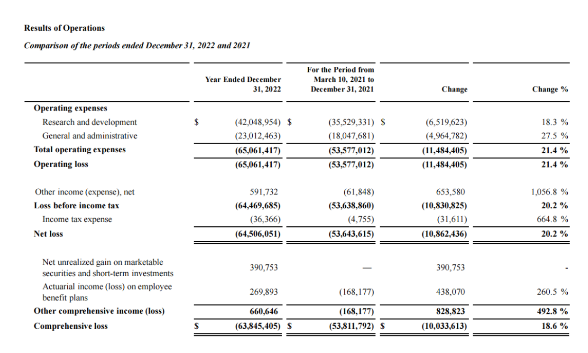
2023年上半年,公司研发费用为1610万美元(-25.6%),一般及行政开支为1000万美元(-16.3%),上半年净亏损2457万美元(-26.2%)。

2023年6月,MoonLake以每股50.00美元的价格完成了800万股A类普通股的公开发行,还授予此次发行的承销商以公开发行价格减去承销折扣和佣金,再购买120万股A类普通股的选择权,使本次发行的总收益达到4.6亿美元。因此截至2023年6月底,MoonLake持有的现金和现金等价物以及短期有价证券共8.63亿美元,足以支持Sonelokimab推进多项3期临床试验,并使公司在下一轮增长中处于非常有利的地位。
管线单一的biotech在产品开发与企业运营过程中往往需要承担巨大风险,用“一荣俱荣,一损俱损”来形容再贴切不过,因此在项目进展释放出积极信号的时期寻求资产出售也是一个抵御风险的不错选择。2023年7月14日,据路透社报道,有消息人士称,MoonLake正在寻求出售资产。消息人士称,该公司正与一家投资银行合作,并与对潜在收购有兴趣的制药商进行早期对话。对此,MoonLake并未立即回应置评请求。
另外,IL-17是免疫与炎症性疾病领域的热门靶点,吸引了众多企业争相布局,药融云数据www.pharnexcloud.com显示,国内布局IL-17赛道的企业有:智翔金泰、恒瑞医药、康方生物、三生国健、君实生物、鑫康合、丽珠生物、创响生物、荃信生物、华博生物、先声药业、再鼎医药、上药帛康、巨石生物、百奥泰、迈博太科、神州细胞、方坦思等。
参考:
NMPA/CDE;
FDA/EMA/PMDA;
相关公司公开披露(正文图片均来自企业官方,除非另有说明);
https://moonlaketx.com/;
Papp, Kim A et al. “IL17A/F nanobody sonelokimab in patients with plaque psoriasis: a multicentre, randomised, placebo-controlled, phase 2b study.” Lancet (London, England) vol. 397,10284 (2021): 1564-1575. doi:10.1016/S0140-6736(21)00440-2;
中国反常性痤疮/化脓性汗腺炎诊疗专家共识制订小组.中国反常性痤疮/化脓性汗腺炎诊疗专家共识(2021版)[J].中华皮肤科杂志,2021, 54(2):97-104. doi:10.35541/cjd.20200802;
https://www.businesswire.com/news/home/20211004005327/en/%C2%A0MoonLake-Immunotherapeutics-AG-and-Helix-Acquisition-Corp.-Announce-Business-Combination-Agreement-to-Create-Publicly-Listed-Biotechnology-Company-Advancing-Tri-specific-Nanobody%C2%AE-Sonelokimab;
https://www.merckgroup.com/en/news/statement-on-out-licensing-agreement-sonelokimab-03-05-2021.html;
https://www.reuters.com/business/healthcare-pharmaceuticals/moonlake-immunotherapeutics-explores-sale-sources-2023-07-14/;等等
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论