
1月5日,默沙东宣布,其创新药物 欣瑞来®(注射用索特西普)已在中国获得上市批准。该药物是全球首个且目前唯一获批的激活素信号传导抑制剂,适用于世界卫生组织(WHO)功能分级为II-III级的肺动脉高压成年患者,旨在改善患者的运动能力及功能状态。

截图来源:默沙东官微
这款药物源自默沙东于2021年以约115亿美元收购Acceleron公司所获得的核心资产。索特西普是一种首创的融合蛋白,通过独特的机制靶向并调节与肺动脉高压疾病进展相关的异常信号通路,旨在从根源上抑制肺部血管的异常重塑,从而治疗疾病。
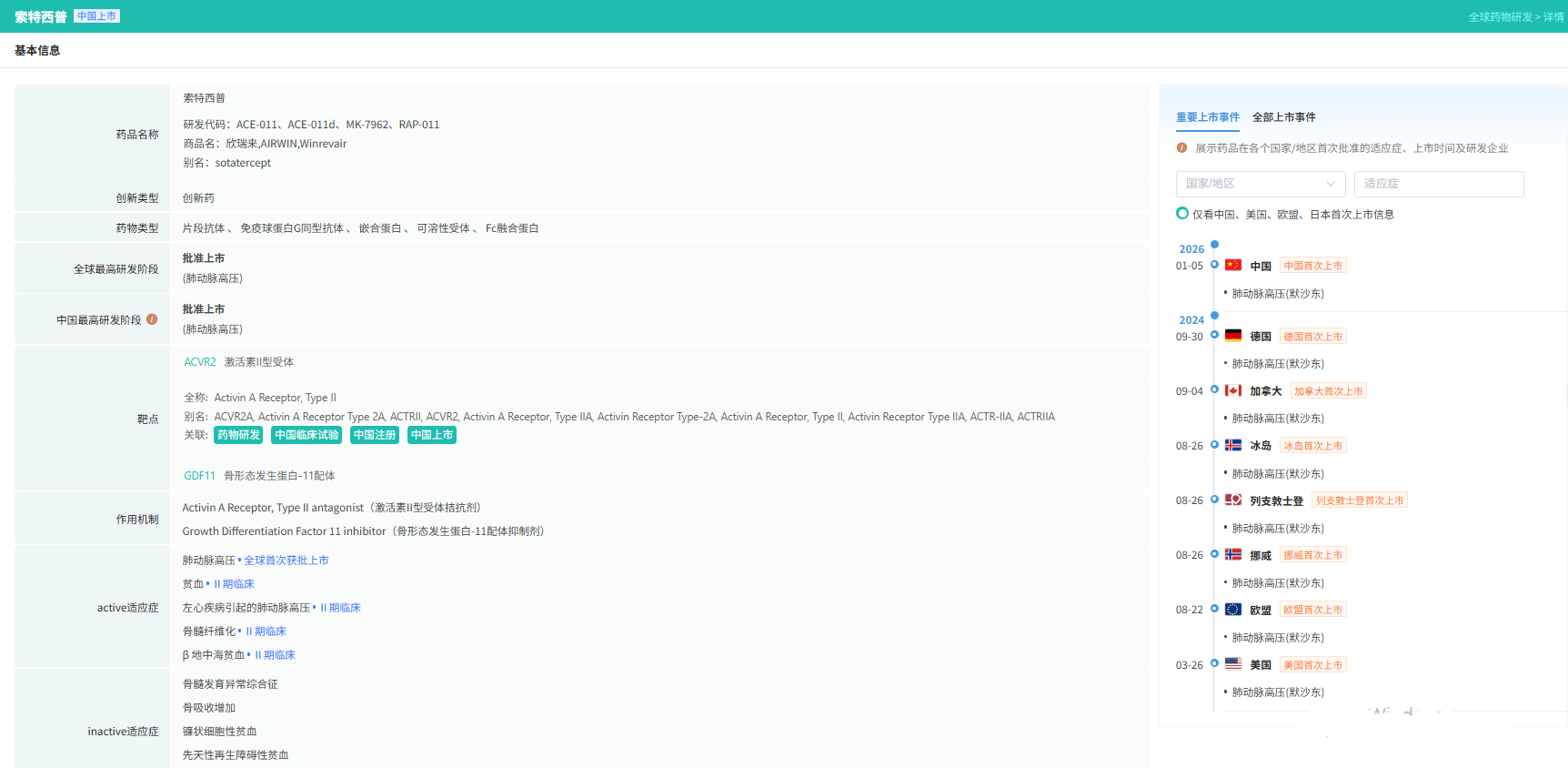
查数据,找摩熵!图源:摩熵医药全球药物研发数据库
据摩熵医药数据库显示,自2024年3月首次在美国获批以来,该药物(商品名:Winrevair)的商业化进程迅速,同年即在欧盟获批。其市场表现同样亮眼,上市首年全球销售额即达4.19亿美元,在2025年第二季度单季销售额更是达到3.36亿美元,展现出成为“重磅炸弹”药物的巨大潜力。进入2025年,该药继续拓展全球市场,相继在日本、韩国获批,此次在华获批标志着其全球化布局又迈出关键一步。
此次获批主要基于一项名为STELLAR的关键III期临床试验的积极数据。该研究显示,在稳定背景治疗基础上加用索特西普治疗24周后,患者的6分钟步行距离较基线显著增加了41米。更为重要的是,与单用背景治疗相比,索特西普将患者发生任何原因死亡或疾病临床恶化事件的风险降低了84%。
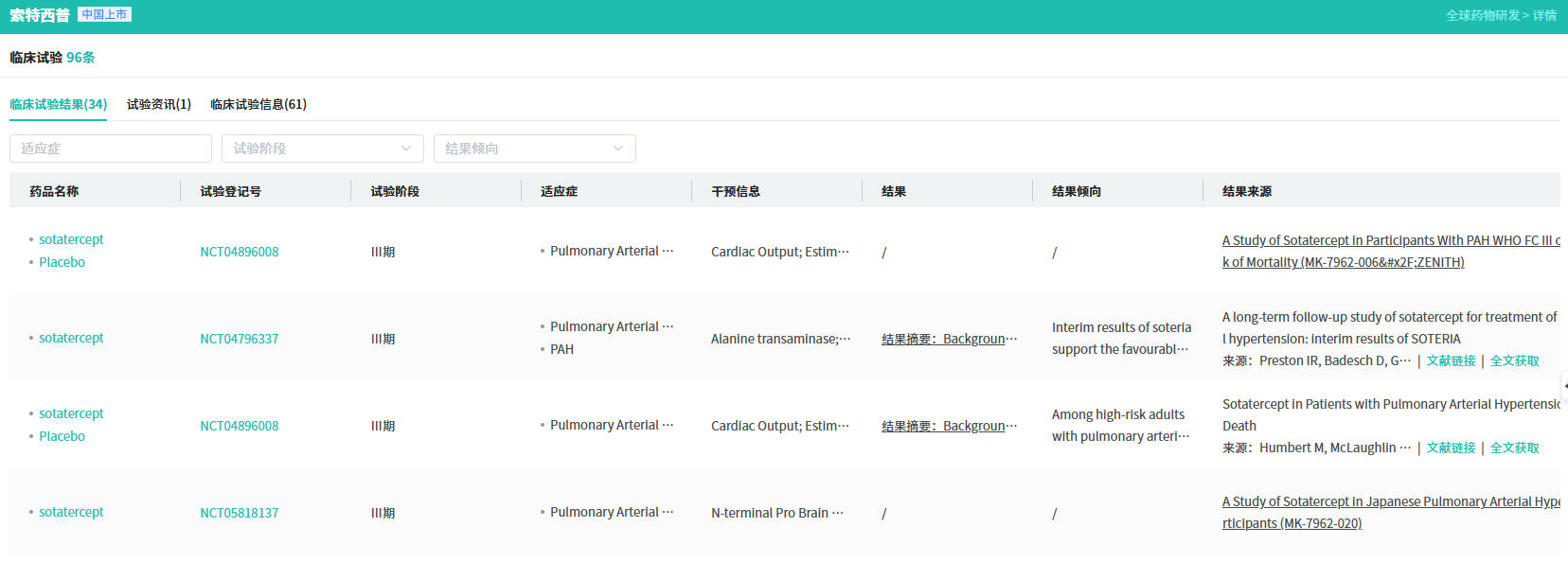
查数据,找摩熵!图源:摩熵医药全球药物研发数据库
除STELLAR研究外,多项后续III期研究也持续验证了其疗效。例如,针对高危患者的ZENITH研究,因其显著降低临床恶化事件风险达76%而提前终止,并支持了其在美国获批扩大适应症。另一项针对新诊断中高危患者的研究也显示出76%的临床恶化风险降幅。
肺动脉高压是一种罕见、进展迅速的严重疾病,传统靶向疗法通常需要患者每日服药。索特西普作为一种皮下注射剂型,为治疗模式带来了重要改变。其用药频率为每三周一次,且在后续治疗中符合条件的患者可学习自行注射,这有望在提供新治疗选择的同时,显著提升用药便利性,减轻患者长期治疗负担。
参考来源:
[1] 企业官微
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 头颈癌一线免疫治疗!默沙东Keytruda(可瑞达)2种方案获欧盟批准,治疗PD-L1阳性患者
3. 默沙东中国区业绩强劲,PD-1药物Keytruda全球热卖,上半年销售额破140亿美元
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论