
11月14日,据NMPA官网显示,罗氏制药的PD-L1单抗 阿替利珠单抗皮下注射剂 在国内获批上市。据摩熵医药数据库显示,这是首个在国内获批的进口 PD-(L)1 皮下注射剂。

截图来源:NMPA官网
阿替利珠单抗是一种靶向 PD-L1 的单克隆抗体,自2016年在美国获批以来,该药已经获批超过 10 个适应症,覆盖非小细胞肺癌、小细胞肺癌、肝癌、乳腺癌、尿路上皮癌、黑色素瘤等癌种。作为 PD-(L)1 免疫治疗时代的一大明星药,在 2024 年其全球销售额就已经达到 44.17亿美元。
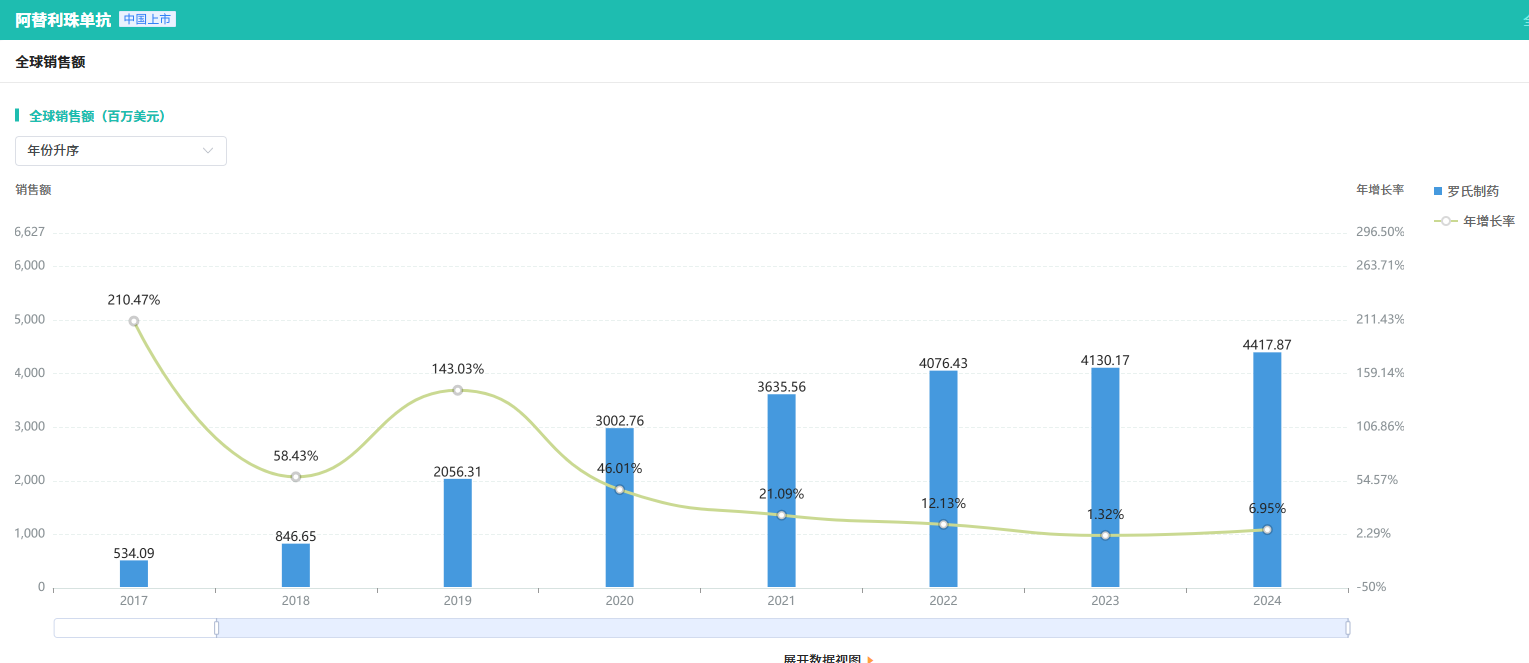
截图来源:摩熵医药全球药物研发数据库
阿替利珠单抗皮下注射剂(阿替利珠单抗 SC)最早于 2024 年 9 月在英国实现全球首批,目前也已经在欧盟、加拿大、美国都获批上市。而国内上市申请则在 2024 年 7 月 27 日获受理,今日成功在国内获批上市。
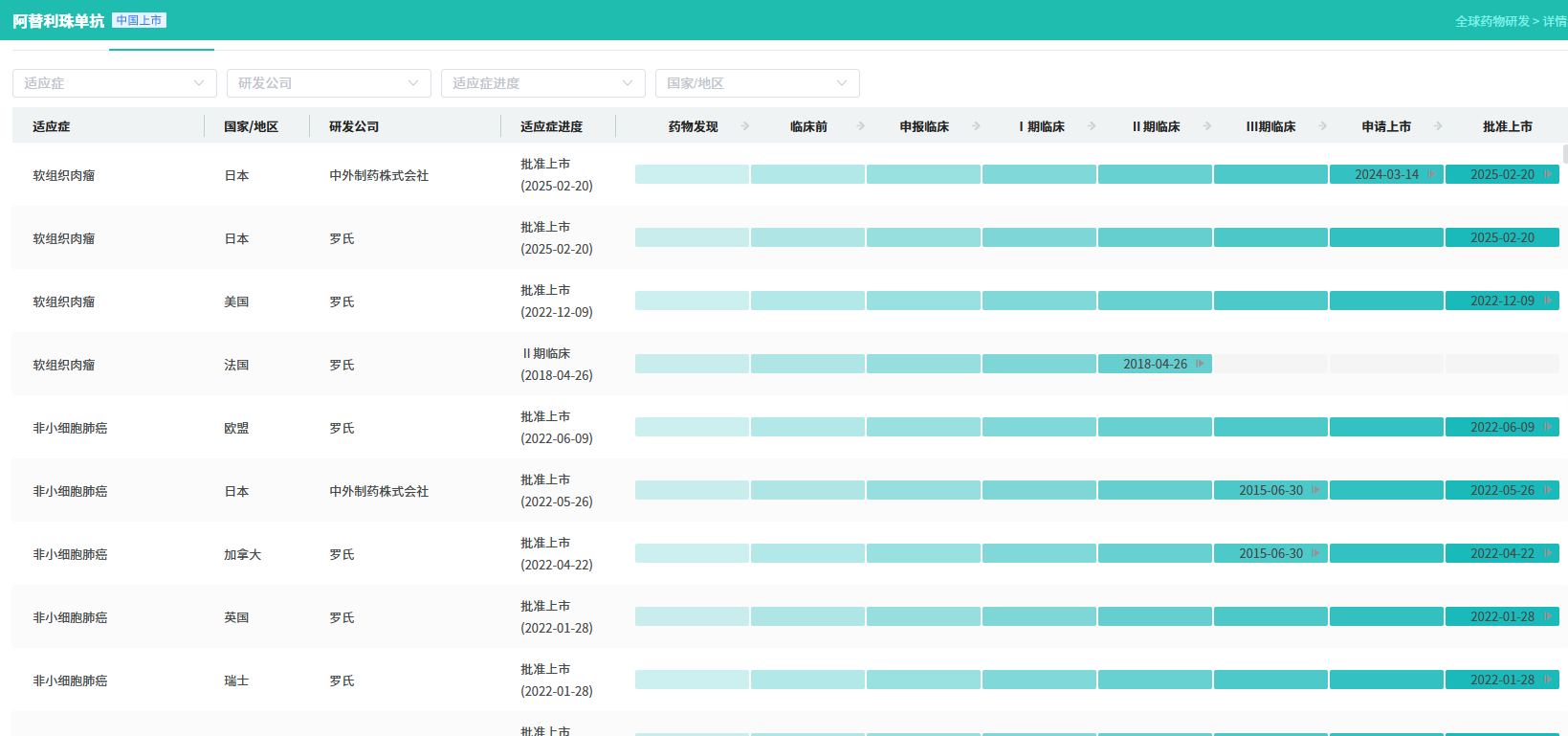
截图来源:摩熵医药全球药物研发数据库
罗氏将 阿替利珠单抗 与 Halozyme Therapeutics的Enhanze药物输送技术相结合,通过重组人透明质酸酶 PH20 (rHuPH20) 实现皮下制剂的开发。皮下制剂在依从性上有着巨大优势,可将注射时间从静脉注射的 30 - 60 分钟降低至 7 分钟,在疗效相似的情况下改善患者的用药体验、提高患者的用药满意度。
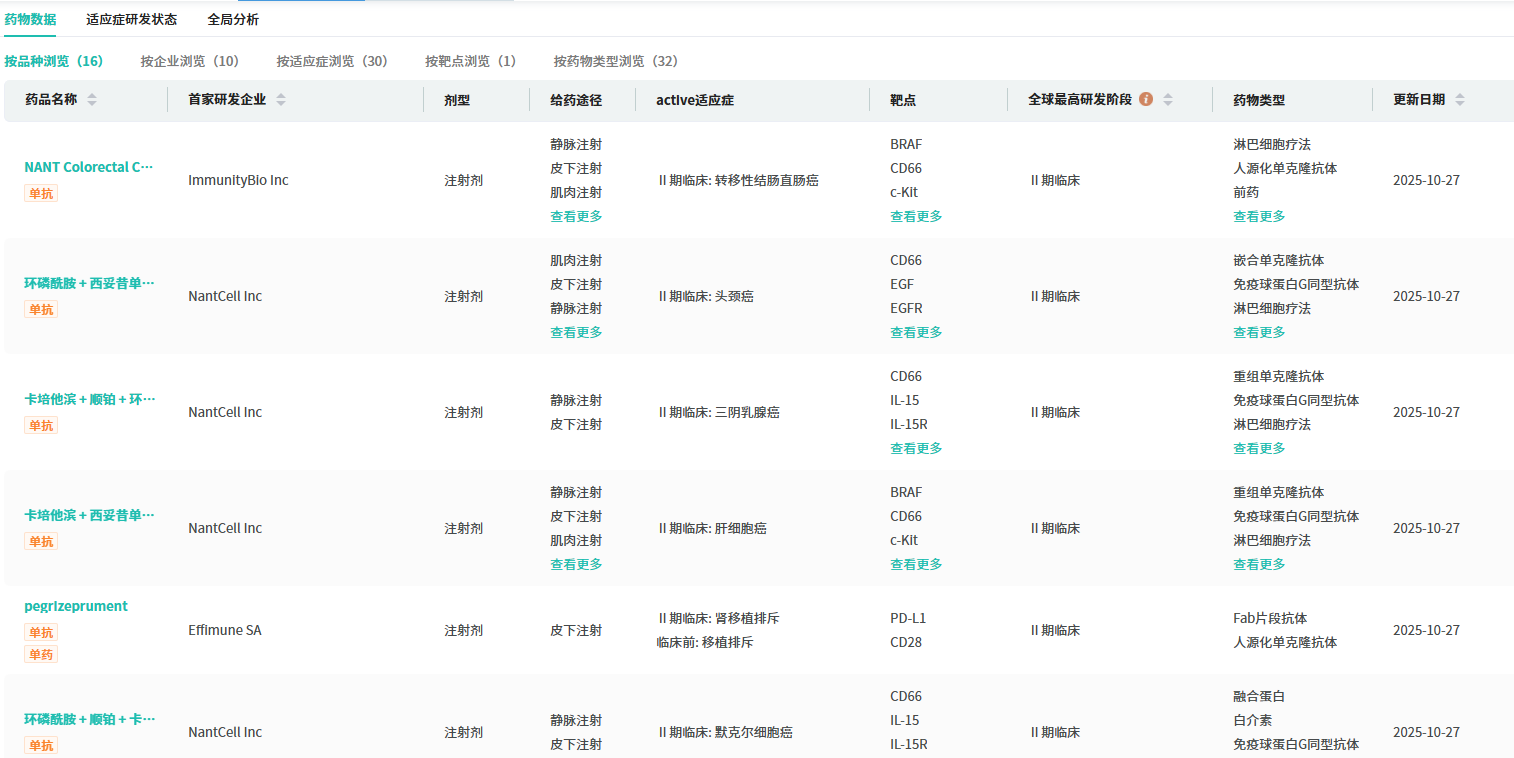
截图来源:摩熵医药全球药物研发数据库
目前,十余款 PD(L)-1 皮下制剂处于临床开发阶段。从跨国药企(MNC)看,默沙东 K药、BMS O药已开发成皮下制剂,2024年末 - 2025年陆续在海外获批;辉瑞的 PD-1 皮下注射剂 Sasanlimab 公布针对非肌层浸润性膀胱癌的 III 期积极结果。
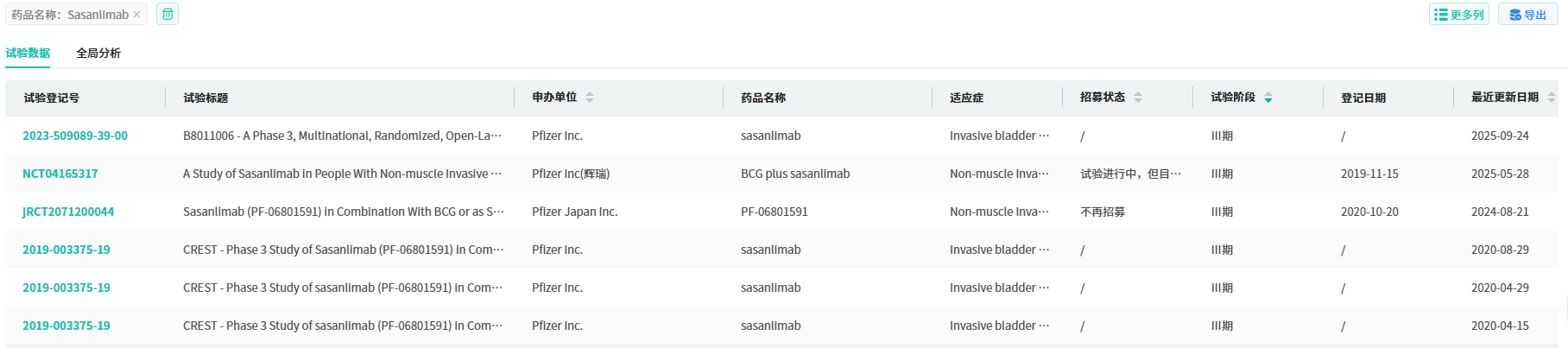
截图来源:摩熵医药全球临床试验数据库
国内,百济神州、君实生物、恒瑞医药等积极布局,将自家 PD-1 单抗开发成皮下注射剂,恒瑞还开发了 PD-L1 阿得贝利单抗皮下注射剂。罗氏布局早且成熟,与 Halozyme 合作,肿瘤领域有9个皮下注射抗体药项目在开发,7款已上市。
参考来源:
[1] NMPA官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 罗氏ALK抑制剂盐酸阿来替尼胶囊在华获批新适应症,治疗非小细胞肺癌!
2. 罗氏:TIGIT单抗治疗NSCLC II/III期研究失败!
3. 罗氏mosunetuzumab获FDA突破性药物资格 治疗滤泡性淋巴瘤
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论