
10月28日,国家卫健委药物政策与基本药物制度司正式发布《关于第四批鼓励仿制药品建议目录的公示》,为仿制药行业送来重大利好,公示期为5个工作日。
截图来源:国家卫生健康委员会官网
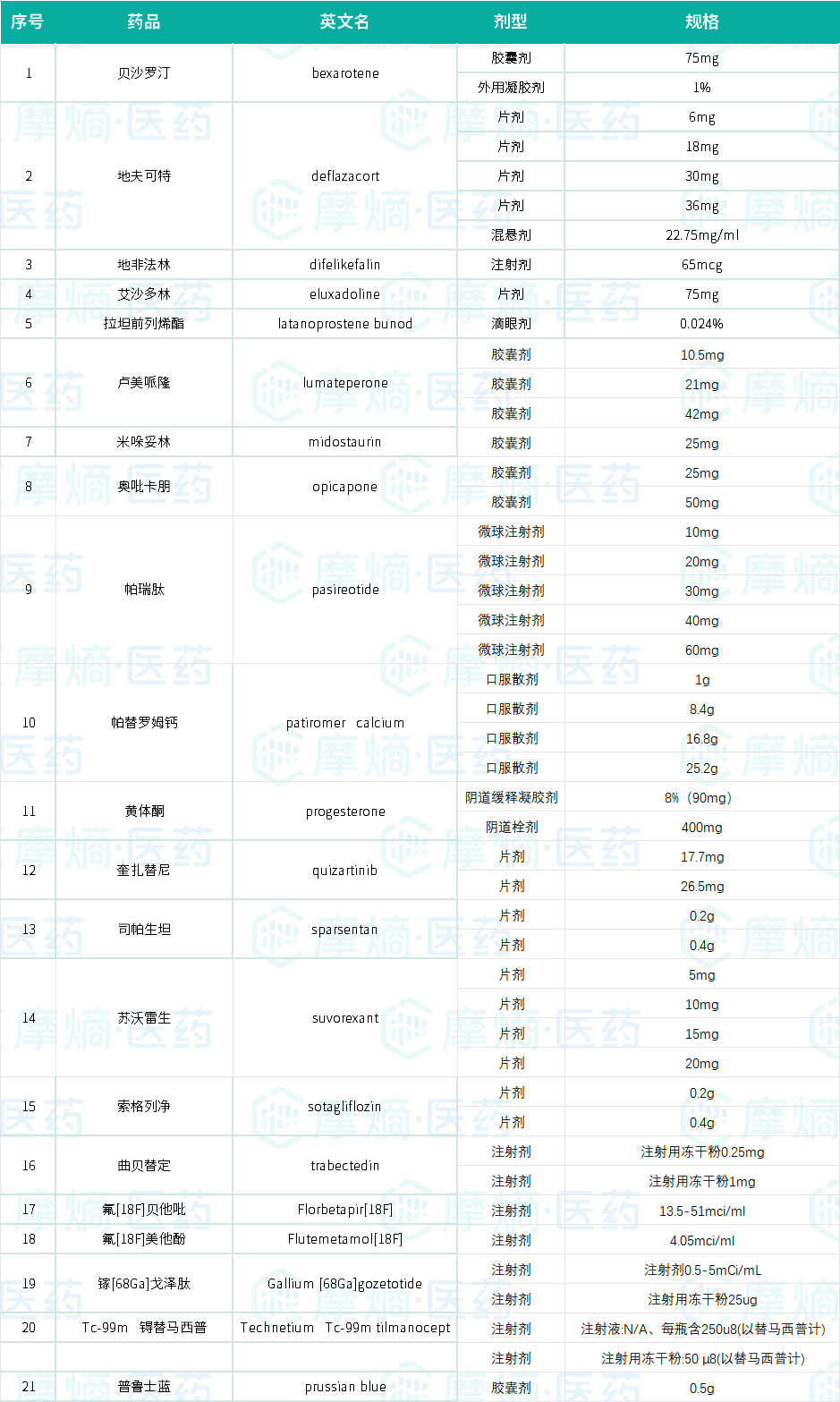
21款“明星药品”入选目录,涉及强生、默沙东等药企
在本次公示的《第四批鼓励仿制药品建议目录》中,入围的21个药品,其中多款兼具高临床价值、高技术壁垒和潜在市场价值的“明星药品”赫然在列。像强生的卢美哌隆,卫材的贝沙罗汀,默沙东的苏沃雷生等知名原研药,覆盖内分泌、肿瘤、神经、呼吸等多个治疗领域,为相关企业提供了明确的仿制方向。
卢美哌隆是一种多靶点作用的新型抗精神病药,Pharma ONE药物研发大数据平台显示,其最初由百时美施贵宝公司(BMS)研制,2005年独家授权给Intra-Cellular公司,2019年由美国FDA批准用于治疗成人精神分裂症,2021年批准用于成人I型或II型相关的抑郁发作治疗。
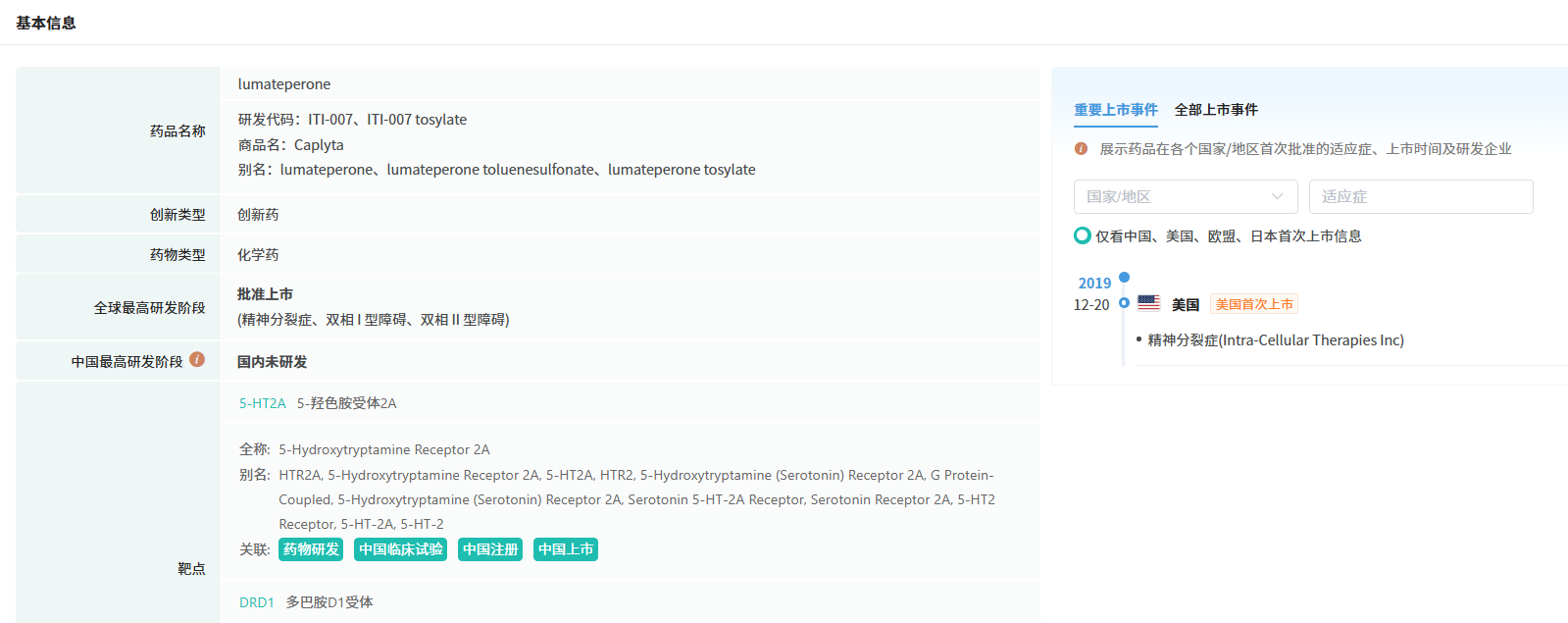
截图来源:摩熵医药全球药物研发数据库
据摩熵医药数据库显示,贝沙罗汀作为新型合成维甲酸类似物,获美国 FDA 批准用于皮肤 T 细胞淋巴瘤治疗。它能选择性结合 RXR 亚单位,发挥诱导肿瘤细胞死亡等作用,且分子量小、脂溶高、易透过血脑屏障。此次目录建议仿制其胶囊与外用凝胶剂,兼顾全身与局部治疗需求。原研药价高,纳入鼓励目录,意在引导企业攻克工艺,为国内患者提供可负担治疗。
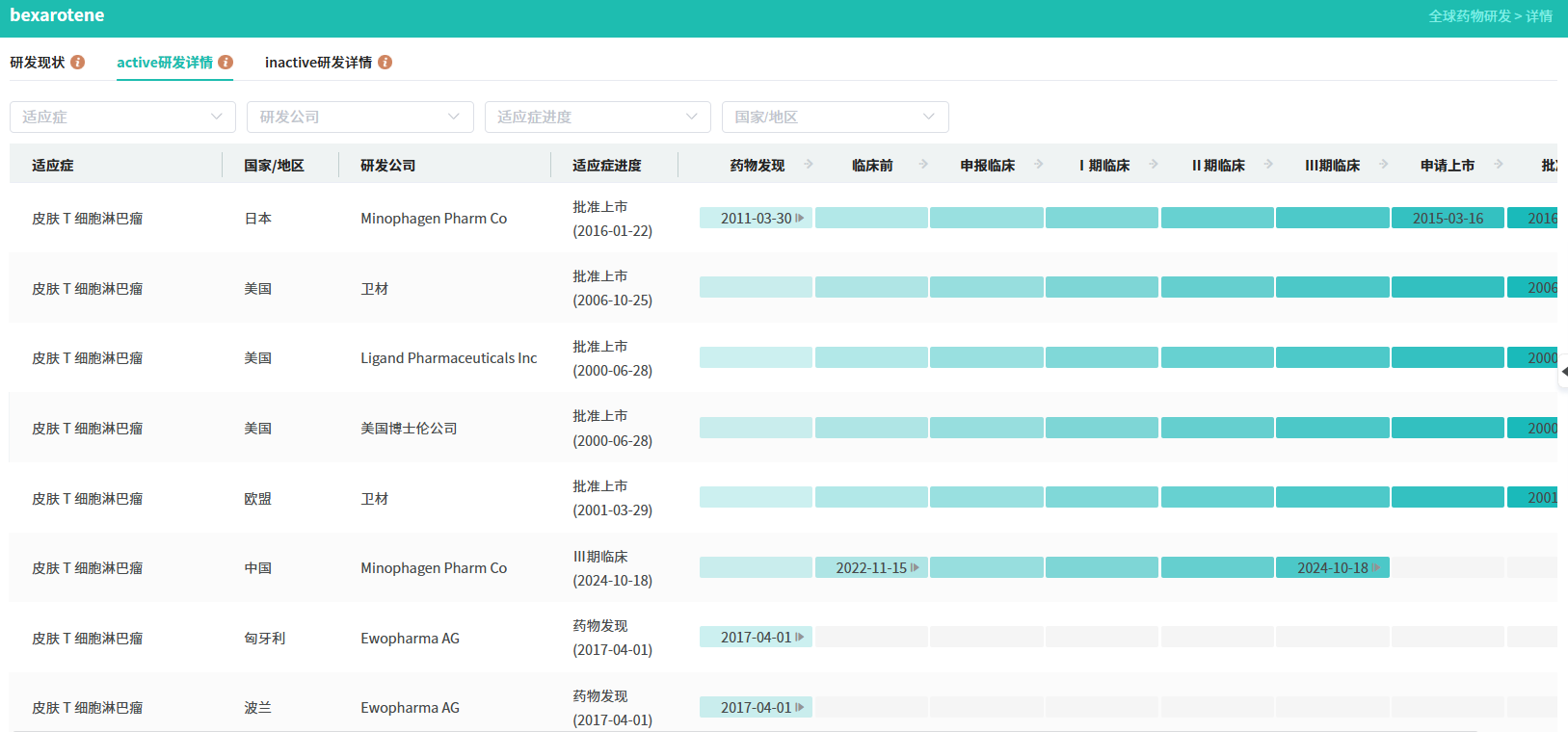
截图来源:摩熵医药全球药物研发数据库
此次21款药品纳入鼓励目录,是国家鼓励国内药企突破技术,实现高端复杂注射剂国产化。第四批目录秉持“以临床需求为导向、兼顾企业研发可行性”原则,聚焦临床必需且疗效确切的重大疾病防治及短缺药品,同时考量国内研发、工艺、原料药供应等实际,保障目录科学可行。作为药品供应保障体系的重要组成部分,仿制药在填补临床用药空白、提高药品可及性、降低医疗支出等方面发挥着不可替代的作用。
三批鼓励仿制药物目录,89个品种入选
鼓励仿制药品目录内的药品享有诸多政策支持,可按程序优先申报纳入国家医保目录。此前,国家已公布3批鼓励仿制药物目录,共纳入89个品种。其中,第一批目录有33个品种,第二批17个品种,第三批目录有39个品种。
从前两批目录的实施情况来看,政策效果显著。已有14个药品通过优先审评审批程序获得上市许可,12个品种成功通过谈判进入国家医保目录,其中不乏罕见病用药以及治疗地中海贫血、乳腺癌等重大疾病的药品。
此次第四批鼓励仿制药品目录推出,将推动我国仿制药行业迈向高质量发展。“健康中国 2030”下,药品政策聚焦保障可及、激励创新、提升规范,鼓励仿制与创新相辅相成,仿制可满足用药需求、释放医保空间,还能为创新研发打基础。
结语
当前,我国仿制药行业深度洗牌,通过一致性评价的占比提升、市场向头部集中,新目录将加速企业转型,提升行业竞争力。展望未来,鼓励仿制药品目录的动态更新将成为常态。对于企业而言,应紧跟政策导向,聚焦目录内高价值品种,加大研发投入,提升生产工艺水平,以高质量的仿制药满足临床需求。
参考来源:
[1] 国家卫生健康委员会官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
3. 2025医保目录调整启动:首设商保创新药目录,CAR-T等高价药迎新支付路径
想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论