
10月24日,CDE 官网显示,康方生物 AK112 注射液(依沃西单抗)又一项申请拟纳入突破性治疗,适应症为依沃西单抗联合化疗一线治疗局部晚期不可切除或转移性三阴性乳腺癌。
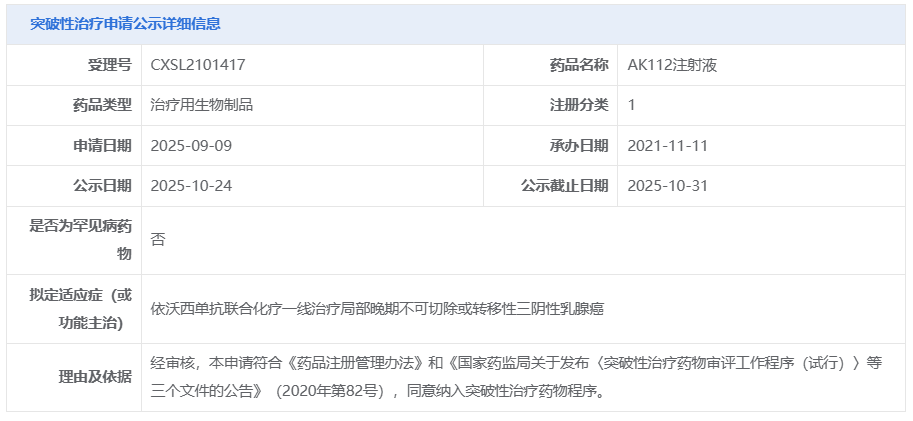
依沃西单抗是康方生物自主研发的、全球首创 PD-1/VEGF 双特异性肿瘤免疫治疗药物。此前,该药已有三项申请被 CDE 纳入突破性治疗品种,适应症分别为:
- 一线治疗 PD-L1 表达阳性(TPS≥1%)的局部晚期或转移性非小细胞肺癌(NSCLC)
- 联合化疗治疗经 EGFR-TKI 治疗失败的 EGFR 突变的局部晚期或转移性非鳞 NSCLC
- 联合多西他赛治疗既往 PD-1/L1 抑制剂和含铂化疗治疗失败的局部晚期或转移性 NSCLC
目前,康方正在国内开展一项随机、对照、多中心 III 期临床研究(CTR20250033),以评估依沃西联合注射用紫杉醇 (白蛋白结合型) 对比安慰剂联合注射用紫杉醇 (白蛋白结合型) 一线治疗 PD-L1 阴性的局部晚期不可切除或转移性三阴性乳腺癌的效果和安全性。
依沃西单抗已在国内获批两项适应症,分别为:
- 联合培美曲塞和卡铂用于经 EGFR-TKI 治疗进展的 EGFR 基因突变阳性的局部晚期或转移性非鳞状 NSCLC 患者的治疗;
- 单药用于 PD-L1 阳性的 EGFR 基因突变阴性和 ALK 阴性的局部晚期或转移性 NSCLC 的一线治疗。
今年 7 月,依沃西单抗的第三个适应症上市申请获得 NMPA 受理,联合化疗一线治疗晚期鳞状 NSCLC。
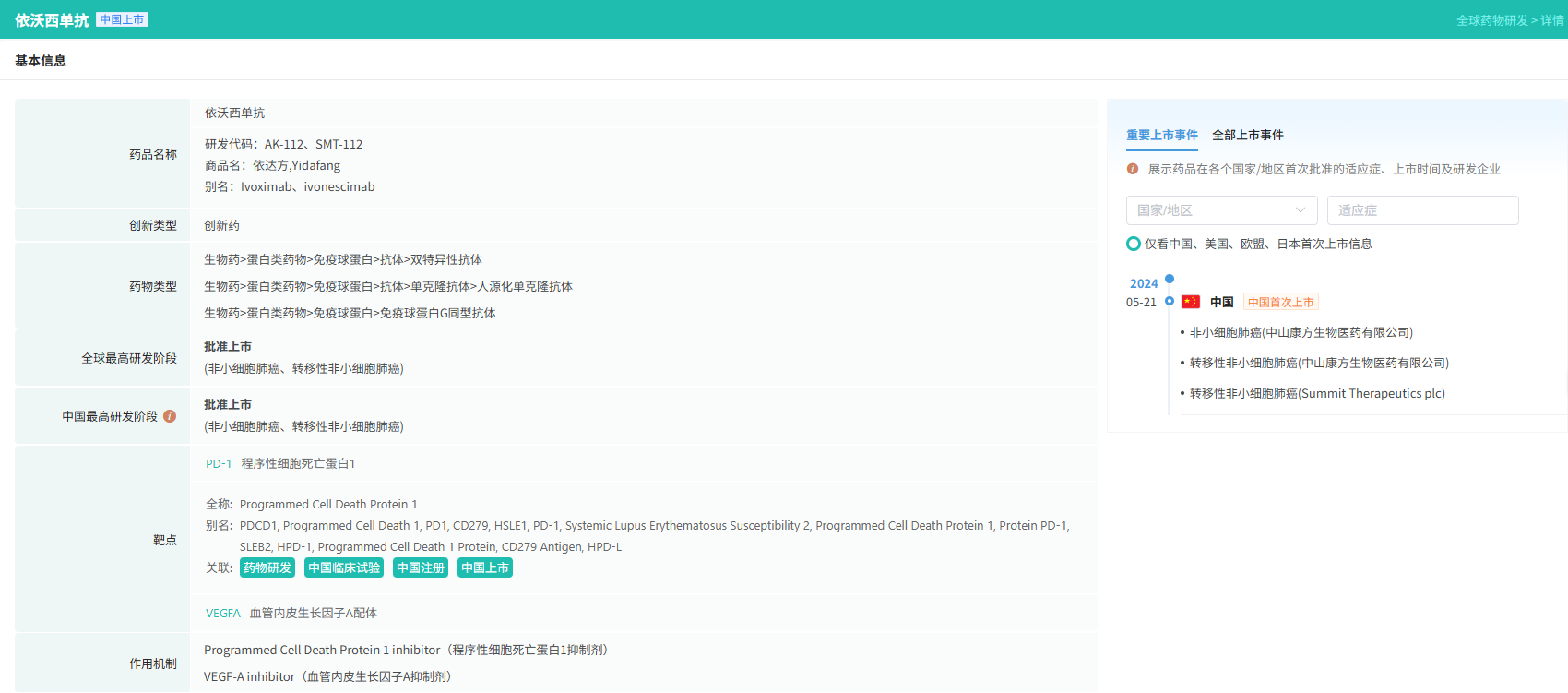
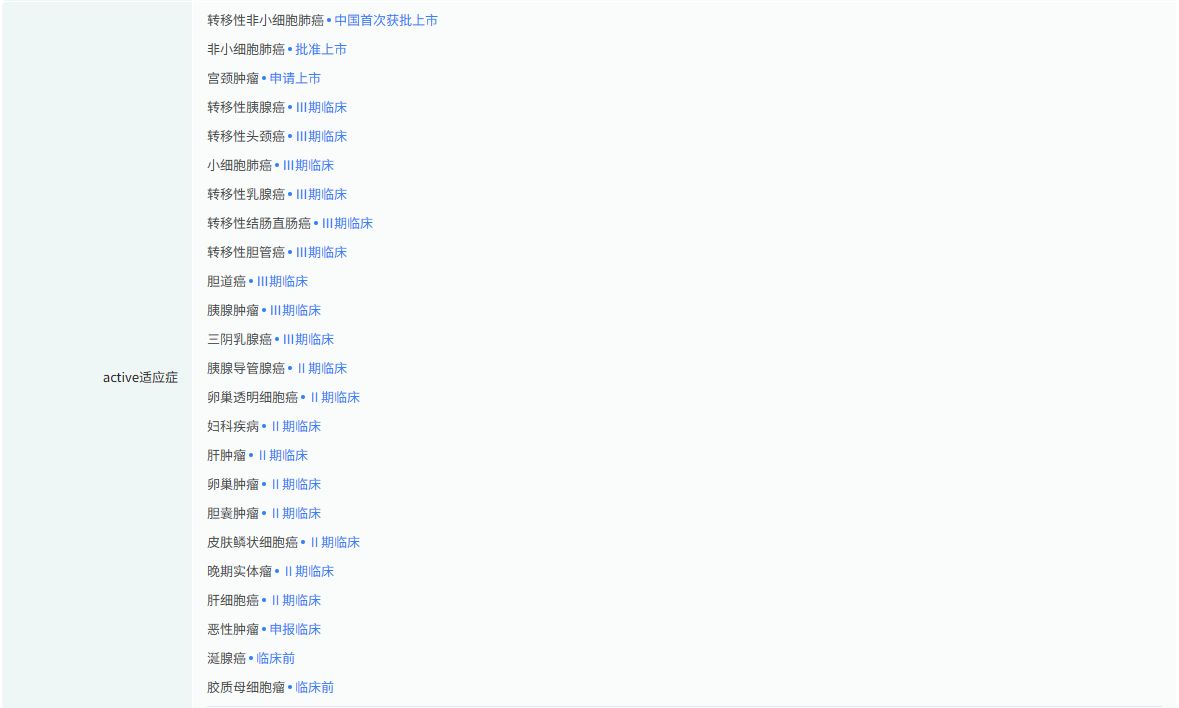
截图来源:摩熵医药数据库-全球药物研发数据库
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 2024年10月:122款新药获批临床!66款纳入突破性治疗,涉及阿斯利康、中山康方等
2. 康方生物&正大天晴:派安普利单抗联合安罗替尼肝癌治疗上市申请获受理
3. 2024年有望获批的18款国产新药,涉及恒瑞、康方生物....
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论