1.4.1 本周全球TOP10创新药研发进展
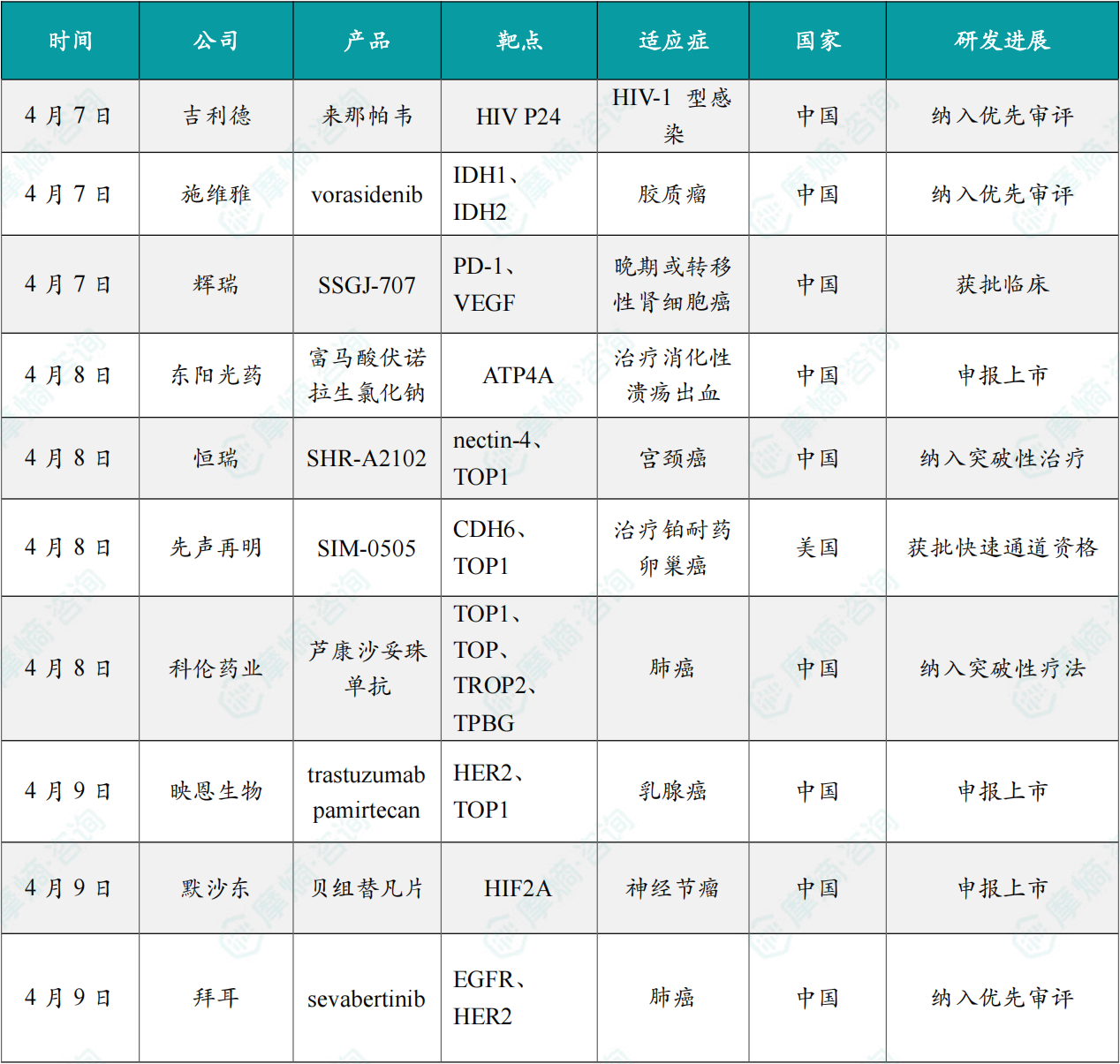
(1)吉利德长效HIV预防新药在华拟纳入优先审评
4月7日,CDE 官网显示,吉利德「来那帕韦钠片」和「来那帕韦钠注射液」新适应症拟纳入优先审评,适用于与安全的性行为相结合,对于感染风险较高的成人和青少年(体重至少在35kg以上)进行暴露前预防,以降低通过性行为感染HIV-1的风险。其中来那帕韦钠片为来那帕韦钠注射液的注射前口服导入用药,并用于在两次来那帕韦钠注射给药之间需要时进行口服桥接。
来那帕韦钠是一款全球首创的HIV-1衣壳抑制剂,因为采用缓释技术,来那帕韦钠注射液制剂可从注射部位缓慢释放,并维持有效浓度达26周,实现每半年一次的皮下给药。
此前,来那帕韦钠已在欧盟、美国、中国等国家和地区获批,联合其他抗逆转录病毒药物,用于治疗多重耐药HIV感染的成人患者。
(2)施维雅的First in class新药拟纳入优先审评
4月7日,CDE官网显示,施维雅的Vorasidenib片拟纳入优先审评,用于携带异柠檬酸脱氢酶-1(IDH1)或异柠檬酸脱氢酶-2(IDH2)突变的 级星形细胞瘤或少突胶质细胞瘤成人和12岁及以上儿童患者的手术(包括活检、次全切除或全切除)后治疗。
Vorasidenib是施维雅在 2020 年通过收购Agios公司所得的一款口服、选择性、高度脑渗透性的双重抑制剂,2024年8月,该药首次获得FDA批准上市,成为全球首个获批上市的IDH1/2双靶点抑制剂,也是近20年来IDH突变型弥漫性脑胶质瘤治疗领域首个创新靶点药物。
(3)辉瑞重金引进的PD-1/VEGF双抗国内获批临床
4月7日,CDE官网显示,辉瑞申报的1类新药PF-08634404多项适应症获批临床,包括:1)联合化疗用于既往未接受过治疗的转化型小细胞肺癌的一线治疗;2)单药或联合治疗既往未接受治疗的局部晚期或转移性肾细胞癌。
PF-08634404(三生制药研发代号:SSGJ-707)是三生制药开发的一款PD-1/VEGF双抗,2025年5月,辉瑞以超60亿美元引进该产品全球开发与商业化权利,其中包括14亿美元首付款及1亿美元股权合作,一举刷新中国创新药单笔出海授权交易的首付款纪录。
依托于辉瑞的临床资源,PF-08634404的临床进度正在高效推进中,已经开展3项III期临床试验,适应症包括结直肠癌、非小细胞肺癌,而计划开展的III期临床适应症还包括子宫内膜癌、尿路上皮癌等。
(4)东阳光药改良型新药伏诺拉生申报上市
4月8日,东阳光药发布公告称,其改良型新药富马酸伏诺拉生氯化钠注射液的上市许可申请获得中国NMPA受理(受理号:CXHS2600048),申报适应症为:用于治疗消化性溃疡出血。
伏诺拉生(Vonoprazan)是一种新型钾离子竞争性酸阻滞剂 (P-CAB),主要用于治疗胃酸相关疾病,它通过抑制胃酸的分泌来发挥作用。东阳光药开发的富马酸伏诺拉生氯化钠注射液是基于已经上市的富马酸伏诺拉生片进行改良,属于 2 类新药。
(5)恒瑞Nectin-4 ADC拟纳入突破性治疗
4月8日,CDE 官网公示,恒瑞SHR-A2102的一项申请拟纳入突破性治疗品种,适应症为:治疗含铂化疗及PD-(L)1抑制剂治疗失败的复发或转移性宫颈癌。
SHR-A2102是恒瑞医药自主研发的一款靶向 Nectin-4的抗体偶联药物(ADC),其有效载荷是拓扑异构酶抑制剂(TOP1i)。
2024年12月,HR-A2102单药治疗既往含铂化疗和PD-(L)1抑制剂治疗失败的局部晚期或转移性尿路上皮癌的申请已被CDE纳入突破性治疗品种。美国FDA已授予HR-A2102治疗晚期尿路上皮癌适应症的快速通道资格。除了尿路上皮癌、宫颈癌,恒瑞还在探索SHR-A2102治疗非小细胞肺癌、头颈部鳞状细胞癌、食管癌、乳腺癌等适应症的效果。
(6)先声再明ADC疗法获FDA快速通道资格,治疗卵巢癌
4月8日,先声再明宣布,靶向CDH6的抗体偶联药物(ADC)在研新药SIM0505,获得美国FDA授予的快速通道资格,用于治疗铂耐药卵巢癌。
SIM0505是由先声再明研发的一款靶向CDH6(Cadherin-6,钙粘蛋白-6)的新型ADC,搭载了专有的拓扑异构酶1抑制剂(TOPOi)有效载荷。该药物设计旨在达到广泛的抗肿瘤活性、快速的全身清除率以及更佳的潜在治疗窗口。
2025年6月,先声再明与NextCure公司建立战略合作,后者获得了SIM0505在中国以外的全球独家权益。此后,双方在中美两地协同,快速推进SIM0505用于治疗包括卵巢癌在内的晚期实体瘤的1期临床研究。
(7)芦康沙妥珠单抗联合K药一线治疗NSCLC拟纳入突破性疗法
4月8日,CDE网站显示,芦康沙妥珠单抗(SKB264,sac-TMT)联合帕博利珠单抗(皮下注射)用于PD-L1 TPS≥1%的EGFR基因突变阴性和ALK阴性的局部晚期或转移性非小细胞肺癌(NSCLC)的一线治疗,拟纳入突破性疗法(BTD)。
此前,芦康沙妥珠单抗联合K药(静脉输注)一线治疗NSCLC已纳入BTD。而根据公开资料,K药皮下制剂可在1-2分钟内完成给药,相较于需30分钟给药的静脉输注制剂,极大节省了治疗时间。对于肿瘤负荷较重的晚期患者而言,这种给药方式的补充与升级将显著提高用药便利性与依从性。
(8)映恩生物首个创新药帕康曲妥珠单抗申报上市
4月9日,CDE官网显示,映恩生物的首个ADC药物——帕康曲妥珠单抗(DB-1303/BNT323)递交上市申请。这是映恩生物首个申报上市的创新药。
2025年9月,帕康曲妥珠单抗对比T-DM1治疗既往接受曲妥珠单抗和紫杉烷类治疗的HER2阳性不可切除或转移性乳腺癌患者的III期临床试验(DYNASTY Breast02)达到主要研究终点,即无进展生存期(PFS)显著延长。
帕康曲妥珠单抗是一款处于临床阶段的HER2 ADC候选药物,采用稳定的、可裂解连接符及专有的基于拓扑异构酶抑制剂的有效载荷设计,旨在降低脱靶毒性及增强抗肿瘤活性,包括旁观者杀伤效应。
(9)默沙东小分子新药「贝组替凡片」新适应症国内报上市
4月9日,CDE官网显示,默沙东贝组替凡片新适应症上市申请获受理,推测用于局部晚期、不可切除或转移性嗜铬细胞瘤或副神经节瘤(PPGL)成人和12岁及以上青少年患者。
此前2025年12月,该适应症已获CDE优先审评资格。2025年10月,默沙东在ESMO大会上公布了贝组替凡治疗晚期嗜铬细胞瘤和副神经节瘤的II期LITESPARK-015研究数据。截至2024年5月23日,共入组72例患者,中位年龄51.5岁,中位既往治疗次数为1次(范围:0-5)。结果显示,中位随访23.6个月时,ORR为26%,DCR为85%。中位DOR、中位PFS 和中位OS 分别为20.4 个月、22.3个月和NR。
(10)拜耳first in class肺癌新药拟纳入优先审评
4月9日,CDE官网显示,拜耳的first in class肺癌新药塞伐艾替尼(sevabertinib,BAY 2927088)拟纳入优先审评,用于一线治疗携带HER2(ERBB2)激活突变的晚期非小细胞肺癌(NSCLC)成人患者。
此前,塞伐艾替尼已于2025年7月在中国申报上市,用于治疗携带HER2(ERBB2)激活突变且既往接受过一种系统治疗的晚期NSCLC成人患者。
塞伐艾替尼是拜耳开发的一款口服非共价可逆选择性酪氨酸激酶抑制剂,对携带EGFR和HER2突变(包括HER2 exon 20插入突变)的肿瘤有抑制活性。2025年11月19日,塞伐艾替尼在美国获批上市。
1.4.2 本周全球TOP10积极/失败临床结果
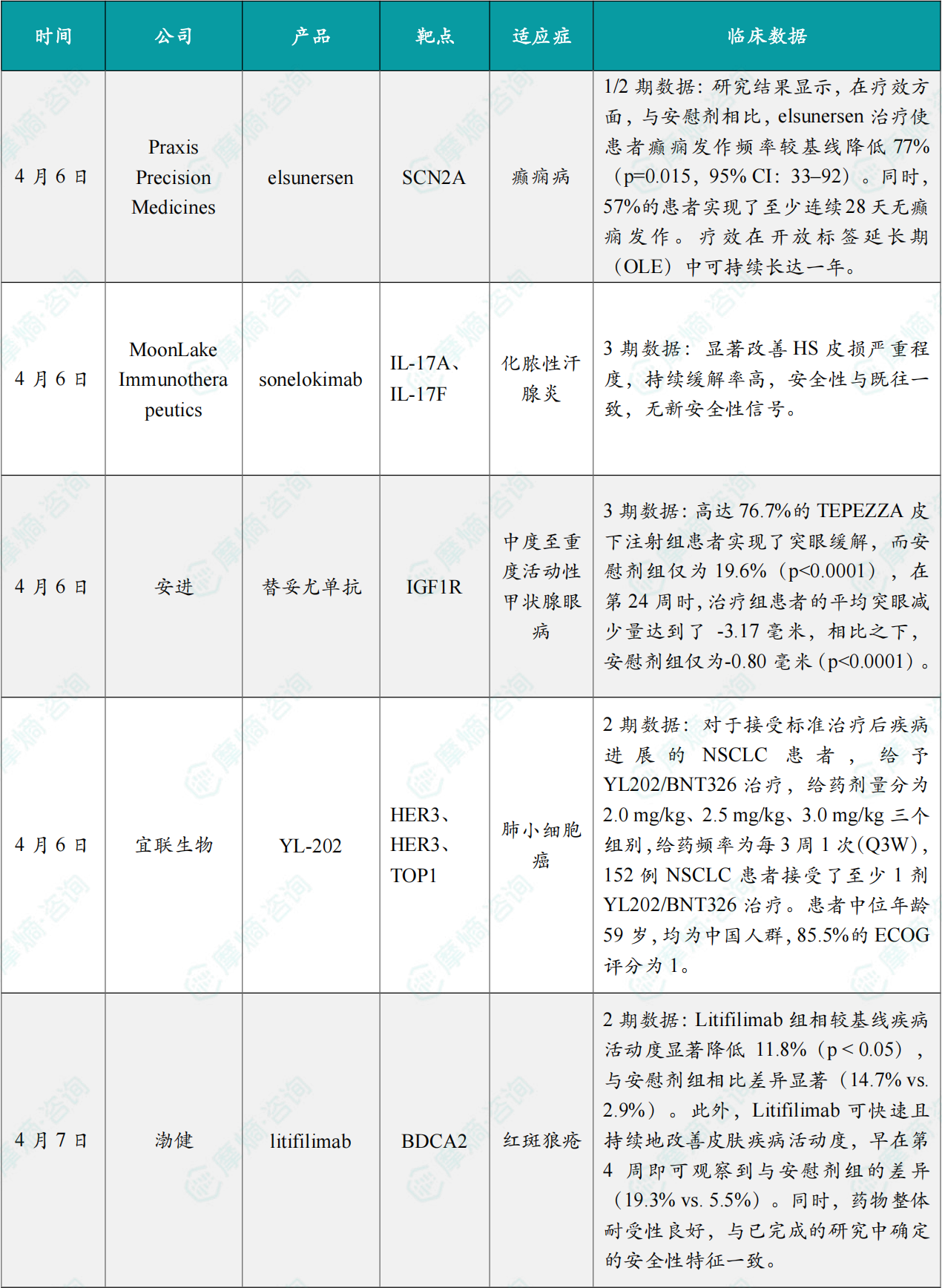
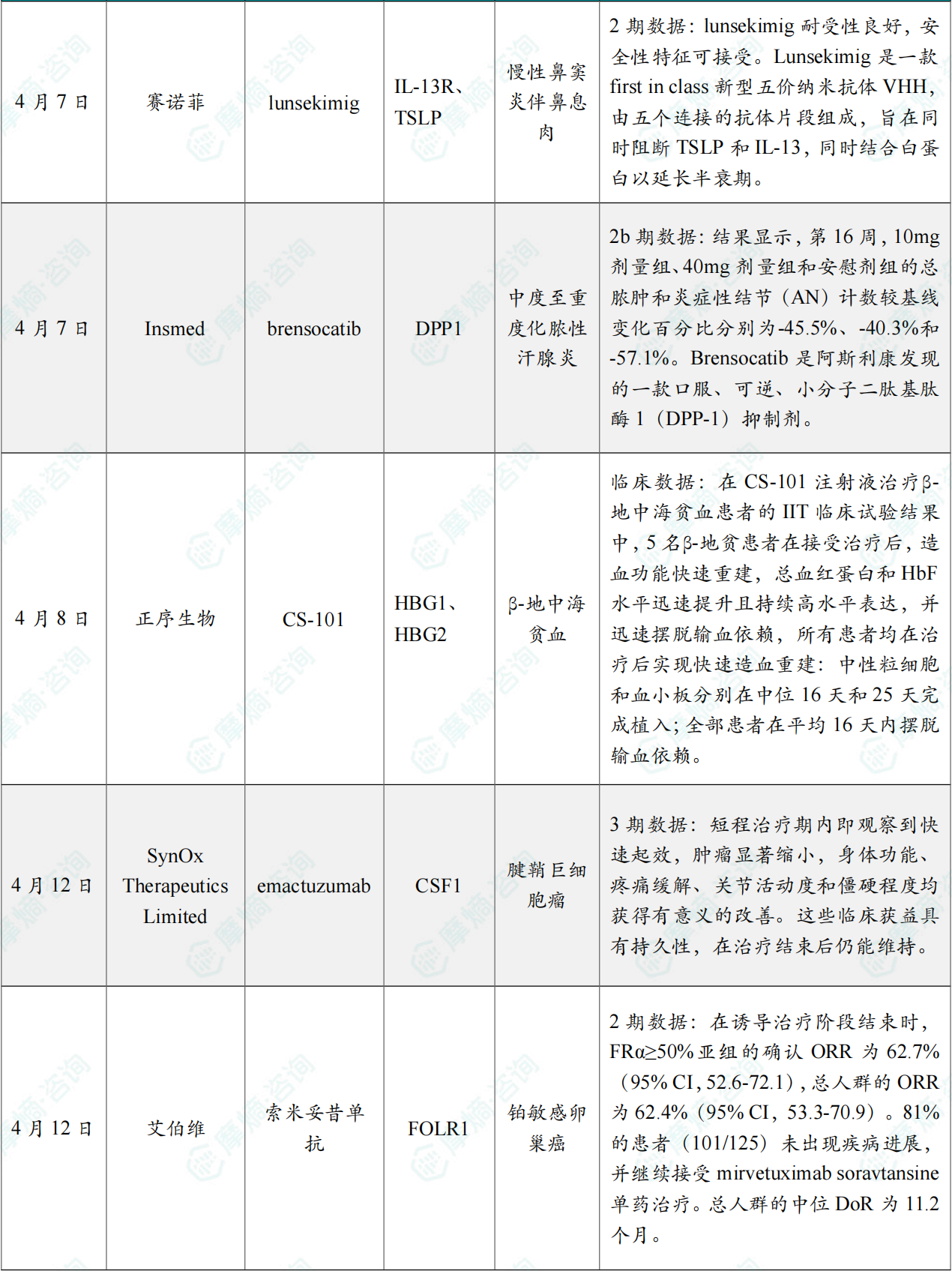
(1)Praxis Precision Medicines宣布在研疗法elsunersen在1/2期试验中取得积极结果
4月6日,Praxis Precision Medicines宣布,其在研疗法elsunersen在EMBRAVE临床1/2期试验A部分中取得积极结果。该研究在早发性癫痫型SCN2A发育性与癫痫性脑病(SCN2A-DEE)儿童患者中开展。
Elsunersen是一种反义寡核苷酸(ASO)疗法,旨在选择性降低SCN2A基因表达,从而直接靶向早发性癫痫型SCN2A-DEE的致病机制,用于治疗携带SCN2A功能获得性突变患者的癫痫发作及其他相关症状。
研究结果显示,在疗效方面,与安慰剂相比,elsunersen治疗使患者癫痫发作频率较基线降低77%(p=0.015,95% CI:33–92)。同时,57%的患者实现了至少连续28天无癫痫发作。疗效在开放标签延长期(OLE)中可持续长达一年。
(2)MoonLake Immunotherapeutics公布Ⅲ期研究积极结果疗
4月6日,Sonelokimab是一种同时抑制IL-17A和IL-17F的双特异性纳米抗体,截至第40周的评估采用“按观察到的数据”分析,包括HiSCR50/75/90/100、皮肤疼痛(较基线改善≥3分)和HiSQOL(平均降幅)。
数据为初步结果,在数据库锁定后可能发生变化。在VELA-1和VELA-2研究中,分别有283名和276名患者被分配至持续Sonelokimab组,138名和141名患者分配至安慰剂转换组。至第40周,持续接受Sonelokimab治疗的患者展现出深度的、持续的疗效:HiSCR50、HiSCR75、HiSCR90和HiSCR100的应答率分别维持在≥75%、≥60%、≥35%和≥25%的高水平;皮肤疼痛改善≥3分应答率≥35%;HiSQoL评分较基线(VELA-1: 26.5分;VELA-2: 28.0分)平均改善≥11分。两项研究的结果高度一致。对于在第16周从安慰剂转换为Sonelokimab治疗的患者,在换药后迅速出现改善。HiSCR75应答率最高增加22%,疼痛应答率最高增加19%,HiSQOL评分最高降低7.7分。
(3)安进宣布注射治疗甲状腺眼病3期临床取得积极结果
4月6日,安进宣布其重磅药物TEPEZZA通过贴敷式注射器进行皮下注射,治疗中度至重度活动性甲状腺眼病(TED)成人患者的3期临床试验获得了积极的顶线结果,为患者带来更加便捷、且疗效媲美静脉输注(IV)的全新给药选择。
高达76.7%的TEPEZZA皮下注射组患者实现了突眼缓解,而安慰剂组仅为19.6%(p<0.0001)。在第24周时,治疗组患者的平均突眼减少量达到了 -3.17毫米,相比之下,安慰剂组仅为-0.80毫米(p<0.0001)。超过3毫米的突眼减少对于患者而言具有极其重要的临床意义,能够显著改善患者的眼部外观和舒适度。
(4)苏州宜联生物医药有限公司公布靶向HER3 ADC YL202单药治疗NSCLC数据
4月6日,YL202/BNT326是一款在研HER3靶向ADC,由抗HER3抗体通过三肽连接子,与药物抗体比(DAR)为8的新型拓扑异构酶I抑制剂载荷偶联而成。152例NSCLC患者接受了至少1剂YL202/BNT326治疗。患者中位年龄59岁,均为中国人群,85.5%的ECOG评分为1。疗效分析分别纳入EGFR突变型NSCLC患者(n=96)、AGA阴性非鳞状NSCLC患者(n=27)及鳞状NSCLC患者(n=22)。中位随访7.8个月,ORR在EGFR突变型患者中为41.7%,AGA阴性非鳞状NSCLC患者中为48.1%,鳞状NSCLC患者中为22.7%。148例患者(97.4%)出现治疗相关不良事件(TRAE),64例(总体:42.1%,2 mg/kg组:30.6%,3 mg/kg组:55.8%)发生≥3级不良事件,8例患者(5.3%)因TRAE停止治疗,1例2 mg/kg剂量组患者因肺炎死亡。常见的TRAE为贫血(67.8%)、恶心(44.7%)和食欲下降(43.4%)。≥3级TRAE主要包括淋巴细胞计数减少(13.2%)、贫血(10.5%)、中性粒细胞计数减少(8.6%)和白细胞计数减少(7.9%)。
(5)渤健BDCA2单抗II期再获成功
4月7日,在刚刚结束的AAD Annual Meeting(美国皮肤病学会年会)上,渤健(Biogen)公司宣布其全球首创的BDCA2单抗Litifilimab,在针对皮肤型红斑狼疮(CLE)的第二项II期临床试验AMETHYST取得积极结果。该药物有望成为70年来针对该疾病的首个靶向疗法。
具体来看,Litifilimab在第16周时,达到皮肤红斑狼疮活动度评分(CLA-IGA-R)0-1 分(完全清除/几乎清除)的患者中,Litifilimab组相较基线疾病活动度显著降低 11.8%(p < 0.05),与安慰剂组相比差异显著(14.7% vs. 2.9%)。此外,Litifilimab可快速且持续地改善皮肤疾病活动度,早在第 4 周即可观察到与安慰剂组的差异(19.3% vs. 5.5%)。同时,药物整体耐受性良好,与已完成的研究中确定的安全性特征一致。
(6)赛诺菲first in class双抗两项II期临床告捷
4月7日,赛诺菲宣布TSLP/IL-13双抗lunsekimig在两种慢性呼吸系统疾病中进行的II期研究均达到了主要终点和关键次要终点。在两项研究中,lunsekimig耐受性良好,安全性特征可接受。
Lunsekimig是一款first in class新型五价纳米抗体VHH,由五个连接的抗体片段组成,旨在同时阻断TSLP和IL-13,同时结合白蛋白以延长半衰期。AIRCULES是一项随机、双盲、安慰剂对照的IIb期临床研究,旨在评估皮下注射lunsekimig联合标准治疗在中重度哮喘成人患者中的疗效、安全性和耐受性。
结果显示,lunsekimig达到了主要终点和关键次要终点,显示出哮喘急性加重率的统计学显著性和临床意义的降低,以及肺功能的改善。DUET是一项随机、双盲、安慰剂对照的IIa期研究,旨在评估皮下注射lunsekimig在慢性鼻窦炎伴鼻息肉(CRSwNP)成人患者中的疗效、安全性和耐受性。该研究同样达到了主要终点,即鼻息肉评分自基线的变化,以及关键次要终点,患者报告的鼻塞/阻塞评分变化和Lund-Mackay计算机断层扫描(LMK-CT)评分变化。
(7)Insmed宣布Brenocatib治疗中度至重度化脓性汗腺炎的IIb期研究未达到主要终点
4月7日,Insmed宣布Brenocatib治疗中度至重度化脓性汗腺炎(HS)的IIb期CEDAR研究未达到主要终点和次要终点。基于此结果,Insmed将放弃开发HS适应症。
CEDAR研究是一项随机、双盲、安慰剂对照IIb期临床试验(n=214),旨在评估Brenocatib(10mg或40mg)在中度至重度HS成人患者中的疗效和安全性。结果显示,第16周,10mg剂量组、40mg剂量组和安慰剂组的总脓肿和炎症性结节(AN)计数较基线变化百分比分别为-45.5%、-40.3%和-57.1%。。
(8)正序生物发布碱基编辑药物CS-101临床结果发布
4月8日,正序生物在Nature报道了体外碱基编辑药物CS-101在β-地中海贫血患者中的临床应用结果。在CS-101注射液治疗β-地中海贫血患者的IIT临床试验结果中,5名β-地贫患者在接受治疗后,造血功能快速重建,总血红蛋白和HbF水平迅速提升且持续高水平表达,并迅速摆脱输血依赖。
该临床试验(IIT,NCT06024876)共纳入5例输血依赖型β-地中海贫血患者。所有患者均接受了1次动员和单采流程。临床结果显示,所有患者均在治疗后实现快速造血重建:中性粒细胞和血小板分别在中位16天和25天完成植入;全部患者在平均16天内摆脱输血依赖。治疗后,患者胎儿血红蛋白(HbF)及总血红蛋白水平显著升高并长期维持稳定,3个月时总血红蛋白达12.4 g/dL,15个月时进一步提升至13.4 g/dL。截至随访中位时间23个月,所有患者均持续无输血超过12个月,且未观察到脱靶编辑或与治疗相关的不良事件,显示出良好的安全性与持久性。
(9)SynOx Therapeutics Limited发布III期TANGENT研究的积极顶线结果
4月12日,SynOx Therapeutics Limited发布了其关键性III期TANGENT研究的积极顶线结果。这项全球多中心、随机双盲、安慰剂对照试验评估了Emactuzumab在成人腱鞘巨细胞瘤(TGCT)患者中的疗效与安全性,研究达到了主要终点和所有关键次要终点,且均显示出高度统计学显著性。
患者在短程治疗期内即观察到快速起效,肿瘤显著缩小,身体功能、疼痛缓解、关节活动度和僵硬程度均获得有意义的改善。这些临床获益具有持久性,在治疗结束后仍能维持。SynOx目前正在继续随访TANGENT研究中的患者,以进一步表征缓解持续时间,并评估再次治疗和交叉开放标签治疗的潜在作用。
(10)艾伯维公布Mirvetuximab Soravtansine治疗铂敏感卵巢癌的Ⅱ期临床数据
4月12日,艾伯维对外宣布叶酸受体α(FRα)的复发性铂敏感卵巢癌(PSOC)患者中的潜在疗效和安全性,在诱导治疗阶段结束时,FRα≥50%亚组的确认ORR为62.7%(95% CI,52.6-72.1),总人群的ORR为62.4%(95% CI,53.3-70.9)。81%的患者(101/125)未出现疾病进展,并继续接受mirvetuximab soravtansine单药治疗。总人群的中位DoR为11.2个月。在从联合治疗转为mirvetuximab soravtansine-gynx单药治疗的患者中,总人群的ORR为68%(59.1-76.1)。在近半数(49%)既往暴露于PARPi的总人群(FRα≥25%)患者中,ORR为63.9%(50.6-75.8)。
同期事件:
1. 2026年第15周04.06-04.12国内创新药/改良型新药申请临床/获批临床/申请上市/获批上市数据分析
2. 2026年第15周04.06-04.12国内仿制药/生物类似物申报/审批数据分析
3. 2026年第15周04.06-04.12国内医药大健康行业政策法规汇总
以上内容均来自{ 摩熵咨询医药行业观察周报(2026.04.06-2026.04.12) },如需查看或下载完整版报告,可点击!
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论