近日,药明康德子公司合全药业与生物医药高科技公司诺诚健华达成战略合作,携手加快诺诚健华肿瘤免疫领域的新药研发。根据协议,合全药业将成为诺诚健华首选CDMO合作伙伴,为诺诚健华在研及后续产品管线提供原料药研发及委托生产服务。
与此同时,今日(7月28日)诺诚健华宣布,公司旗下新型蛋白酪氨酸磷酸酶SHP2变构抑制剂ICP-189的新药研究(IND)申请,已获药监局受理,将成为诺诚健华第7个进入临床阶段的创新药。
凭借合全药业深耕CDMO领域20年的经验,诺诚健华的药物管线开发进程或将得到大幅提升。那么,诺诚健华的新药研发布局如何?核心产品竞争力如何?有哪些值得业界关注?
深度布局肿瘤&免疫诺诚健华12款创新药引人期待
自2013年成立以来,目前诺诚健华共有12款在研创新药,药物适应症主要集中在肿瘤及免疫疾病上。
12款在研新药中,除奥布替尼已上市外,其余药物均处于临床或临床前阶段。
表1 诺诚健华在研创新药
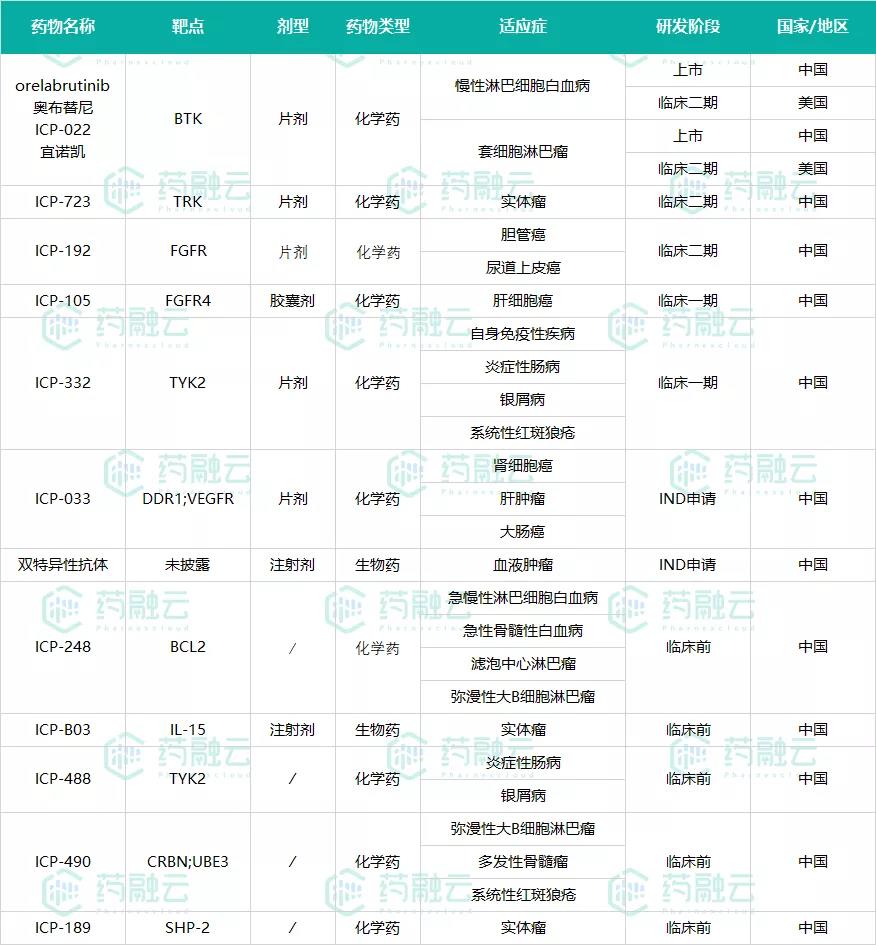
数据来源:药融云全球药物研发数据库
4款药物在临床,其中2款处国内第一梯队
ICP-723、ICP-192、ICP-105和ICP-332处于临床I/II期,分别针对TRK、FGFR、FGFR4和TYK2靶点。其中ICP-332片7月26日刚开展临床一期。
值得一提的是,ICP-192和ICP-105目前都处于国内第一梯队:
- 在国内范围,ICP-192是除erdafitinib以外,临床进展最快的泛FGFR抑制剂。
- 而在FGFR4抑制剂上,在国内只有诺诚健华的ICP-105与基石药业的CS-3008进入了临床试验阶段。
2款药物提交IND申请,还有5款药物在临床前
ICP-248/ICP-B03/ICP-488/ICP-490/ICP-189等5款新药仍处于临床前阶段,其中ICP-189的IND申请已于今日(7月28日)获NMPA受理;ICP-033和双特异性抗体处于提交IND申请阶段,且前者已获批临床。
而作为诺诚健华目前唯一一款上市的创新药,在正式进入商业化阶段的同时,BTK抑制剂奥布替尼也没有停下其研发的脚步。
商业化与研发同步进行,奥布替尼拓展多个适应症
奥布替尼是诺诚健华自主研发的新型BTK抑制剂,以其独特的结构优势,提高了激酶选择性,减少了脱靶效应,疗效更好,安全性也更高,具有成为Best-in-class(同类最佳)的潜力。
2020年12月25日,奥布替尼正式获得NMPA批准上市,用于既往至少接受过一种治疗的成人套细胞淋巴瘤和慢性淋巴细胞白血病患者。就在本月13日,诺诚健华还就奥布替尼与渤健达成许可合作协议,正式出海,诺诚健华将获得1.25亿美元首付款,未来有资格获得最多8.125亿美元的潜在临床开发里程碑和商业里程碑付款。
迎来收获期后,奥布替尼的研发并没有就此停下,目前正在国内外登记开展多项临床试验,适应症包括肿瘤领域的套细胞淋巴瘤、慢性淋巴细胞白血病、边缘区B细胞淋巴瘤、非霍奇金淋巴瘤,和自身免疫性疾病的系统性红斑狼疮、多发性硬化症等。其中已有多个适应症进入临床II期。
表2 奥布替尼研发进展

数据来源:药融云全球药物研发数据库
恒瑞、人福、艾森医药……众多药企冲击BTK抑制剂百亿市场
由于BTK抑制剂在治疗B细胞恶性肿瘤及一些B细胞免疫类疾病中优势明显,近年来,BTK靶点已成为该领域的热门靶点,市场空间潜力巨大。据Frost&Sullivan预测,随着新产品和新适应症的陆续获批,到2030年,BTK抑制剂的全球销售额将达到178亿美元。
面对前景如此广阔的百亿市场,BTK抑制剂的研发竞争也相当激烈,国内外众多药企纷纷投身加入这个赛场之中。奥布替尼并不是第一个进入这个市场的选手,也不会是最后一个。
2019年11月14日,FDA批准百济神州的BTK抑制剂泽布替尼上市,这是我国完全自主研发的抗癌新药首次获得FDA批准,堪称“零的突破”。2020年6月2日,泽布替尼在我国获批上市,用于既往至少接受过一种治疗的成人套细胞淋巴瘤和慢性淋巴细胞白血病患者,是我国第一个获批的国产BTK抑制剂创新药。
奥布替尼则是中国自主研发的第二款国产BTK抑制剂,也是继伊布替尼(强生/艾伯维)、泽布替尼后,国内第三款上市的BTK抑制剂。它的上市,将BTK抑制剂的竞争推入一个白炽化的阶段。
截止目前为止,我国创新药企共有42个BTK抑制剂创新药在研,2个已上市,1个已提交NDA申请,4个BTK抑制剂处于临床二期(浙江导明的DTRM-555,杭州艾森医药的AC-0058、恒瑞的SHR-1459、北京赛林泰的CT-1530),另有12个处于临床一期,13个处于临床前阶段。
图1 我国1类BTK抑制剂研发情况
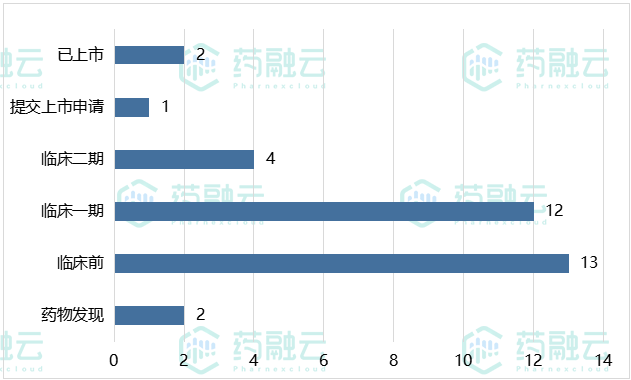
数据来源:药融云全球药物研发数据库
结语
诺诚健华是一个根植于中国,拥有一体化生物医药平台的领先生物医药公司,致力于研发肿瘤免疫领域的me-better或me-first药物,为患者提供更好的选择。其核心产品奥布替尼能否在百花齐放的BTK抑制剂市场中分得一杯羹?其后续又会有哪些造福患者的新药研发动作?让我们拭目以待。





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论