恒瑞医药作为中国创新药研发领域的标杆,有国内“创新药一哥”之称。据药融云数据库统计,目前公司已有11款创新药获批上市,另有60多款创新药正在临床开发,260多项临床项目在国内外开展。
2月12日,恒瑞医药抗肿瘤新药成功出海。公告显示:将自研抗肿瘤新药SHR2554授权给美国Treeline公司在大中华外的开发、生产和商业化权益,潜在交易总金额超过7亿美元(《国内ADC药物研发火热!恒瑞医药8款在研,捷报频传》)。据悉,截至目前,恒瑞医药在该产品的相关项目上已投入研发费用约8,938万元人民币。
创新国际化,是恒瑞医药的长期发展战略。目前,恒瑞医药在海外开展国际临床试验近20项,覆盖抗肿瘤、血液、心血管等不同疾病领域,其中7项国际多中心项目进入III期临床。
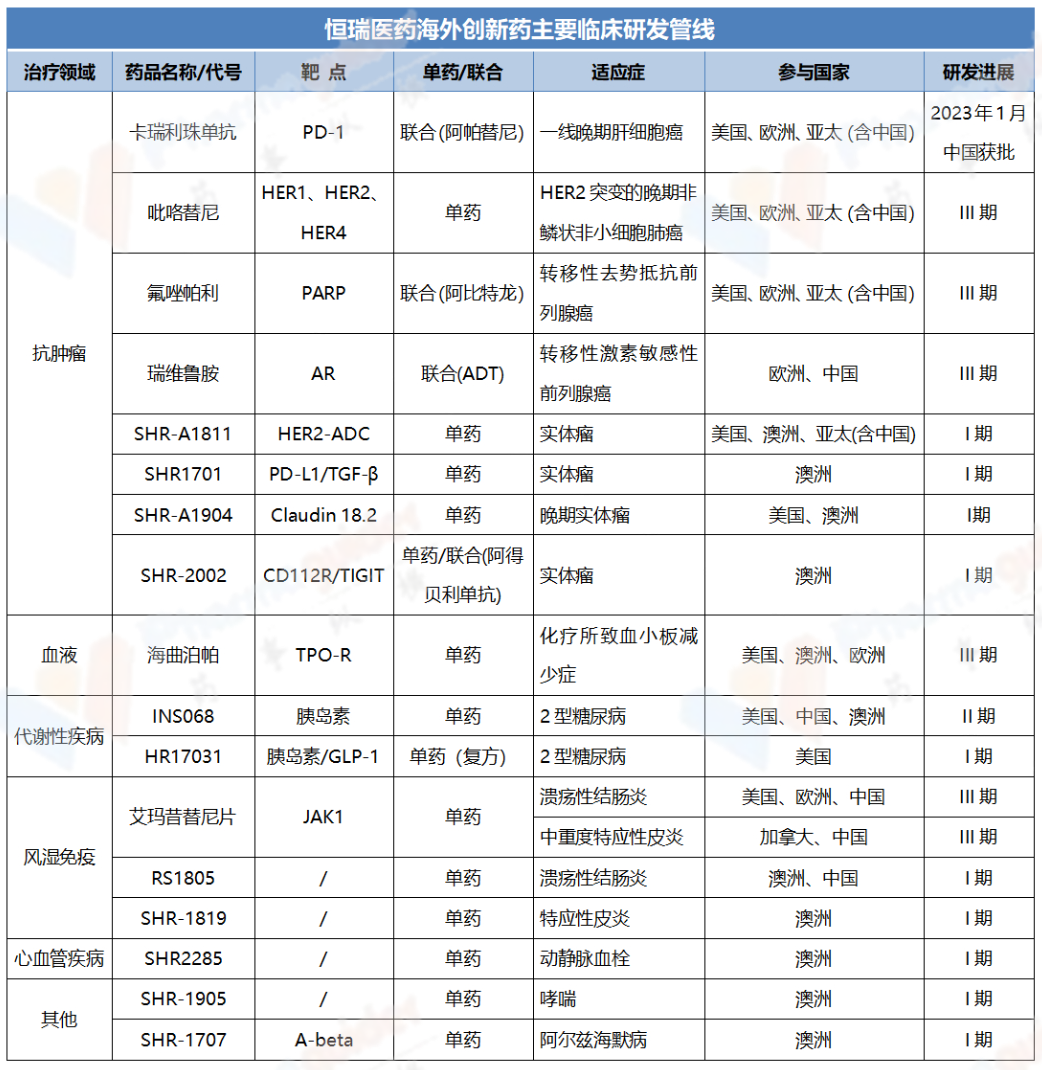
一、国际化稳步推进,恒瑞医药即将迎来收获期
01.卡瑞利珠单抗
卡瑞利珠单抗是恒瑞医药自主研发的人源化PD-1单抗,于2019年5月在获批上市。目前已在肺癌、肝癌、食管癌、鼻咽癌以及淋巴瘤五大瘤种中获批9个适应症。2023年1月,中国国家药监局批准卡瑞利珠单抗(商品名:艾瑞卡®)联合阿帕替尼(商品名:艾坦®)(“双艾”组合)用于晚期肝细胞癌一线治疗。
卡瑞利珠单抗适应症研发现状(部分,微信搜索"药融云小程序"进行相关更多数据查询)
截图来源:药融云全球药物研发数据库
本次“双艾”组合用于肝癌一线治疗适应症的获批,是基于恒瑞医药推进开展的一项国际多中心III期临床研究(SHR-1210-Ⅲ-310研究)。研究结果显示,“双艾”组合一线治疗晚期肝癌具有显著的生存获益和可耐受的安全性,中位总生存期(OS)达到22.1个月,为目前晚期肝癌一线治疗最长OS获益组合。
SHR-1210-Ⅲ-310研究也是恒瑞医药推进开展的首个国际多中心III期临床研究,项目团队已完成与美国FDA的多轮沟通,计划在美国递交新药上市申请。此前2021年4月,卡瑞利珠单抗获得了美国FDA孤儿药资格认定(ODD),用于肝细胞癌适应症。
02.吡咯替尼
吡咯替尼是一种小分子、不可逆、泛ErbB受体酪氨酸激酶抑制剂,也是中国首个自主研发的HER1/HER2/HER4靶向药物。吡咯替尼于2018年8月获国家药监局有条件批准上市(商品名:艾瑞妮®),并于2020年7月获得完全批准,获批适应症为联合卡培他滨用于治疗HER2阳性、接受过曲妥珠单抗的复发或转移性乳腺癌患者。
目前,一项吡咯替尼对比多西他赛治疗含铂化疗失败的HER2突变的晚期非鳞状非小细胞肺癌的国际多中心III期临床研究(NCT04447118)正在进行中。
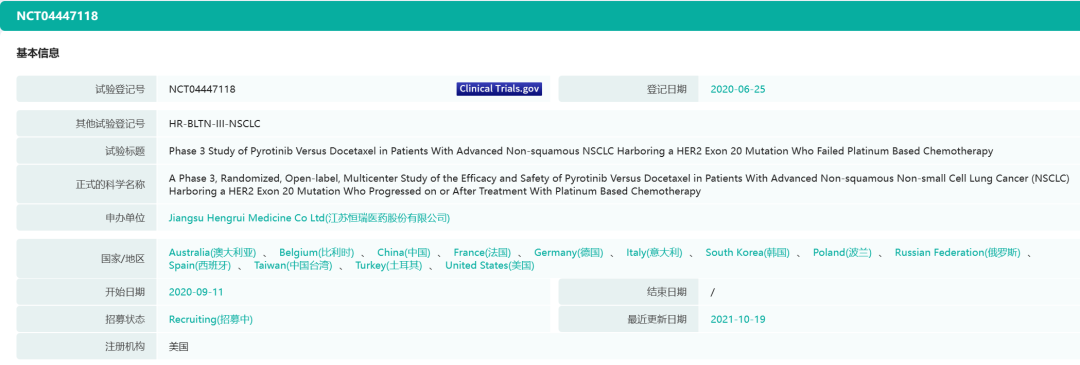
截图来源:药融云中国临床试验数据库
03.氟唑帕利
氟唑帕利是一种聚腺苷二磷酸核糖聚合酶(PARP)抑制剂,也是中国首个自主研发、拥有知识产权专利的PARP抑制剂。2020年12月,氟唑帕利胶囊获得国家药监局批准上市(商品名:艾瑞颐®),用于既往经过二线及以上化疗的伴有胚系BRCA突变(gBRCAm)的铂敏感复发性卵巢癌、输卵管癌或原发性腹膜癌患者的治疗。
氟唑帕利审评概况
截图来源:药融云中国药品审评数据库
目前,氟唑帕利正在开展联合醋酸阿比特龙片和泼尼松片(AA-P)对比安慰剂联合AA-P一线治疗转移性去势抵抗性前列腺癌患者的国际多中心、随机、双盲、安慰剂对照的III期临床研究。该研究在全球约有150家参研中心。
04.瑞维鲁胺
瑞维鲁胺是一种新型AR抑制剂,2022年6月,瑞维鲁胺获得国家药监局批准上市(商品名:艾瑞恩®),用于高瘤负荷的转移性激素敏感性前列腺癌(mHSPC)的治疗。
2022年9月,由复旦大学附属肿瘤医院叶定伟教授牵头的国际多中心、随机、对照的III期临床研究——CHART研究重磅发表于国际权威医学期刊《柳叶刀·肿瘤学》,这项研究旨在评估瑞维鲁胺联合雄激素剥夺疗法(ADT)对比标准治疗联合ADT在高瘤负荷mHSPC患者中的疗效和安全性。
此次发表的结果显示,相较于标准治疗联合ADT,瑞维鲁胺联合ADT治疗高瘤负荷mHSPC患者,可显著延长影像学无进展生存期(rPFS)和总生存期(OS),降低影像学进展或死亡风险56%,降低死亡风险42%。
05.海曲泊帕乙醇胺片
海曲泊帕乙醇胺片是一种口服非肽类血小板生成素受体(TPO-R)激动剂。2021年6月,获国家药监局批准上市(商品名:恒曲®),用于既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性原发免疫性血小板减少症(ITP)成人患者的治疗,以及用于对免疫抑制治疗疗效不佳的重型再生障碍性贫血成人患者的治疗。
2022年1月,恒瑞医药创新药海曲泊帕乙醇胺片治疗恶性肿瘤化疗所致血小板减少症(CIT)的III期临床研究获批在美国开展临床试验,同年6月,海曲泊帕乙醇胺片获得美国FDA授予的孤儿药资格认定。除了美国外,海曲泊帕乙醇胺片治疗CIT的临床研究也正在欧洲及澳大利亚开展。
海曲泊帕乙醇胺适应症研发现状及特殊审批认证
截图来源:药融云全球药物研发数据库
06.艾玛昔替尼片
艾玛昔替尼片是首个国内自主研发的新一代JAK1抑制剂。2021年1月,艾玛昔替尼片被CDE纳入突破性治疗品种(BTD)。
2022年11月,恒瑞医药宣布用于治疗成人和12岁及以上青少年特应性皮炎的III期国际多中心临床研究QUARTZ3(NCT04875169),经评估达到研究预设的共同主要终点及所有关键次要终点。
恒瑞医药子公司瑞石生物正在筹备与国家药监部门沟通新药上市申请事宜,艾玛昔替尼片有望成为首个针对自免适应症获批上市的国内自研JAK1抑制剂。
除了特应性皮炎,艾玛昔替尼片还在多个自身免疫疾病开展II/III期临床研究,包括溃疡性结肠炎、克罗恩病、斑秃、类风湿关节炎、强直性脊柱炎、银屑病关节炎等。
小结
近年来,恒瑞医药大力推进科技创新和国际化战略,在全球多个国家和地区设立研发中心,积极拓展海外市场。目前,恒瑞医药多个国际多中心临床项目迎来重要节点,海外新药研发的布局,或将陆续开花结果。
参考来源:
[1] 药融云数据库
[2] 恒瑞医药官方披露
想要解锁更多药企创新药研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品管线、药物研发现状、申报审批情况、临床试验信息、最新进展、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论