
蓝鸟生物原计划于8月19日提交美国FDA的基因疗法Zynteglo(beti-cel)提前2天迎来了好消息。
8月17日,蓝鸟生物宣布美国FDA批准Zynteglo用于治疗β地中海贫血。这是第一个针对需要定期输血的β地中海贫血患者的基因疗法。这让原本因为Zynteglo迟迟未批而出现财务危机的蓝鸟生物一下子“复活”过来。据药融云数据库显示,该药是蓝鸟生物自主研发的一款HBB靶向、针对血液系统、适用于β地中海贫血疾病的创新药物。
Zynteglo药物基本信息
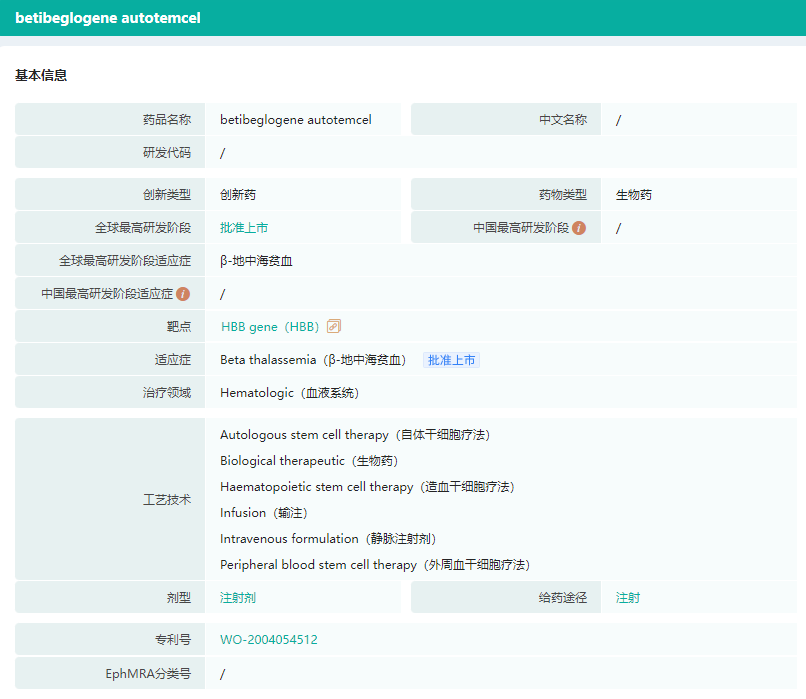
截图来源:药融云全球药物研发数据库
事实上,蓝鸟生物Zynteglo早先已在多国获批上市。其中,最早于2019年5月底获欧盟委员会(EC)批准,进入欧盟市场。后又在同年6月初,同步在挪威、冰岛、列支敦士登上市。
Zynteglo各国研发状态

截图来源:药融云全球药物研发数据库
据了解,蓝鸟生物为Zynteglo的定价为280万美元,超过诺华的基因疗法Zolgensma(定价210万美元),一跃成为“史上最贵药”。
蓝鸟生物研发管线
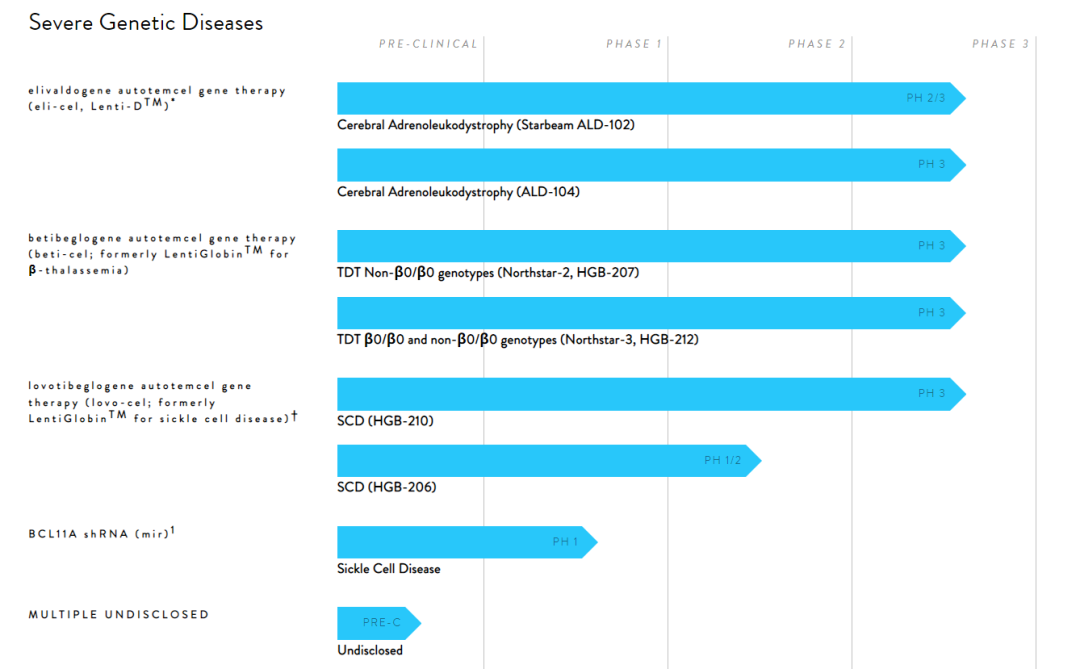
来源:蓝鸟生物官网
β地中海贫血是一种罕见的遗传性血液病,由β-珠蛋白基因突变引起,其特征是成人血红蛋白生成显著减少或缺失。患者会出现严重贫血并需要终生输血。尽管治疗取得了进步,输血技术得到改进,但输血只能暂时解决贫血症状。而定期输血也带来了严重的并发症——铁超负荷,导致脏器功能异常,增加死亡率。有数据表明:过去十年中,输血依赖型β地中海贫血患者的死亡年龄中位数是37岁。蓝鸟生物估计,美国约有1,300-1,500人患有输血依赖型β-地中海贫血。
蓝鸟生物首席执行官Andrew Obenshain说道:“FDA对Zynteglo的批准为β地中海贫血患者提供了新的治疗方式,避免了长期繁重的常规红细胞输血治疗和铁超负荷并发症。Zynteglo经过十多年坚持不懈的研究与临床开发,成为第一个获批用于β地中海贫血的基因疗法,它的获批标志着基因治疗进入一个分水岭阶段。
最后,让我们拭目以待蓝鸟生物计划于9月16日接受审查的另一款基因疗法eli-cel的获批结果。
参考资料:
[1] https://investor.bluebirdbio.com/news-releases/news-release-details/bluebird-bio-announces-fda-approval-zynteglor-first-gene-therapy
[2] 药融云数据库
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、研发阶段、最新进展、申报获批情况、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论