药融云中国药品审评数据库显示,近日,国家药品监督管理局通过优先审评审批程序批准了南京圣和药业自主研发的化学1类创新药品种「奥磷布韦片」(商品名:圣诺迪)上市。
一、国内首个HCV NS5B聚合酶抑制剂,治愈率98.5%
奥磷布韦片(曾用名:和乐布韦片,SH229片)是国内首个拥有自主知识产权的HCV NS5B聚合酶抑制剂,属于泛基因型慢性丙肝治疗直接抗病毒药物(Direct antiviral agent, DAA),与盐酸达拉他韦联用,治疗初治或干扰素经治的泛基因型成人慢性丙型肝炎病毒(HCV)感染,可合并或不合并代偿性肝硬化。
奥磷布韦片审评时间轴—获批上市耗时912天
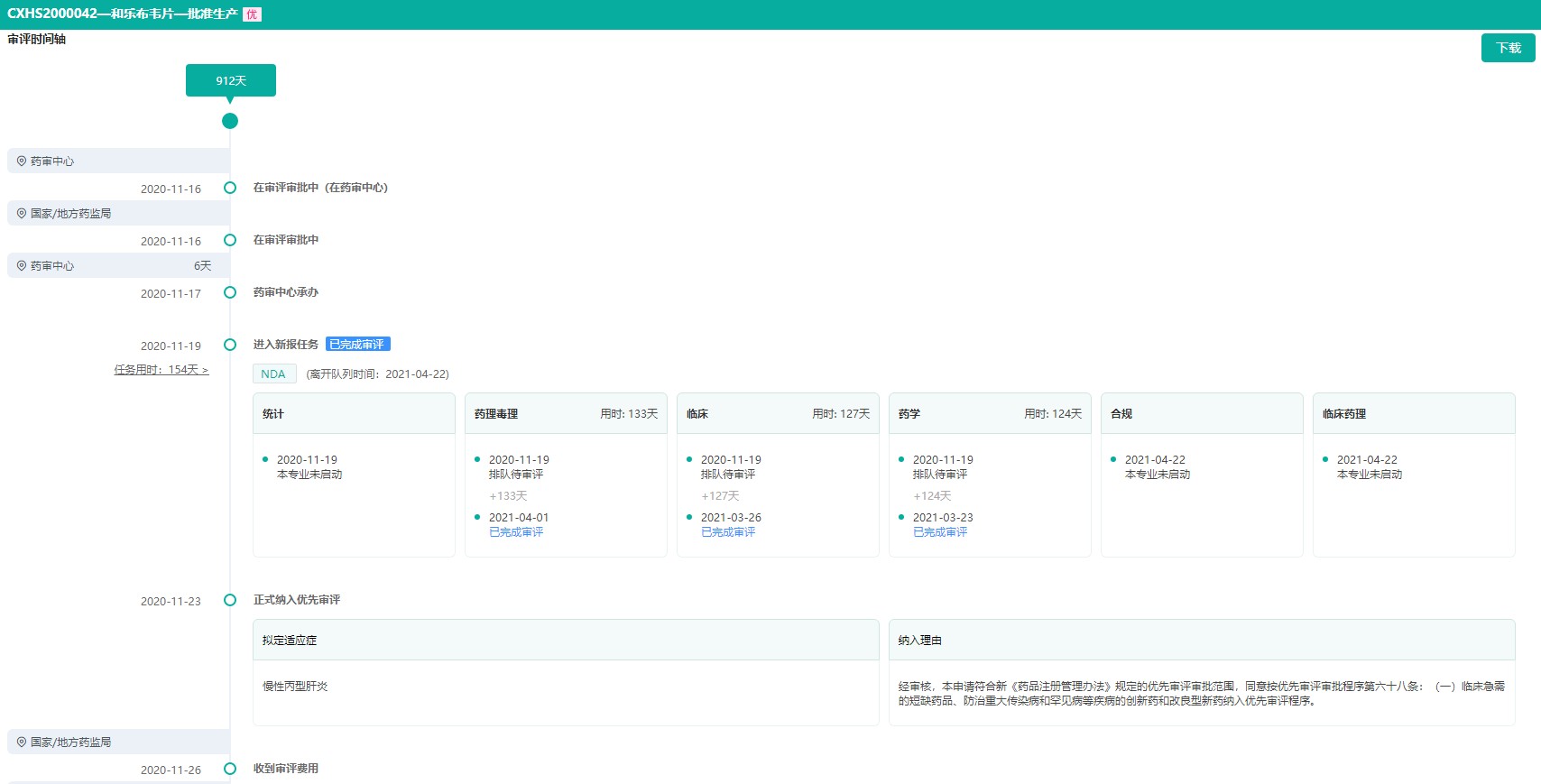
图片来源:药融云中国药品审评数据库
奥磷布韦是一种核苷酸前体药物,可通过肝脏代谢,转化为具有抗病毒活性的非天然核苷三磷酸。该非天然核苷三磷酸可以与丙肝病毒复制所需的NS5B聚合酶发生竞争性结合,“假扮”成病毒复制时需要的天然核苷三磷酸掺入到HCV RNA链中,形成错误的病毒RNA模板,导致病毒RNA链的延长提前终止,丙肝病毒的复制也因此被终止。
奥磷布韦的III期临床研究数据显示,奥磷布韦联合盐酸达拉他韦的治疗方案在不同基因型的HCV患者中均表现出良好的治疗效果,在治疗结束后第12周时,共有321例受试者获得了持续病毒学应答,SVR12率及95%置信区间为98.5%(96.5%,99.5%)。
奥磷布韦III期临床试验结果查询(部分展示)
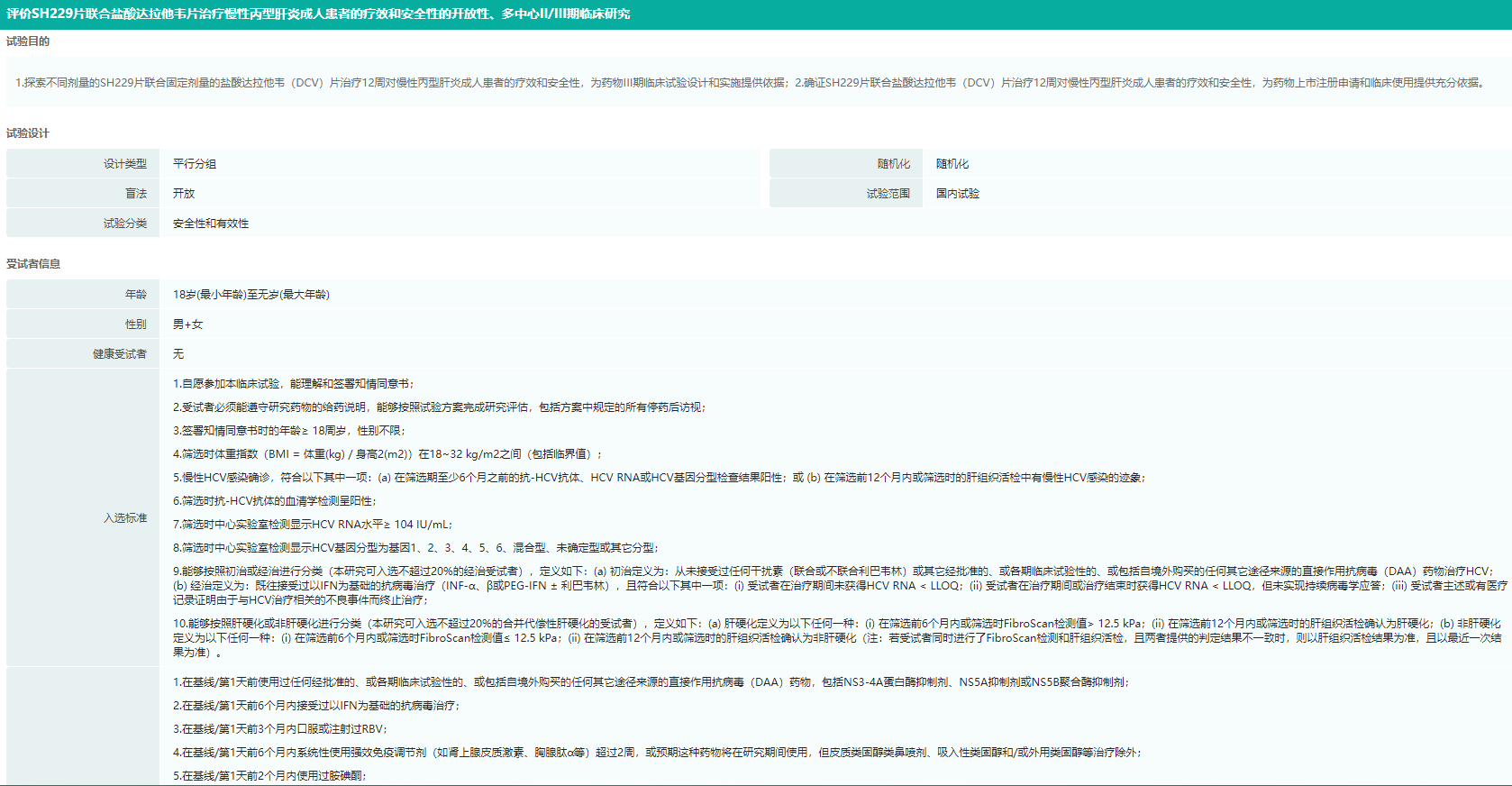
图片来源:药融云中国临床试验数据库
而且,对于目前最难治的GT-3患者(特别是GT3b患者),奥磷布韦联合盐酸达拉他韦的治疗方案表现出了比现有标准治疗(SOC)更高的持续病毒学应答率,具有更优秀的治疗效果。因此,奥磷布韦片的上市,为成人慢性丙型肝炎病毒患者提供了新的治疗选择。
二、丙型肝炎——“一个隐匿的杀手”
丙型肝炎是由丙型肝炎病毒(HCV)感染引起的肝损伤性疾病,感染初期症状轻微或无症状,后期可能会导致各种肝脏疾病、肝硬化甚至肝癌。丙肝属于经血传播的疾病,其传播路径播途径包括经输血和血液制品传播,经破损的皮肤和粘膜传播,经性接触传播以及母婴传播。
在国内,丙肝近年来保持着年增20万左右病例的速度,但这些感染者被发现的人极少,已确诊患者仅 7%~8%接受正规治疗,很多患者不知已被感染丙肝,等出现症状时已发展到肝硬化、腹水、肝癌。因此,丙肝常被称为“沉默的杀手”。
目前,针对丙型肝炎可以通过抗病毒治疗,包括口服的抗病毒药物和干扰素、HCV直接作用抗病毒药物,有效的控制病毒的复制,延缓疾病的进展。
丙型肝炎全球药物研发进展查询(部分,完整内容请登录“药融云数据库www.pharnexcloud.com/?mh”查看)
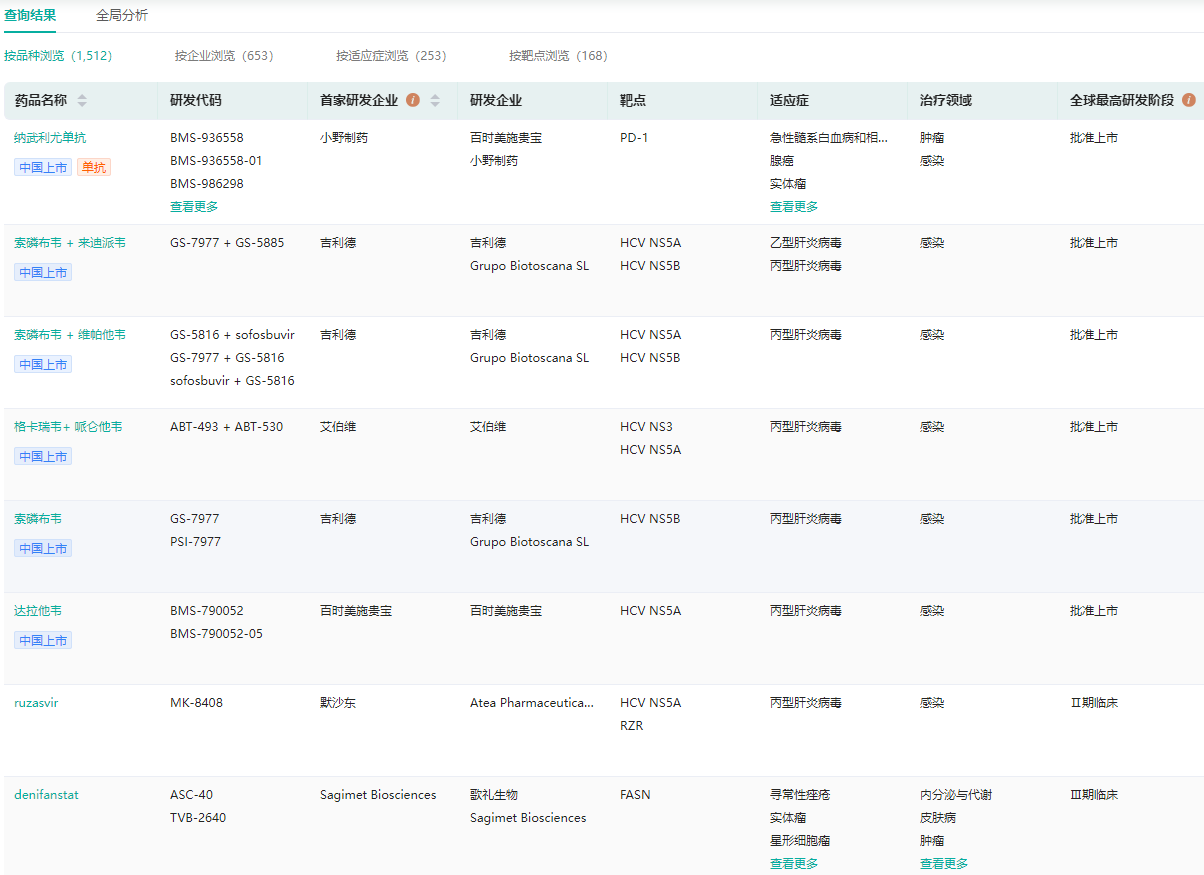
图片来源:药融云全球药物研发数据库
1.干扰素类药物
干扰素α和干扰素β被广泛应用于丙型肝炎治疗中。干扰素的机制是通过激活宿主免疫系统,抑制HCV复制和生长。但是,干扰素类药物需要经过注射给药,副作用明显,且疗效有限,只能在一部分患者中产生有效的治疗效果。
2.利巴韦林类药物
利巴韦林类药物是一类广谱抗病毒药物,可用于治疗多种病毒感染,包括丙型肝炎、流感、RS病毒等。其作用机制是通过抑制HCV NS5B RNA聚合酶的活性,从而阻断HCV的复制。
利巴韦林是第一代HCV治疗药物之一,在使用DAAs出现之前曾是HCV治疗的主要选择。但由于其副作用较多,如贫血、恶心、呕吐和头痛等,以及疗效不佳,需要与其他药物联合应用,因此在DAAs的出现后逐渐被取代。
利巴韦林生产企业查询(部分展示)
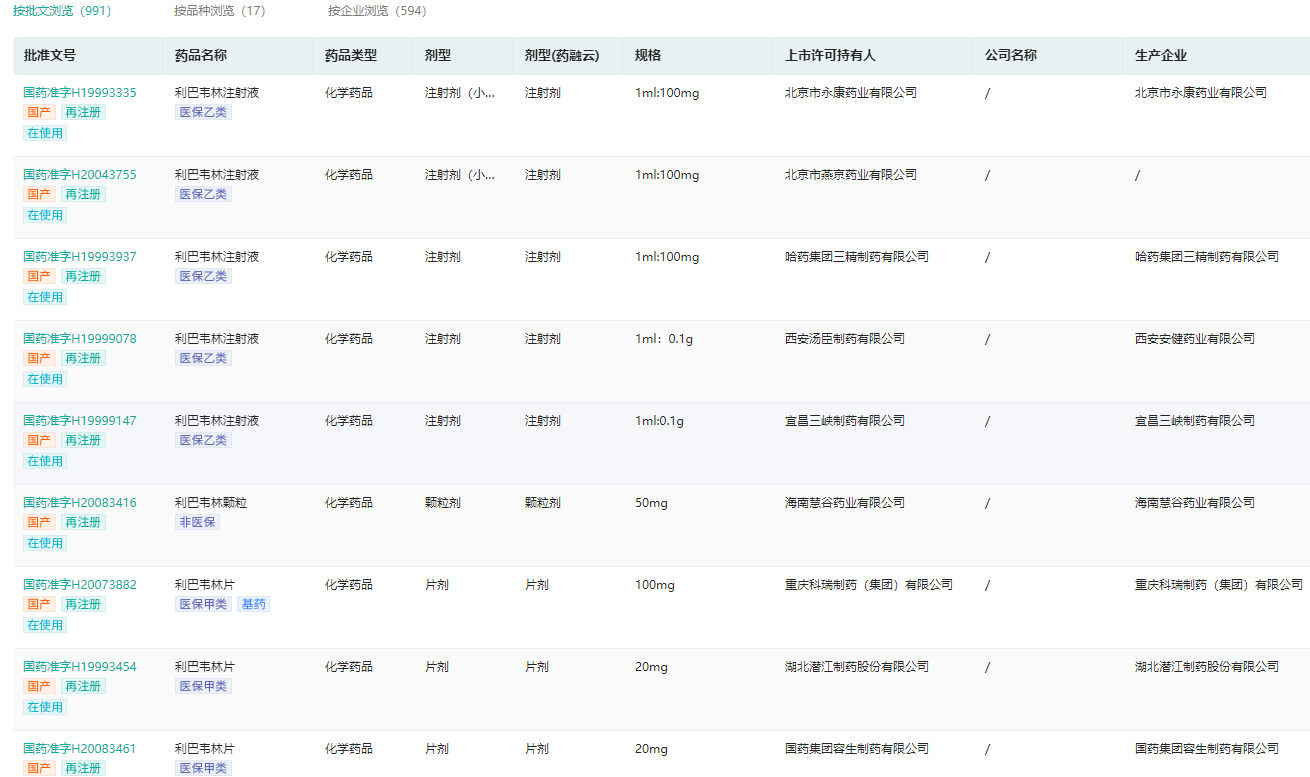
图片来源:药融云中国药品批文数据库
3.HCV直接作用抗病毒药物(DAAs)
HCV直接作用抗病毒药物(DAAs)是一类针对丙型肝炎病毒(HCV)的新一代药物。它们直接与病毒的生命周期相关的分子结构进行作用,从而抑制病毒的复制和传播。根据其作用机制的不同,可以将DAAs分为多种类型,例如NS3/4A蛋白酶抑制剂、NS5A抑制剂和NS5B聚合酶抑制剂等。
目前已经上市的DAAs有索非布韦(Sofosbuvir)、达拉他韦(Daclatasvir)、维康宁(Viekira Pak),以及奥磷布韦片等药物,这些药物可以与其他抗病毒药物联合使用。同时,也有不同的DAAs联合治疗方案,如以达卡他韦和阿巴卡韦为主的治疗方案等。
药融云数据库显示,达拉他韦是全球首个获批上市的NS5A复制复合体抑制剂,由百时美施贵宝公司研发,于2014年7月获日本PMDA批准上市,于2015年7月获得美国FDA批准上市,商品名Daklinza®;后又于2017年4月在中国获批上市。
达拉他韦上市时间轴
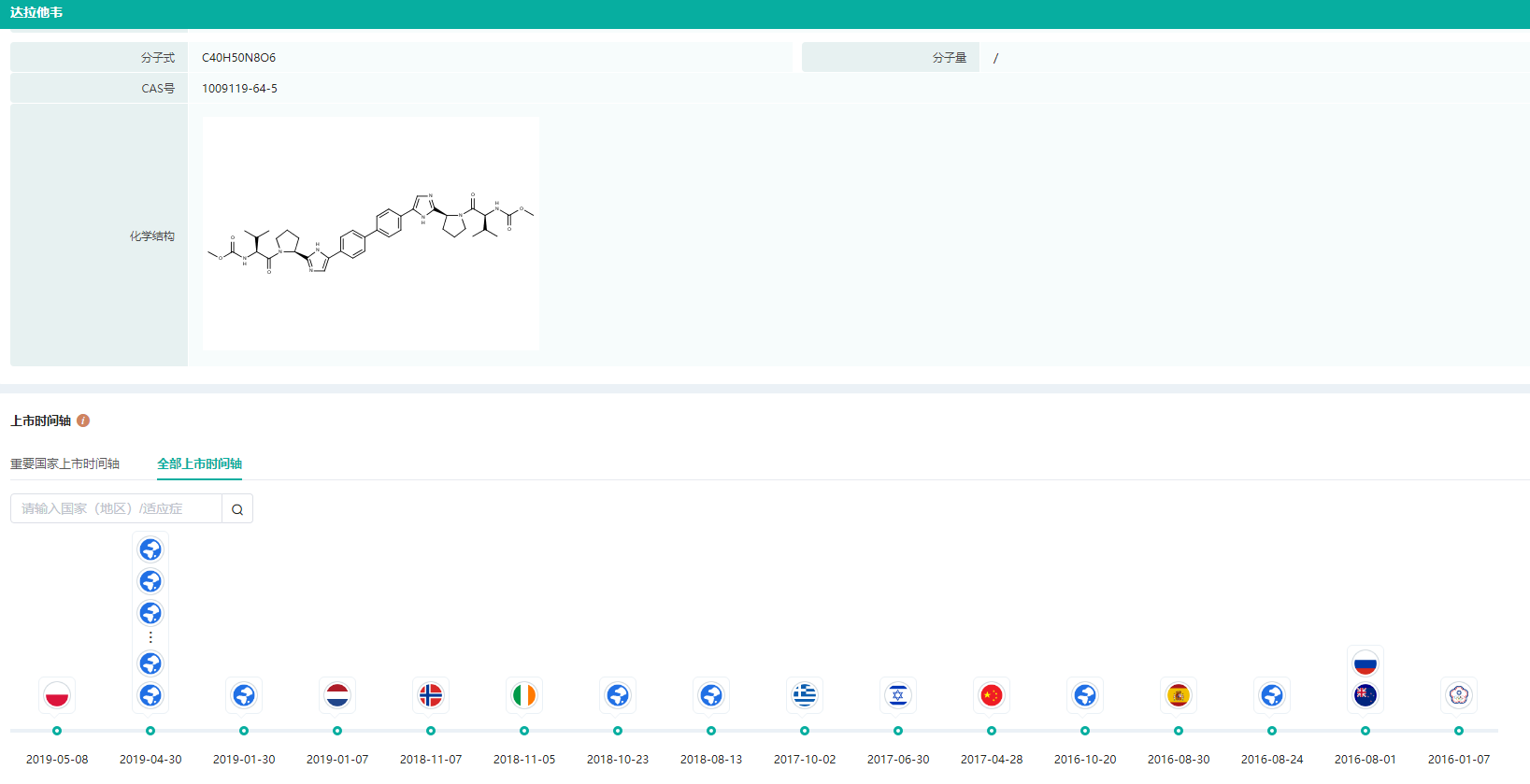
图片来源:药融云全球药物研发数据库
使用DAAs治疗HCV感染的优点在于其疗效高、安全性好、疗程短、副作用小等。因此,DAAs已成为HCV感染治疗的主要选择,并在近年来得到了广泛应用。需要注意的是,不同的DAAs方案和不同的患者情况都可能影响丙型肝炎的治疗效果,因此治疗方案需要个体化制定,并严格按照医生的建议进行治疗。
除此之外,基因治疗也是一种新兴治疗方法,其原理是将外源DNA或RNA导入人体细胞中,从而产生相应的蛋白质,以达到治疗疾病的效果。在丙型肝炎治疗中,基因治疗能够通过介导宿主细胞产生抗HCV蛋白质,从而抑制病毒的复制和生长,具有潜在的治疗价值。
想要解锁更多疾病领域信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握疾病领域涉及药物信息、销售情况与各维度分析、市场竞争格局、创新药研发情况、仿制药布局情况、最新进展、市场规模与前景等,以及帮助企业抉择可否投入仿制与研发时提供数据参考!注册立享15天免费试用!

<END>























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论