1.1.1 总体概况
根据摩熵医药数据统计,2024.08.26-2024.09.01期间共有72个创新药/改良型新药临床申请/上市申请获国家药品监督管理局药品审评中心(CDE)承办(按受理号统计,不含补充申请)。其中,国产药品受理号58个,进口药品受理号14个。
本周共计39款创新药/改良型新药临床试验申请获得“默示许可”,包括化学药20款,生物药19款,中药1款。其中值得注意的有:
(1)HP515片
8月26日,CDE官网公示:海创药业的HP515片获得临床试验默示许可,用于治疗非酒精性脂肪性肝炎。公开资料显示,HP515片是海创药业自主研发的一种口服高选择性THR-β激动剂,能直接作用于THR-β激活下游基因转录,通过增强肝细胞脂质代谢活性、提高肝脏脂肪代谢、降低脂毒性达到对非酒精性脂肪性肝炎的改善效果。
(2)AK135注射液
8月27日,CDE官网公示:康方生物的AK135注射液获得临床试验默示许可,用于治疗化疗诱导的周围神经病变。公开资料显示,AK135为靶向IL-1RAP的生物药,IL-1RAP通过白细胞介素1、33和36 (IL-1, IL-33, IL-36)信号通路高度参与炎症过程,并且在多种血液学和实体癌的肿瘤细胞中被发现过表达。
(3)177Lu-TR0471注射液
8月27日,CDE官网公示:通瑞生物的177Lu-TR0471注射液获得临床试验默示许可,用于治疗已接受雄激素受体抑制剂但未接受过紫杉类化疗的前列腺特异性膜抗原(PSMA)阳性转移性去势抵抗性前列腺癌(mCRPC)的成年患者。公开资料显示,177Lu-TR0471是一款放射性药物。
本周共4款新药获批上市,即福泽雷塞片、夫那奇珠单抗注射液、赛立奇单抗注射液和西达基奥仑赛注射液。8月27日,CDE发布药品批准证明文件送达信息,信达生物的福泽雷塞片获批上市,适用于至少接受过一种系统性治疗的鼠类肉瘤病毒癌基因(KRAS)G12C突变型的晚期非小细胞肺癌(NSCLC)成人患者,为患者提供新的治疗选择。公开资料显示,福泽雷塞是我国自主研发的一款新型、具有口服活性的强效KRAS G12C抑制剂,可通过阻断KRAS依赖的信号转导,诱导细胞凋亡,并抑制肿瘤细胞的增殖。
8月27日,CDE批准恒瑞医药的夫那奇珠单抗注射液上市,用于治疗适合接受系统治疗或光疗的中重度斑块状银屑病的成人患者。公开资料显示,夫那奇珠单抗是恒瑞医药自主研发的一种靶向人IL-17A的重组人源化单克隆抗体。
8月27日,CDE批准智翔金泰的赛立奇单抗注射液上市,用于治疗中、重度斑块状银屑病。公开资料显示,该药品是由智翔金泰自主研发的全人源(IgG4亚型)抗人IL-17A单克隆抗体,是国内首个全人源IL-17A靶点药物。
8月27日,CDE批准传奇生物的西达基奥仑赛注射液上市,用于治疗复发或难治性多发性骨髓瘤成人患者,既往接受过至少三线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。公开资料显示,该药品是一种靶向B细胞成熟抗原(BCMA)的经基因修饰的自体嵌合抗原受体T细胞(CAR-T)治疗产品,该产品具有独特的CAR结构,由两个靶向BCMA的纳米抗体串联构成,在体内与表达BCMA的骨髓瘤细胞结合,诱导T细胞的活化与增殖,从而清除骨髓瘤细胞。
1.1.2 本周获批临床创新药/改良型新药信息速览(不含补充申请)
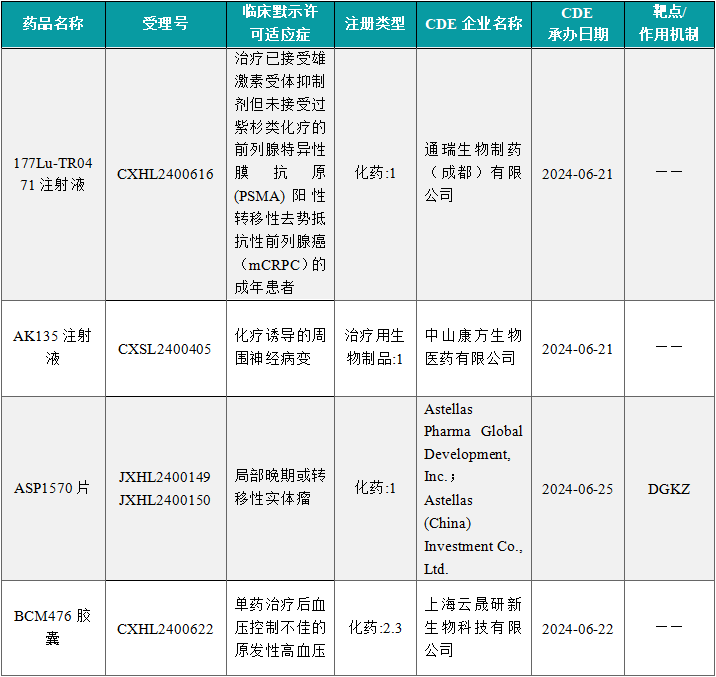
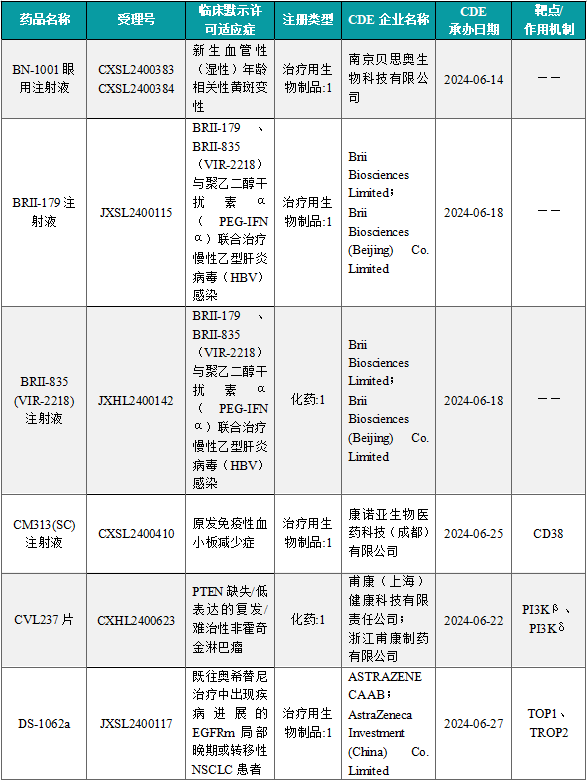
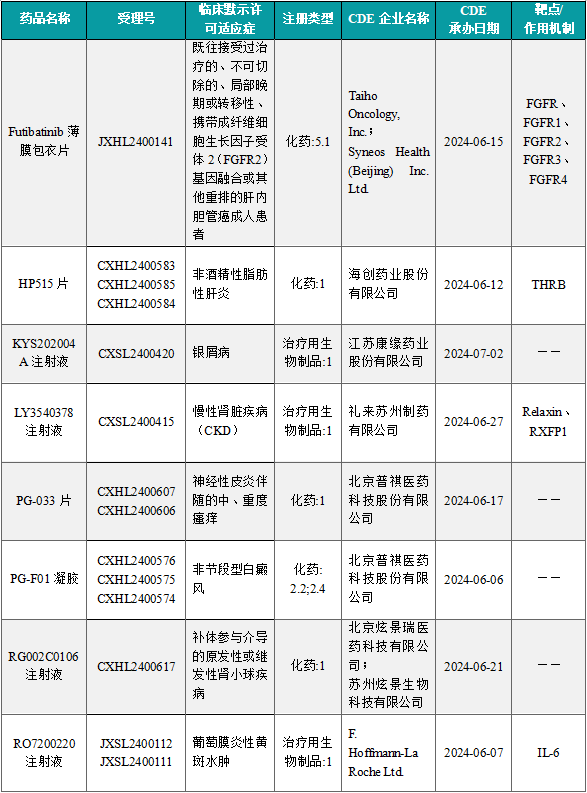
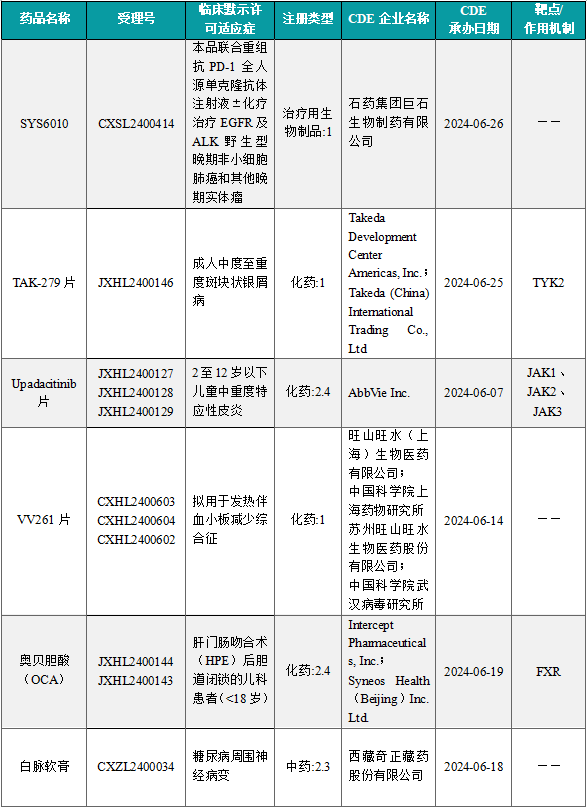
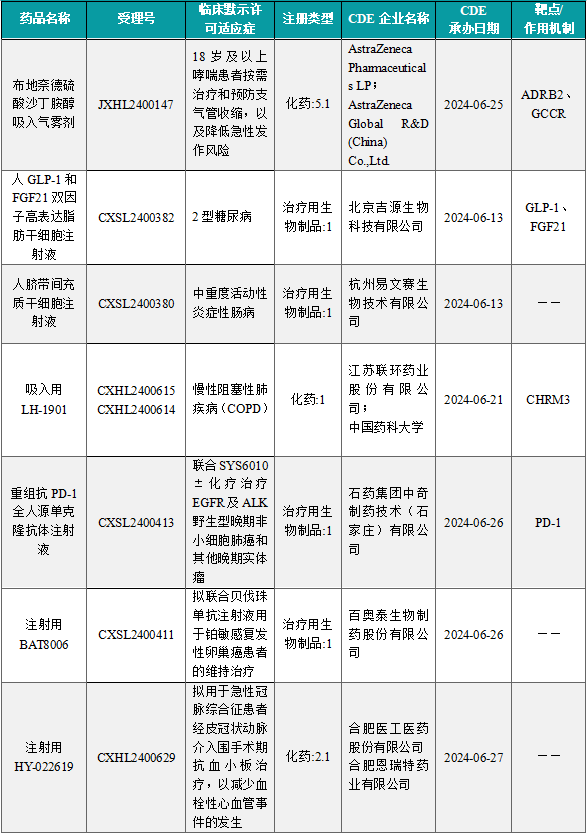
备注:(1)此处未包括补充申请之情形;(2)此处所列创新药/改良型新药,主要是指CDE受理批准的1类、2类、5.1类以及生物制品3.1类和3.2类。(3)更多获批临床信息及研发进展详情及相关靶点全局分析等,可通过摩熵医药中国药品审评数据库获取并下载EXCEL表格。
1.1.3 本周获批上市创新药信息速览
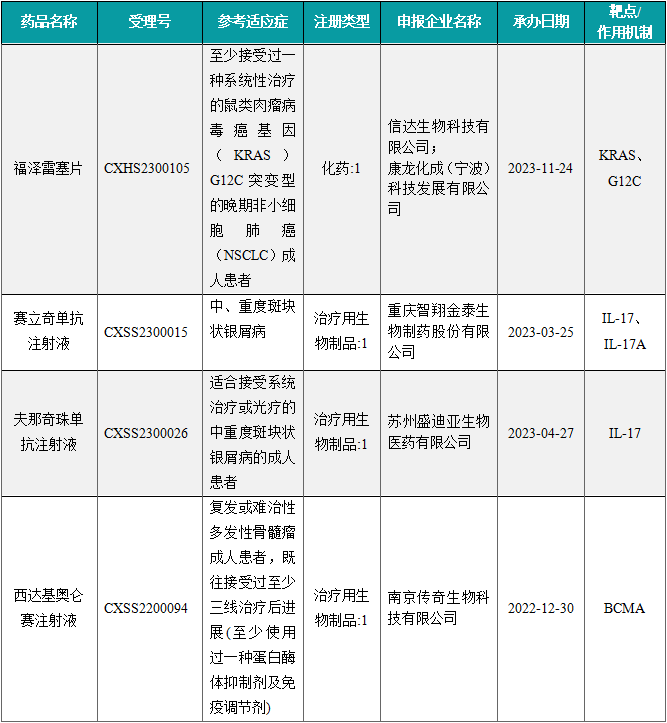
备注:(1)此处所列新药,主要是指国家药品监督管理局(NMPA)首次批准在中国上市的药品,包括新分子实体(以及包含有新分子实体的复方)、生物药、中药和疫苗。其中,新分子实体主要是化药注册分类下的1类(境内外均未上市的创新药)、5.1类(境外上市的原研药申请在国内上市);生物药主要为NMPA首次批准的国产及进口生物药;不包括生物类似物、新适应症、新剂型。(2)更多信息如获批临床品种相关靶点、研发企业、全球上市及研发进展及相关靶点全局分析等,可通过摩熵医药投融资数据库获取并下载EXCEL表格。
同期事件:
1. 2024年第35周08.26-09.01国内仿制药/生物类似物申报/审批数据分析
2. 2024年第35周08.26-09.01国内医药大健康行业政策法规汇总
3. 2024年第35周08.26-09.01全球医药大健康行业投融资数据
4. 2024年第35周08.26-09.01全球创新药研发概览
以上内容均来自{摩熵咨询医药行业观察周报(2024.08.26-2024.09.01)},如需查看或下载报告,可点击!
<END>
想要解锁更多药物研发信息吗?查询摩熵医药数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论