
近期,曾凭借 4.25 亿美元 A 轮融资轰动行业的 Biotech 公司 Areteia Therapeutics 传出关闭消息,其唯一核心产品 dexpramipexole 的全球研发(含中国已启动的临床试验)或彻底搁浅。
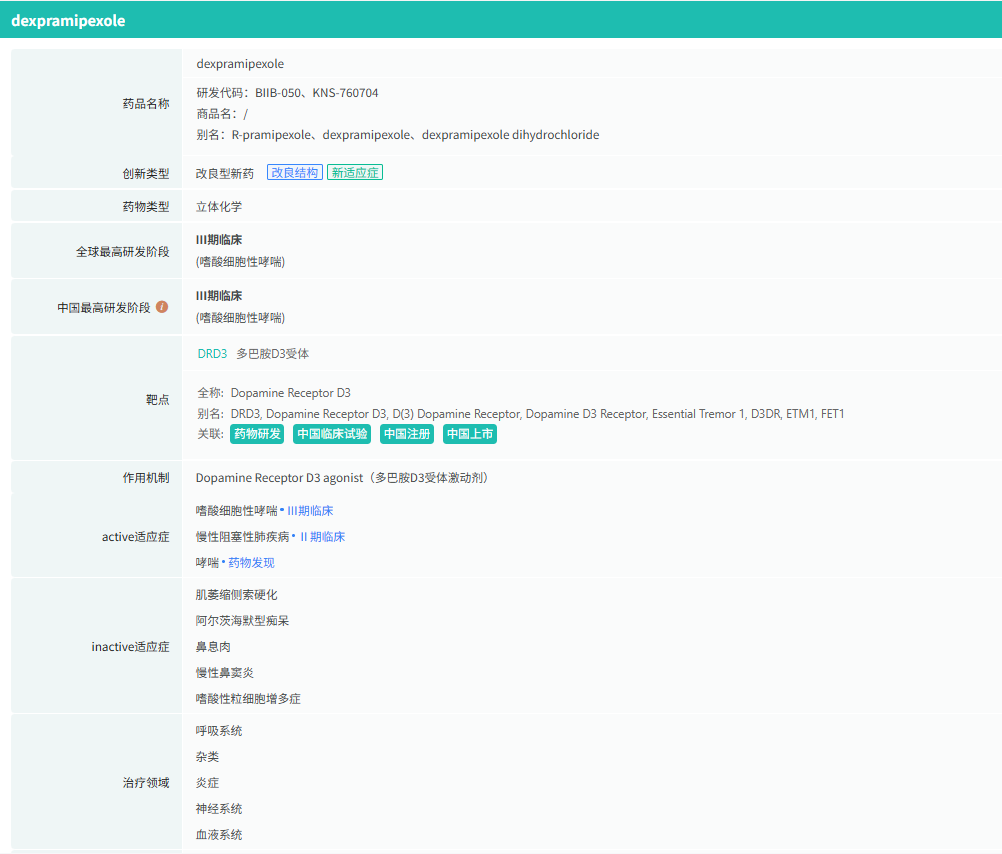
截图来源:摩熵医药数据库-全球药物研发数据库
与资本寒冬的外部压力相比,药物本身疗效未达临床预期才是导致公司猝死的根本原因—— 这款历经肌萎缩侧索硬化症(ALS)研发失败、转型中重度嗜酸性粒细胞性哮喘的口服小分子药物,始终未能证明其在关键临床终点的明确价值,最终在疗效短板与竞争挤压下走向终结。
Dexpramipexole 的研发史本质是一部 “疗效补救史”,但两次布局均因核心疗效不足陷入困境,暴露其分子机制与临床需求的错配:
1. 首次失败:ALS 适应症疗效微弱,未达核心终点
该药最初由 Knopp Biosciences 开发,定位为线粒体功能调节剂,用于 ALS 治疗。尽管早期 II 期试验显示 300mg 剂量组患者运动功能量表(ALSFRS-R)有剂量依赖性改善,且安全性良好,但关键 III 期临床试验未能复制这一结果 —— 不仅未达到 “显著延长患者生存期” 的主要终点,对肌力改善、疾病进展延缓等核心疗效指标也无统计学意义上的获益,最终导致渤健终止合作,ALS 适应症研发彻底停摆。这一失败已埋下伏笔:dexpramipexole 的作用机制(线粒体调节)对神经退行性疾病的干预效果有限,难以转化为临床可感知的疗效。
2. 转型受挫:哮喘适应症 “治标不治本”,疗效深度不足

转向中重度嗜酸性粒细胞性哮喘后,dexpramipexole 的核心卖点是 “口服抑制嗜酸性粒细胞成熟”,II 期 EXHALE 试验显示其能使患者血液嗜酸性粒细胞计数(AEC)降低 77%,但这一 “生物标志物改善” 未能转化为核心临床获益。从已披露的 III 期 EXHALE-4 试验初步数据来看,该药在主要终点 “肺功能 FEV1 改善率” 和次要终点 “哮喘急性发作率降低” 上,仅较安慰剂组有微弱优势,且未达到预设的统计学显著性标准;更关键的是,其对患者呼吸困难、生活质量评分等临床症状的改善作用不明显,远不及现有 IL-5/IL-5R 单克隆抗体(如美泊利珠单抗)的疗效表现。(公司原文为Areteia Therapeutics Announces Positive Topline Results from the First Phase III Study of Oral Dexpramipexole in Eosinophilic Asthma三期数据体现了积极进展)

Areteia 的未来关闭本质是 “单一管线” 与 “疗效失败” 的叠加结果。
果断关闭是利好医药行业的循环。
参考来源:
[1] 摩熵医药(原药融云)数据库
[2] https://www.businesswire.com/news/home/20250916566261/en/Areteia-Therapeutics-Announces-Positive-Topline-Results-from-the-First-Phase-III-Study-of-Oral-Dexpramipexole-in-Eosinophilic-Asthma
[3] https://www.areteiatx.com/
[4] https://www.ftchinese.com/interactive/243566
扩展阅读:
1. 甘油果糖氯化钠注射液修订说明书,新增多项不良反应!涉及企业超50家
查数据,找摩熵!想要解锁更多药企信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论