
近日,小核酸龙头Alnylam发布2023年中报:
上半年总营收6.38亿美元,同比增长46%,研发费用支持4.79亿美元,净利润亏损4.5亿美元。其中Q2单季度实现营收3.19亿美元,同比增长42%;公司预计2023年净产品收入12亿至12.85亿美元。值得注意的是公司去年获批上市的RNAi疗法Amvuttra(vutrisiran)上半年销售额反超老牌产品ONPATTRO (patisiran)。
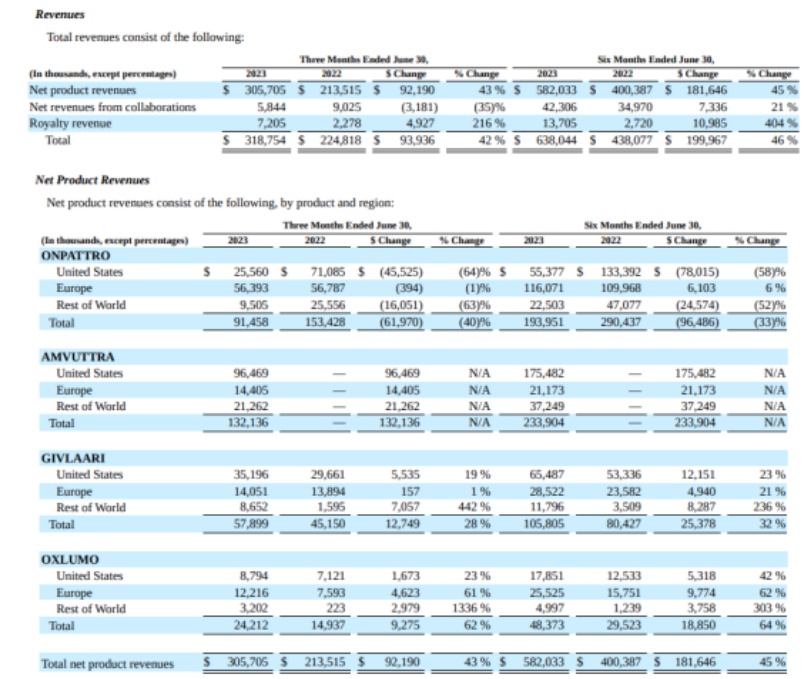
分产品来看:
核心产品ONPATTRO (patisiran)在2023H1年营收1.94亿美元,同比下降33%;2022年营收5.58亿美元,同比增长17.5%。分区域来看,美国市场和其他市场营收下降58%,欧洲增长6%。主要因为ONPATTRO的需求下降,因为正在进行的患者继续转向AMVUTTRA。与ONPATTRO相比,AMVUTTRA的制造成本较低,此外,随着全球对ONPATTRO的需求持续波动,Alnylam可能会对库存和设施进行进一步调整。
ONPATTRO是首款获得FDA批准的RNAi疗法(2018年8月获批),用于治疗由遗传性转甲状腺素蛋白淀粉样变性引起的周围神经疾病(多发性神经病)成人患者。ONPATTRO和AMVUTTRA都用于治疗转甲状腺素蛋白样变,截至2022年底,全球有超过2975名患者正在接受ONPATTRO或AMVUTTRA治疗。
除了患者继续转向AMVUTTRA以外,ONPATTRO还面临着其他公司同类产品的竞争,包括Ionis开发和销售的tafamidis和intertersen,以及处于不同临床开发阶段的候选产品,包括Ionis与阿斯利康(AstraZeneca)合作开发的另一种研究药物eplontersen,该药物在治疗hATTR淀粉样变性的多发性神经病变的3期研究中达到了共同的主要和次要终点。目前正在接受FDA的监管审查,PDUFA生效日期为2023年12月22日。最后,BridgeBio Pharma, Inc.(或BridgeBio)于2023年7月宣布其在研疗法acoramidis在治疗伴有心肌病的转甲状腺素蛋白介导的(ATTR)淀粉样变性(ATTR-CM)患者的3期临床试验中达到主要终点,显著降低患者死亡和因为心血管疾病住院的风险,并预计在今年年底之前向美国FDA递交新药申请(NDA)。
Alnylam表示虽然我们相信ONPATTRO和AMVUTTRA在治疗hATTR淀粉样变性合并多神经病变患者方面已经并将继续具有竞争力,但ONPATTRO和/或AMVUTTRA可能无法与这些产品和候选产品或其他产品竞争,因此可能无法取得商业成功。此外,积极或消极的数据和/或竞争产品的商业成功或失败可能会对我们的股票价格产生负面影响。例如,Alnylam的股票价格受到BridgeBio 3期临床试验A部分结果的负面影响。
Alnylam的另一重磅产品Amvuttra(vutrisiran)上半年营收2.34亿美元。2022年6月,美国FDA批准皮下注射RNAi疗法Amvuttra(vutrisiran)上市,用于治疗遗传性转甲状腺素蛋白介导(hATTR)的淀粉样变性成人患者的多发性神经病,同年9月获得欧盟和英国批准上市,此后在日本和巴西获得监管批准。
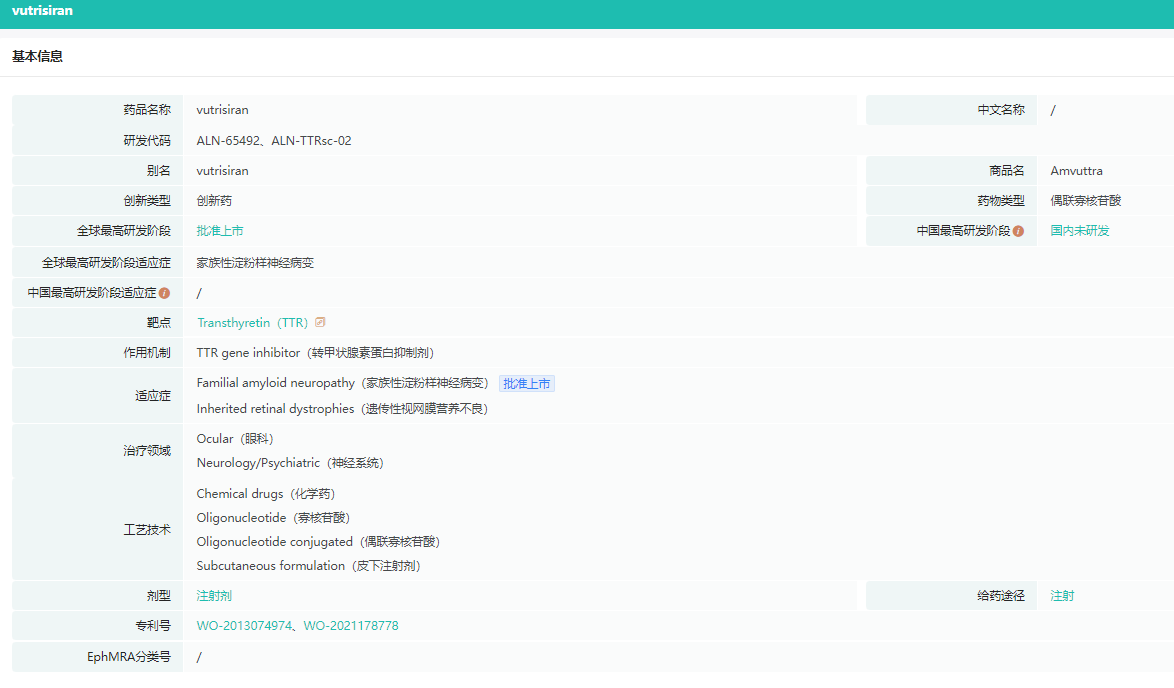
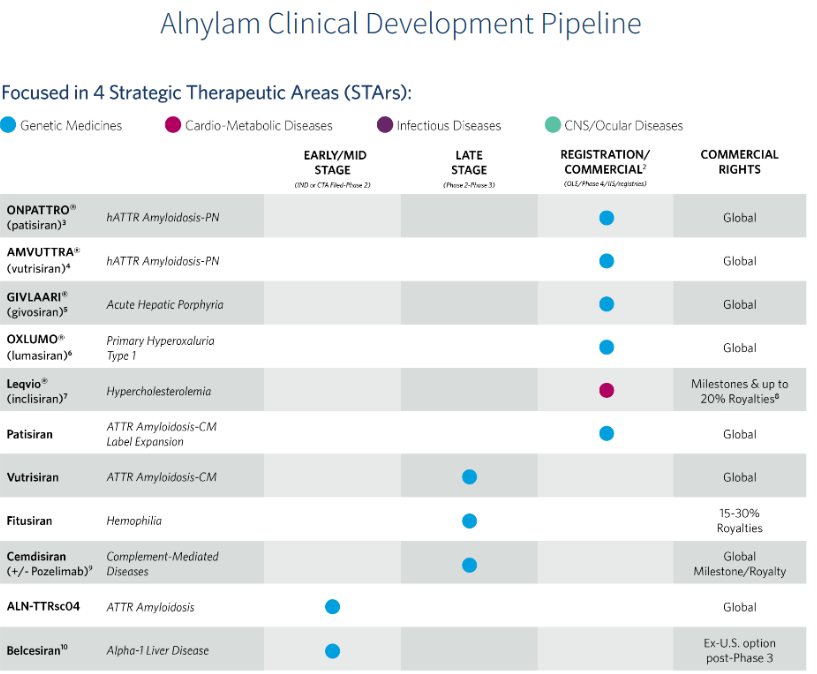
截图来源:药融云全球药物研发
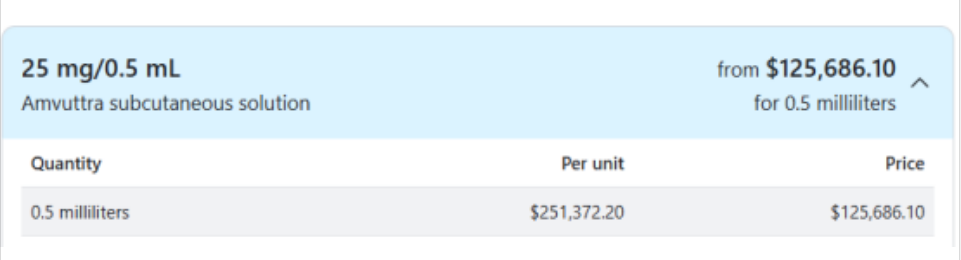
GIVLAARI (givosiran)上半年营收1.06亿美元,增长32%;主要用于治疗急性肝卟啉症(AHP),2019年获得FDA批准上市,截止目前,全球范围内已经有500多名患者在接受本品的治疗。
OXLUMO (lumasiran)上半年营收0.3亿美元,同比增长64%,2021年获得FDA批准上市,主要用于治疗1型原发性高草酸尿症(PH1),目前有280多名患者在接受本品的治疗。
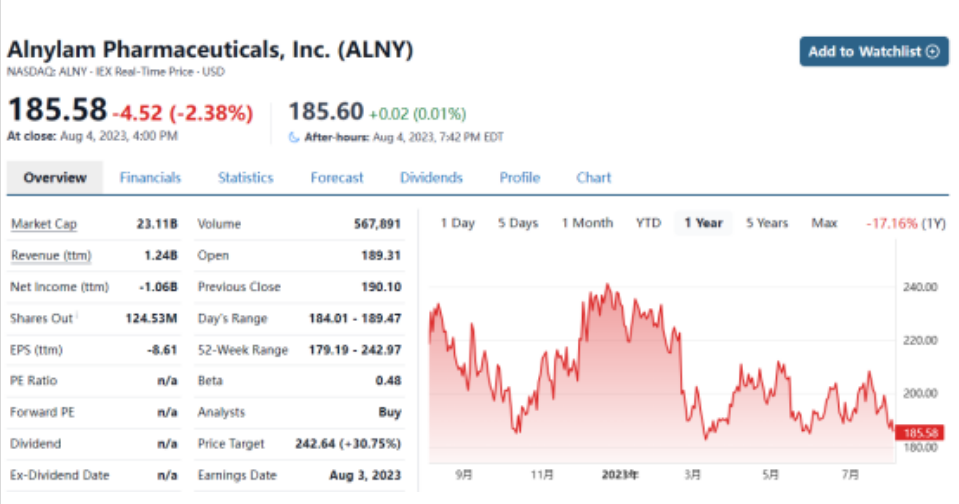
Alnylam Pharmaceuticals目前市值231亿美元左右,今年以来股价下跌17%。
在对外授权方面,除了再生元和诺华等,Alnylam近两月还获得3亿多美元的预付款。2023年7月24日,罗氏3.1亿美元预付款,引进Alnylam的AGT siRNA。2023年8月3日,Agios将向Alnylam预付1750万美元,以及获得高达1.3亿美元的潜在发展和监管里程碑付款,以获得,Alnylam一项临床前TMPRSS6 siRNA产品的独家全球许可。
总结
总的来说,小核酸药物的市场规模仍在进一步扩容,Alnylam的营收仍然保持大幅增长,主要是新品的推出一定程度上抵消了老产品的下滑以及对外授权获得版税。小核酸药物领域,国内也有不少企业布局,如圣诺制药、瑞博生物、悦康药业(2021年收购天龙药业, 布局核酸药物研发平台)等;相关上游企业有兆维生物、吉玛基因等,小核酸药物CDMO公司有锐博生物、凯莱英和药明康德等。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!




































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论