
据NMPA官网显示,扬子江药业的4类仿制化药盐酸艾司洛尔氯化钠注射液获得批准上市。

截图来源:NMPA官网
艾司洛尔原研来自Baxter Healthcare(美国百特医疗用品公司),是一种超短效心血管系统药物选择性的β1肾上腺素受体阻滞剂,被广泛用于治疗室上性快速性心律失常、急性冠脉综合征以及围手术期高血压、心动过速、心肌缺血等。
β-受体阻滞剂被广泛的使用在心脑血管及其它疾病领域中,是抗心绞痛、心衰、心律失常的一线用药,占据着医院用药较大的比例。艾司洛尔具有半衰期短、消除率高、起效迅速、无蓄积作用等优点,2015年被列入了国家出台的《急(抢)救药品直接挂网采购示范药品》。
目前国内已获批上市的产品有盐酸艾司洛尔注射液、注射用盐酸艾司洛尔和盐酸艾司洛尔氯化钠注射液,三个剂型均已被纳入2022年国家医保目录(乙类)。2022年艾司洛尔院内销售额为8.6亿元,以盐酸艾司洛尔注射液为主力品种,企业方面则是齐鲁制药市场份额最高(93.7%)。
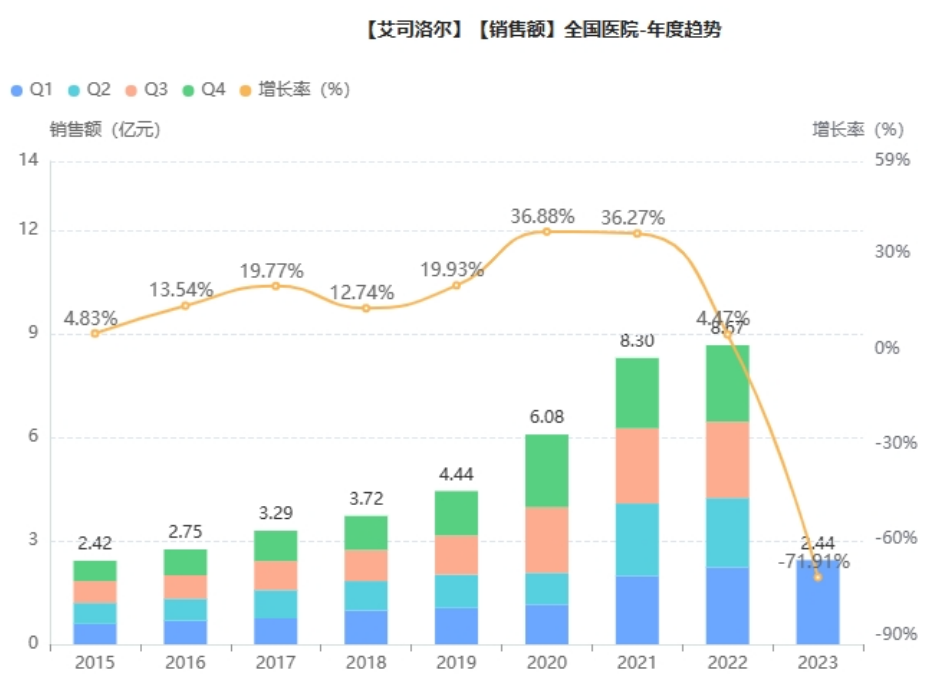
截图来源:药融云全国医院销售数据库
目前盐酸艾司洛尔注射液已经有5家过评,2023年8月28日确定入选了第九批国采。
此前国内仅有上海百特一家企业拥有盐酸艾司洛尔氯化钠注射液批文,且已通过一致性评价。此次扬子江为第2家获批+过评该品种的药企。
至此,扬子江药业今年已有24个品种(27品规)过评,其中头孢克洛缓释片(Ⅱ)、氨氯地平贝那普利胶囊、瑞戈非尼片和盐酸奈康唑乳膏均为首家过评品种。
在心血管系统用药领域,扬子江已有超30个品种获批,其中氨氯地平贝那普利胶囊、氨氯地平贝那普利片(Ⅰ)、盐酸索他洛尔注射液和非诺贝特缓释片均为独家品种。氨氯地平贝那普利片(Ⅰ)近两年院内销售额更是达4亿+,且6月初,扬子江才最新斩获了该品种的胶囊剂型首仿。
此外,扬子江药业还递交了ω-3脂肪酸乙酯90软胶囊的仿制上市申请。目前该品种仅有2家国产+1家进口拥有批文,市场竞争较为缓和。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论