
2023年10月是君实生物的高光时刻,首款国产 PD-1 单抗获 FDA 批准,国际化战略实现重大突破。
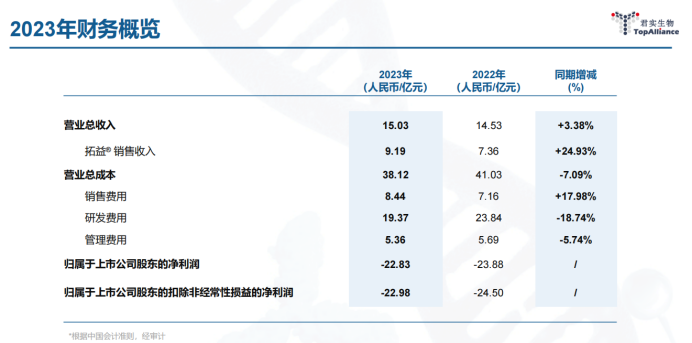
近日,君实生物(688180)发布2023年报:2023年,公司实现营业收入15.03亿元,同比增长 3.38%,主要由于药品销售收入增加,归母净利润为-22.83亿元,去年研发费用支出19.37亿,同比减少18.74%,主要系本期公司加强了各项费用的管控,优化资源配置,聚焦更有潜力的研发管线。

产品销售和公司经营情况
1、特瑞普利单抗收入为9.91亿元,同比增长25%,获FDA批准于美国上市。2024 年起,拓益新增 3 项适应症纳入新版国家医保目录,目前共有 6 项适应症纳入国家医保目录,是国家医保目录中唯一用于治疗黑色素瘤的抗 PD-1 单抗药物。截止去年底,拓益已累计在全国超过五千家医疗机构及约两千家专业药房及社会药房销售。
(推荐阅读:特瑞普利单抗联合疗法有望治疗恶性黏膜黑色素瘤)
2024年1月,公司合作伙伴Coherus宣布特瑞普利单抗正式在美国市场进行商业化销售。根据公司官网,特瑞普利单抗是首个获FDA批准上市的中国自主研发和生产的创新生物药,是首个且唯一在美国获批用于鼻咽癌治疗的药物。此外,公司持续探索特瑞普利单抗在海外的上市申报,英国、欧盟、澳大利亚均受理了特瑞普利单抗的上市申请。同时,公司通过与Coherus、Hikma、Rxilient、Dr. Reddy’s达成商业化协议,拓展全球商业化网络,助力特瑞普利单抗海外销售放量。

2、公司新增一款商业化药品氢溴酸氘瑞米德韦片(商品名:民得维)并纳入国家医保目录,已进入超过2300家医院。
3、Tifcemalimab联合特瑞普利单抗III期临床研究的IND申请分别获得FDA及NMPA批准。
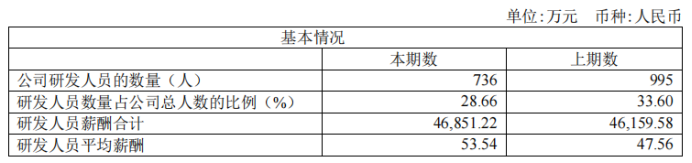
研发人员及薪酬情况
截至2023年底,公司拥有 2,568 名员工,其中 736 名员工负责药物研发,952 名员工负责产品商业化,562 名员工负责生产,其余员工负责财务、行政、IT、人力资源等支持性工作。截止2023年底,公司有研发人员736名,相对去年995人,减少259人。2023年研发人员平均薪酬53.54万元,相比上年47.56万元,涨幅12.56%。
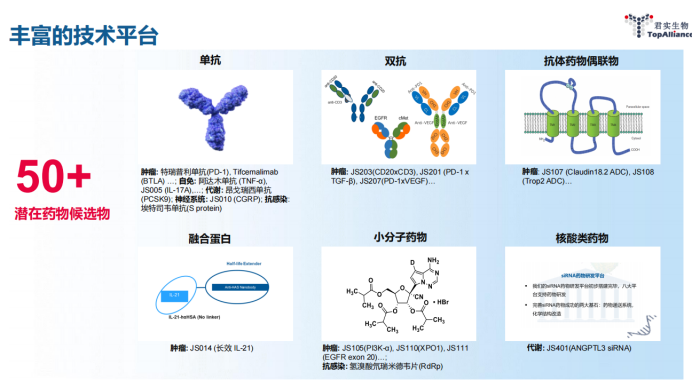
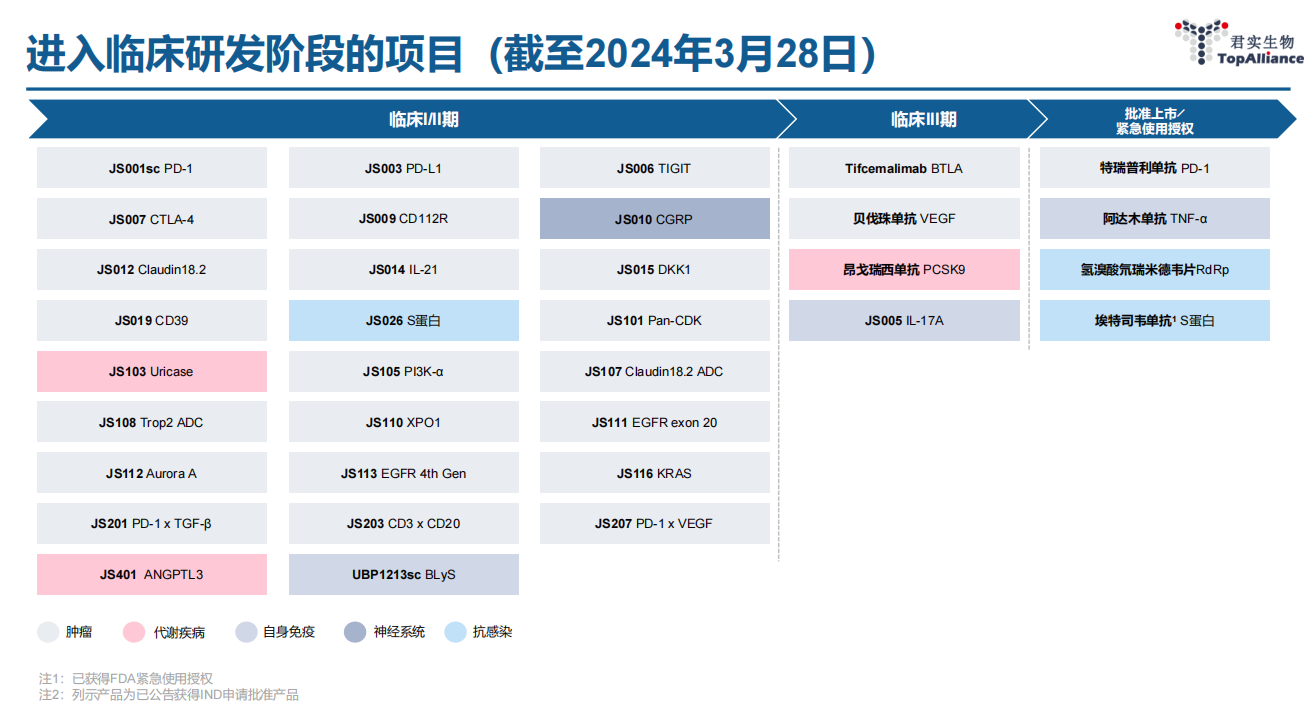
技术平台和管线
公司已建立全球一体化的研发流程,并于美国的旧金山、马里兰以及国内的上海及苏州都设有研发中心。公司建立了涵盖蛋白药物从早期研发到产业化的整个生命周期的完整技术体系,该体系包括多个技术平台:(1)抗体筛选及功能测定的自动化高效筛选平台、(2)人体膜受体蛋白组库和高通量筛选平台、(3)抗体人源化及构建平台、(4)高产稳定表达细胞株筛选构建平台、(5)CHO 细胞发酵工艺开发平台、(6)抗体纯化工艺及制剂工艺开发与配方优化平台、(7)抗体质量研究、控制及保证平台、(8)抗体偶联药研发平台、(9)siRNA 药物研发平台、(10)TwoGATE™。
商业化产能支持业务扩张
公司拥有 2 个商业化生产基地,苏州吴江生产基地和上海临港生产基地均已获得 NMPA 颁发的 GMP 证书,开展生物产品的商业化生产。苏州吴江生产基地拥有 4,500 升(9*500 升)发酵能力,于 2023 年 5 月顺利通过 FDA 许可前检查(Pre-License Inspection,PLI),现阶段美国商业化批次特瑞普利单抗由该生产基地负责生产。上海临港生产基地目前产能 42,000 升(21*2,000 升)。NMPA已批准上海临港生产基地可与苏州吴江生产基地同时生产商业化批次的特瑞普利单抗注射液。由于规模效应,上海临港生产基地产能的扩充亦将为公司带来更具竞争力的生产成本优势,并支持更多在研项目的临床试验用药以及未来的商业化批次生产。
总结
目前君实生物的药品销售收入尚不能完全覆盖研发费用,还属于没有实现盈利的Biotech,但是随着公司核心产品特瑞普利单抗持续拓展适应症以及海外商业化实现突破,以及阿达木单抗、氢溴酸氘瑞米德韦上市后贡献增量,再加上后续PCSK9单抗上市申请已获NMPA受理,IL-17A单抗和BTLA单抗进入临床临床III期阶段陆续推进并逐步进入商业化,未来盈利可期。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论