
2月5日,据CDE官网发布,君实生物申报的1类新药AWT020注射用无菌粉末已获得临床批件,旨在用于治疗晚期恶性肿瘤。据悉,AWT020是一款抗PD-1/IL-2c融合蛋白,具有创新的双靶点设计。
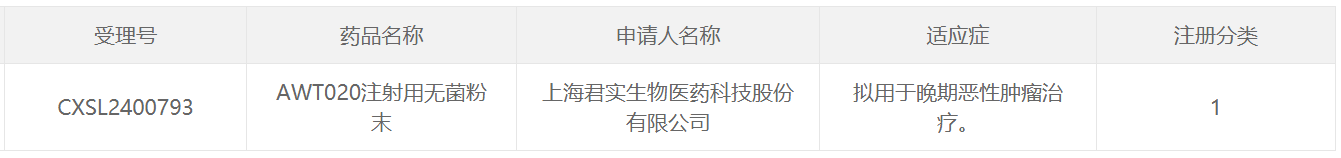
截图来源:CDE
AWT020(aPD1-IL-2c)源自Anwita Biosciences公司的研发管线,目前已在澳大利亚进入1期临床研究阶段。君实生物与Anwita Biosciences的合作始于2020年9月,双方就IL-2系列产品及相关技术在大中华区的独占许可达成协议。此外,双方还在共同开发包括Exenokine-21(JS014,长效IL-21纳米抗体融合蛋白)在内的其他产品。
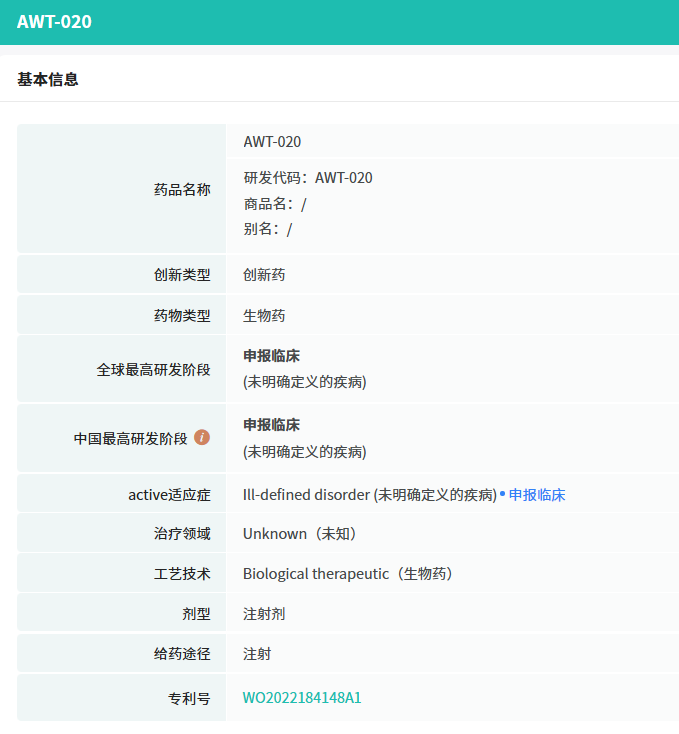
截图来源:摩熵医药数据库(全球药物研发数据库)
白细胞介素2(IL-2)作为肿瘤免疫治疗的关键免疫激动剂,在多种癌症治疗中展现出疗效,但其多效性也带来了副作用和免疫抑制问题。为了克服这一挑战,并结合PD-1阻断疗法的安全性优势,研究人员创新性地设计了AWT020这一双功能融合蛋白。AWT020由抗PD-1抗体与效价优化的IL-2突变蛋白组成,旨在充分利用两者的互补抗肿瘤活性。

截图来源:摩熵医药全球药物研发数据库
AWT020中的IL-2成分经过设计,具有低全身毒性,而抗PD-1抗体成分则能阻断PD-1和PD-L1的相互作用,同时选择性地将IL-2递送到肿瘤微环境中的PD-1阳性T细胞。在临床前研究中,AWT020表现出良好的单药抗肿瘤活性,具有强大的免疫记忆,并能优先激活和扩增肿瘤内的功能性T细胞。此外,在非人类灵长类动物实验中,AWT020在支持临床计划的剂量水平下表现出良好的耐受性。
根据Anwita官网及公开资料,AWT020拟开发的适应症包括抗PD-1难治性非小细胞肺癌、肾细胞癌、黑色素瘤和尿路上皮癌等。目前,Anwita Biosciences正在澳大利亚进行AWT020的1/2期首次人体临床研究,以评估其安全性、药代动力学和药效学。
此次AWT020在中国获批临床,标志着这款创新药物即将在中国开展临床研究,为晚期恶性肿瘤患者带来新的治疗希望。君实生物与Anwita Biosciences的合作将继续深化,共同推动这一创新药物的研发进程。
参考来源:
[1] CDE官网
[2] 摩熵医药(原药融云)数据库
[3] Anwita官网
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论