
3月19日,葛兰素史克宣布,美国FDA已批准利奈昔巴特(Linerixibat)上市,用于治疗原发性胆汁性胆管炎(PBC)成人患者的胆汁淤积性瘙痒。新闻稿指出,这是首个在美国获批治疗该适应症的药物, 代表着PBC瘙痒治疗领域的一个重要里程碑。
一、填补临床空白,直面89%患者的“无形之痒”
原发性胆汁性胆管炎(PBC)是一种胆汁淤积性肝病,其特征是肝脏内胆汁流动受阻。在此过程中过度积累的胆汁酸被认为是引发胆汁淤积性瘙痒的关键因素,这种源自体内的瘙痒感无法通过抓挠缓解,严重困扰患者。
瘙痒可能出现在PBC病程的任何阶段,甚至在生化指标得到控制后仍可持续存在。据统计,约89%的PBC患者会经历不同程度、严重影响生活质量的瘙痒。然而,现有的一线治疗药物仅能使约70%的患者病情得到控制,对瘙痒症状的缓解作用有限,临床存在显著的未满足需求。
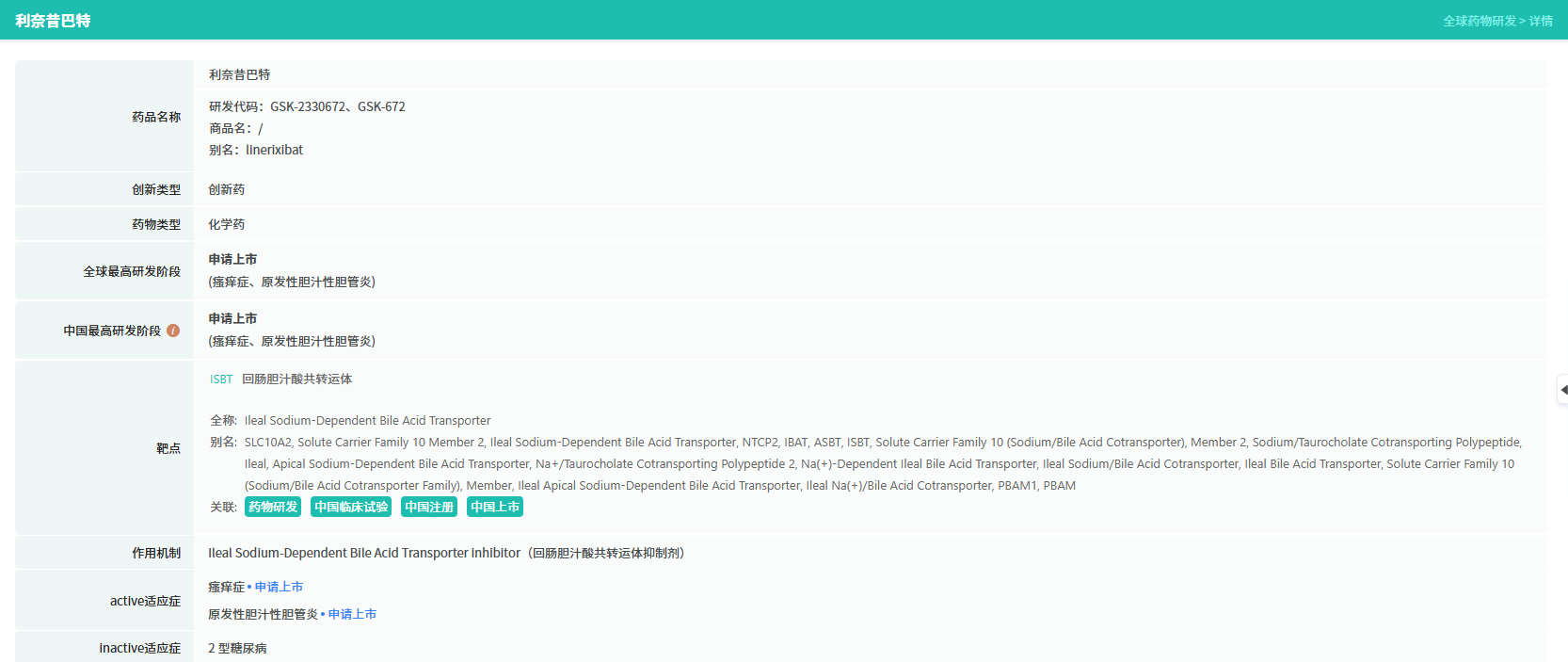
查数据,找摩熵!图源:摩熵医药数据库-全球药物研发数据库
利奈昔巴特是一种口服的回肠胆汁酸转运蛋白(IBAT)抑制剂。其作用机制在于抑制肠道内胆汁酸的再摄取,从而降低全身血液循环中与瘙痒相关的多种介质水平,从源头针对性干预瘙痒的发生。
二、III期临床数据支撑,全球多国上市申请同步推进
本次FDA的批准,主要基于关键III期临床试验GLISTEN的积极结果。GLISTEN是一项双盲、随机、安慰剂对照的III期研究,旨在评估利奈昔巴特治疗PBC患者胆汁淤积性瘙痒的疗效与安全性。试验的主要终点是评估在24周治疗期内,患者每月瘙痒评分(基于数值评定量表NRS)相对于基线的平均变化。
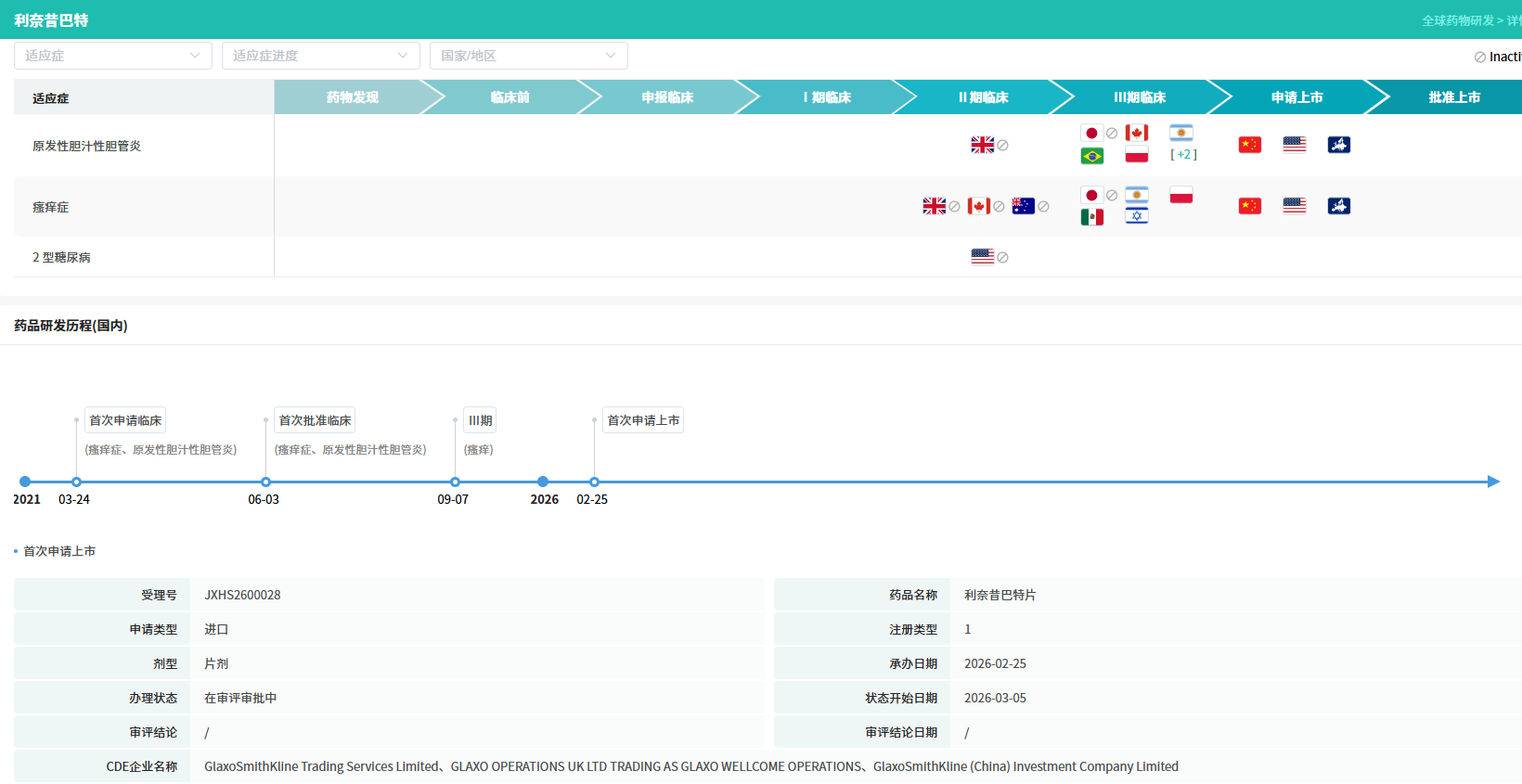
查数据,找摩熵!图源:摩熵医药-全球药物研发数据库
除了在美国获批,利奈昔巴特在欧盟、英国、加拿大和中国的上市许可申请也已提交,正在审评过程中,显示其全球同步开发的布局。
值得注意的是,就在本月上旬(3月9日),GSK宣布与Alfasigma S.p.A.公司达成一项许可协议,将利奈昔巴特的全球独家开发、生产和商业化权利授予后者。此项交易目前仍在进行中,预示着该产品未来的商业化将可能由合作伙伴主导推进。
三、结语
利奈昔巴特在美国的成功获批,终结了PBC胆汁淤积性瘙痒长期缺乏针对性疗法的历史,为饱受瘙痒困扰的大量患者提供了新的治疗选择。其基于明确机制的创新作用路径,以及在全球主要市场的同步申报,不仅展现了GSK在特定疾病领域深挖临床需求的研发策略,也预示着未来在肝病并发症治疗市场的竞争将更加聚焦于改善患者核心症状与生活质量。随着该产品在全球更多地区获批上市,有望重塑PBC的全程管理格局。
参考来源:
[1] 企业官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. GSK全球首创口服抗生素Gepotidacin新适应症获FDA批准!双重阻断机制为淋病治疗带来曙光
2. GSK以3.6亿美元布局!获Syndivia新型前列腺癌ADC全球独家权,扩张肿瘤治疗新版图
3. GSK抗体偶联药Blenrep获批!成全球首个BCMA ADC新药,多发性骨髓瘤治疗现曙光
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论