
当我们翻开人类抗击传染病的历史长卷,在过去四十余年间,人类在对抗艾滋病(AIDS)的战役中,书写了一部充满遗憾、纷争与最终迎来破局的史诗。在这个过程中,科学的火花不断碰撞,抗病毒药物经历了从无到有、从单药到鸡尾酒疗法、再到今天以必妥维(Biktarvy)为代表的极致复方制剂的惊人跨越。
一、溯源黑匣:从“世纪绝症”到诺贝尔奖的风波角力
将时钟拨回1981年,美国疾病控制与预防中心(CDC)首次向世人公开了一个令人毛骨悚然的罕见病例报告:5名男同性恋者感染了卡氏肺囊虫肺炎,且伴随免疫系统的全面崩溃。这份报告发布时,已有2人离世,不久后剩余3人也未能幸免。到1981年底,此类病例急速攀升至270例,并在次年突破了特定群体的界限,CDC正式为其定名为“获得性免疫缺陷综合征(AIDS)”,也就是我们熟知的艾滋病。
面对这只从潘多拉魔盒中逃出的猛兽,寻找病原体成为了全球医学界的头等大事。这里面,上演了一出充满学术争议与大国博弈的戏码。
起初,美国国立卫生研究院(NIH)的罗伯特·加罗(Robert C. Gallo)将嫌疑锁定在了他自己于1980年发现的人体T细胞白血病病毒(HTLV)上。他甚至给出了严密的逻辑闭环:过滤后的血液仍能传播(证明是病毒)、传播途径吻合、动物感染后有类似免疫衰弱症状,且HTLV同样攻击表面带有CD4抗原的T细胞。加罗据此分离出了HTLV-1和HTLV-2。

与此同时,在大洋彼岸的1983年初,法国巴斯德研究所的吕克·蒙塔尼耶(Luc Montagnier)团队从一名淋巴结肿大患者身上分离出了一种全新的逆转录病毒,暂命名为LAV,并将其成果发表于《科学》杂志。紧接着的1984年,加罗团队也在《科学》上连发四文,宣布分离出导致艾滋病的新型逆转录病毒HTLV-3,并成功建立了可在体外连续培养的细胞株(这在蒙塔尼耶的研究中未能实现),为后续的血液检测奠定了关键基础。
戏剧性的是,加罗迅速用HTLV-3申请了专利,这直接惹怒了曾与他共享过LAV病毒样本的蒙塔尼耶。1985年,巴斯德研究所将NIH告上法庭,蒙塔尼耶坚称加罗的HTLV-3就是自己赠送的LAV,是加罗实验室发生了样本污染;加罗则反唇相讥,说是蒙塔尼耶搞混了样本。这场纷争甚至惊动了美法两国最高层,1987年里根总统与法国总理希拉克出面才达成协议。后续长达多年的调查最终证明,两家实验室都发生了样本污染,而加罗用于申请专利的HTLV-3确实带有法国样本的影子,但并无蓄意盗窃之嫌。为了平息争议,科学界将该病毒统一更名为HIV。2008年,诺贝尔生理学或医学奖颁给了蒙塔尼耶等人,加罗遗憾落选,引发了百余位科学家的联名鸣不平。
HIV颗粒的结构
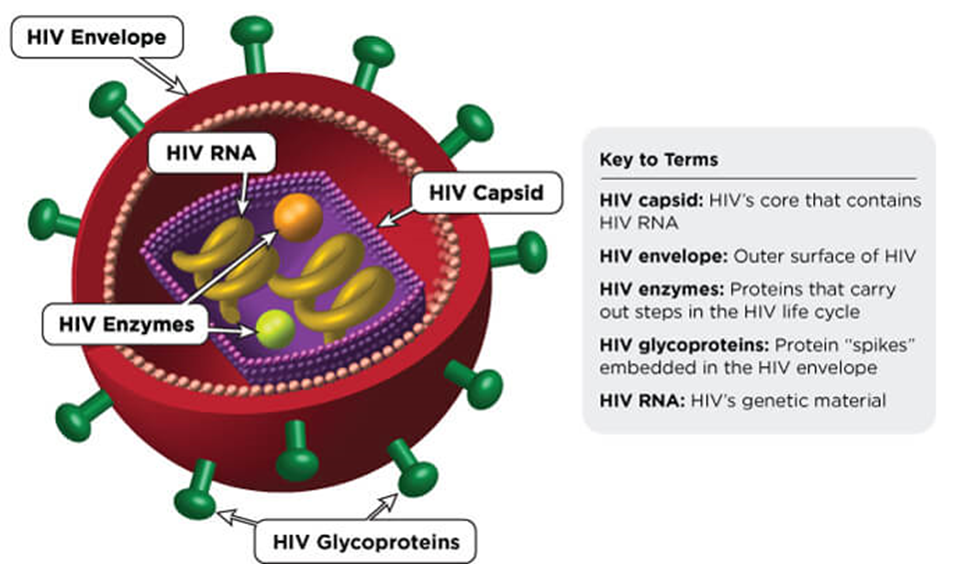
时至今日,这场战役仍未结束。根据WHO的数据,艾滋病已累计夺走约4040万人的生命。截至2022年底,全球仍有约3900万名感染者,当年新增感染130万人,死亡63万人。这些沉甸甸的数据,正是医药产业不断突破的终极动力。
二、破冰前行:疫苗折戟与抗逆转录病毒药物的突围
在彻底看清HIV的真面目后,人类最初寄希望于“一劳永逸”的疫苗。然而,HIV极不稳定的逆转录过程导致其变异极快,让疫苗研发步履维艰。
- 第一代疫苗:VaxGen公司的AIDSVax试图利用HIV包膜糖蛋白诱导体液免疫,宣告失败。
- 第二代疫苗:默沙东尝试用5型腺病毒载体激发T细胞免疫,结果反而增加了感染风险。
- 第三代疫苗:旨在同时激发体液与细胞免疫的RV144疫苗,在接种初期能降低60%风险,但3.5年后效力跌至31.2%,无法推广。至今,全球仍无艾滋病疫苗获批。
所幸,“东方不亮西方亮”,治疗药物领域迎来了曙光。1987年3月13日,齐多夫定在欧盟获批上市,3月19日,于美国获批上市,首个艾滋病治疗药物由此诞生。齐多夫定属于胸腺嘧啶脱氧核苷的叠氮类似物,其结构是将胸腺嘧啶脱氧核苷上的3-羟基转化为叠氮基团,具体结构式如下:
齐多夫定(左)和胸腺嘧啶脱氧核苷(右)的化学结构式
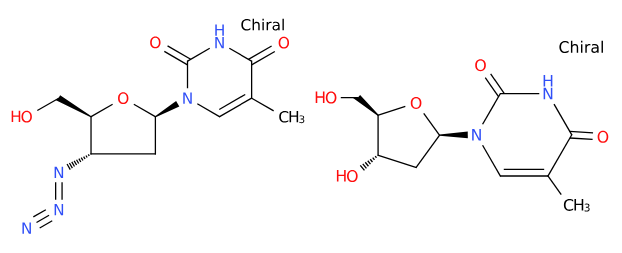
有趣的是,这原本是1964年合成用于抗肿瘤却因效果不佳被搁置的“失败品”。科学家发现它能插入DNA抑制病毒,其独特的结构(脱氧核糖环3位的叠氮基取代了羟基)终止了病毒RNA在宿主DNA上的复制。齐多夫定开启了核苷类逆转录酶抑制剂(NRTI)的时代。
然而,单靠NRTI极易产生耐药性。随着1989年HIV蛋白酶结构被解析,基于结构设计的蛋白酶抑制剂(如沙奎那韦、利托那韦)于1995-1996年相继问世,显著提升了患者的CD4细胞计数。紧接着,非核苷类逆转录酶抑制剂(NNRTI,如奈韦拉平)也于1996年获批。
正是在1996年,美籍华人何大一博士提出了“高效抗逆转录病毒治疗”(HAART),即闻名遐迩的“鸡尾酒疗法”。通过将NRTI“骨干”与另一类抗HIV“核心”药物联合,最大程度遏制病毒复制,艾滋病从此由“绝症”转变为可控的慢性病。
但这远非终点。早期鸡尾酒疗法的药物依从性差、耐药屏障低且副作用明显。直到2007年,全新机制的HIV整合酶抑制剂(INSTI)——拉替拉韦获批,改变了游戏规则。整合酶负责将病毒cDNA整合进宿主染色体,且在人体细胞内无类似物,这赋予了INSTI得天独厚的安全性优势。抗艾药物进入了高歌猛进的新纪元。
HIV复制生命周期
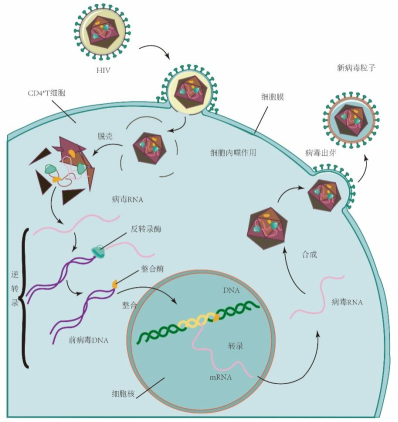
三、巅峰淬炼:必妥维(Biktarvy)的极致分子设计与临床验证
在抗艾领域,吉利德科学公司(Gilead Sciences)无疑是绝对的霸主。从2001年的富马酸替诺福韦二吡呋酯到2003年的恩曲他滨,吉利德深刻洞察到患者每天吞咽大量药片的痛苦。2006年,他们推出了首款三合一复方Atripla,随后不断迭代出Complera(2011年)和首次引入整合酶抑制剂的STRIBILD(2012年)。
而吉利德的终极王牌,是一种名为比克替拉韦(Bictegravir, BIC)的新型整合酶抑制剂。
比克替拉韦化学结构式
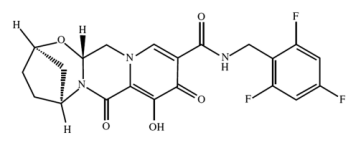
2014年,比克替拉韦进入I期临床。在体外试验中,它展现出了惊人的效力:
- 强效抑制:能够极其高效地抑制纯化重组HIV-1整合酶的链转移和3’端加工活性(IC50分别低至7.5nM和241nM)。
- 超高选择性:在淋巴细胞和巨噬细胞中的选择性指数高达上千至近万倍,意味着它对病毒极度致命,对人体细胞却非常温和。
- 极高耐药屏障:面对拉替拉韦和艾维雷韦耐药的突变株,比克替拉韦依然强效,其耐药屏障与多替拉韦相当,且在突破性耐药研究中表现出临床相关浓度下的高不可攀。
- 优异的药代动力学:口服1.8小时即达峰,半衰期达17.8小时,非常适合每日一次给药。
2015年末至2017年,吉利德豪掷千金,同时启动了5项庞大的Ⅲ期临床试验(涵盖初治、经治、女性、青少年等全场景),将必妥维(比克替拉韦+恩曲他滨+丙酚替诺福韦的终极三联复方)推上擂台。
临床数据堪称“碾压局”:
- 在初治患者的GS-US-380-1490和1489研究中,必妥维在48周时的病毒抑制率高达89%和92.4%,与多替拉韦方案不相上下(非劣效)。
- 在已实现病毒抑制的转换治疗研究(1844和1878)中,换用必妥维后,94%和92%的患者维持了病毒抑制,同样证明非劣效。
- 在安全性上,恶心等不良反应发生率(5%)显著低于含多替拉韦的对照组(17%)。
凭借这组无懈可击的数据,2018年2月7日,FDA正式批准必妥维(Biktarvy)上市。
四、商业传奇:重塑百亿市场格局的王座更迭
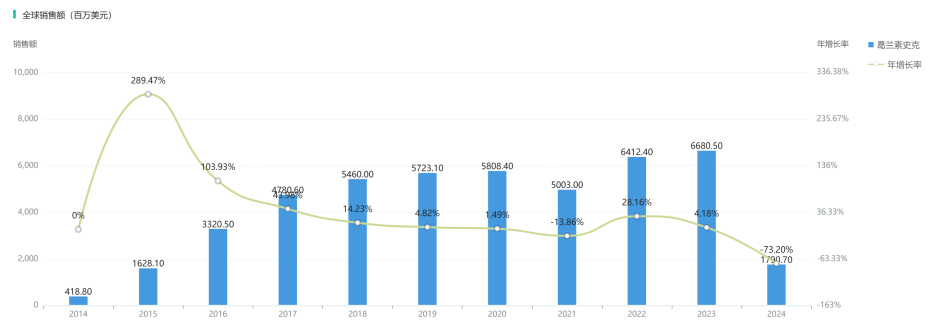
在必妥维问世之前,市场是属于ViiV Healthcare公司的绥美凯(多替拉韦/拉米夫定/阿巴卡韦),于2014年上市,上市次年,销售额便突破10亿美元,成为一款重磅药物。
绥美凯历年销售额
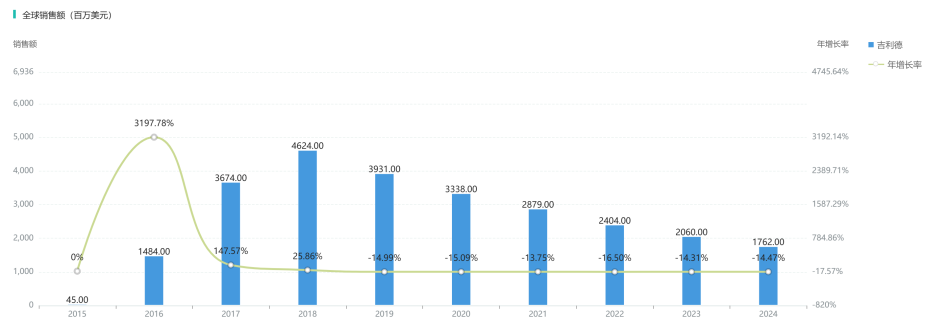
和吉利德自家的捷扶康(丙酚替诺福韦/恩曲他滨/考比司他/艾维雷韦),于2015年上市。
捷扶康历年销售额
但捷扶康存在诸多不足,例如需随餐服用、易受其他药物干扰、耐药屏障较低以及可能引发血脂异常等问题,长期以来饱受广大患者诟病。
2018年,历史的交接棒落在了必妥维手中。它之所以能上市即成爆款,得益于对竞品的降维打击:
① 极小的副作用:恶心发生率远低于多替拉韦方案。
② 无可挑剔的耐药屏障:体外研究证实其优于初代的整合酶抑制剂。
③ 极致的单片体积:必妥维每片仅重275mg,而绥美凯重达950mg,捷扶康为510mg。这种每日吞服一颗小药丸的便利性,极大提升了患者的依从性。
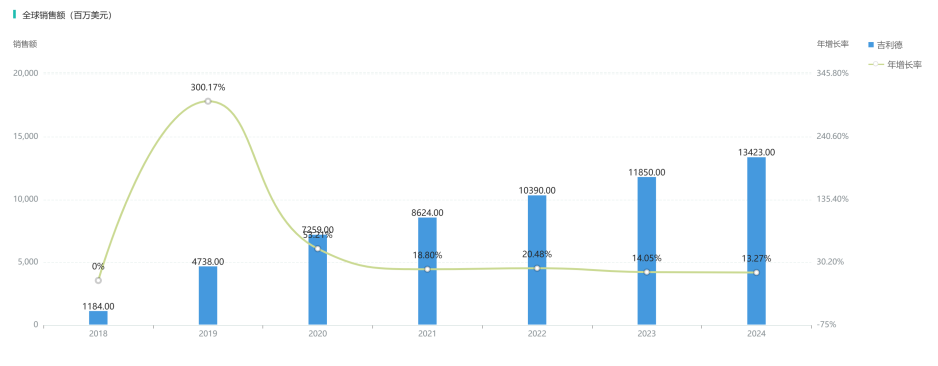
市场用真金白银做出了投票。上市次年,必妥维销售额狂飙至47亿美元以上,更是在2022年强势突破100亿美元大关,成为艾滋病治疗领域无可争议的标志性重磅药物。
必妥维历年销售额
























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论