注:本文不构成任何投资意见和建议,以官方/公司公告为准;本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及)。因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。
近日,上海湃隆生物和英国Exscientia共同宣布,扩大双方在人工智能新药研发方面的合作,联合开发包括特异性CDK7抑制剂在内的多个针对CDK的抗肿瘤新药。这也是湃隆生物成立两年来第一次对外公布在研管线靶点。那么,我们来看一看CDK7抑制剂的特点和最新药物开发进展。
CDK抑制剂是抗肿瘤新药研发热点
细胞周期蛋白依赖性激酶(CDK),作为参与细胞周期调节的关键激酶,围绕该家族的抑制剂开发,成为近年来肿瘤领域药物开发的重要分支。作为近年来最具有代表性的靶向药物之一,CDK4/6抑制剂的吸金程度不亚于PD-1抑制剂。2020年,三大CDK4/6抑制剂全球销售额70亿美元(辉瑞的哌柏西利销售额已经突破50亿美元大关,诺华的瑞波西利销售额约7亿美元,礼来的阿贝西利销售额达9亿美元)。
CDK抑制剂研发颇具挑战性
CDK是丝氨酸/苏氨酸蛋白激酶,可调节细胞周期进程(CDK 1-6和14-18)或转录(CDK 7-13和19-20)。几乎所有的CDK激活都通过:(1)与细胞周期蛋白(Cyclin)结合;(2)T-Loop被CDK激活激酶(CDK Activating Kinase, CAK)磷酸化。由于CDK家族靶点众多,如何选择作用靶点,根据靶点设计出具有生物活性的化学结构,并且化合物在进入临床阶段后,仍对某些类型肿瘤表现出高选择性和强抑制效果,是该领域面临的困难与挑战。第一代CDK抑制剂表现出的广谱和非选择性使其止步于临床试验。与第一代CDK抑制剂相比,第二代CDK抑制剂注重于提高某个或某几个CDK的特异选择性。除了可逆ATP竞争/非竞争抑制剂,近些年还发展了共价结合形式的不可逆ATP竞争抑制剂、可逆/不可逆的变构抑制剂、CDK降解等多种途径的药物开发,为该领域的药物发现提供了众多进展性的思路。
CDK7抑制剂最新药物开发进展
CDK7的独特之处在于其同时涉及转录与细胞周期的调控,在许多类型的癌症中异常过表达,并与侵袭性临床病理特征和不良预后相关。几种选择性的CDK7抑制剂在许多临床前模型中(AML、肝癌、胃癌、宫颈癌、胰腺癌、结直肠癌、神经母细胞瘤、前列腺癌、非小细胞肺癌以及SOX-2扩增的肺鳞状细胞癌等)显示出有希望的抗癌活性,并进入临床试验阶段。其中包括吡唑并嘧啶衍生物,BS-181和ICEC0942(CT7001),以及吡唑三嗪衍生物,LDC4297和QS1189,这些I型抑制剂可逆地结合在CDK7的ATP结合位点。ATP竞争的CDK7共价抑制剂也被开发出来,包括THZ1、 SY-1365以及吡咯烷并吡唑为基础的YKL-5-124等。
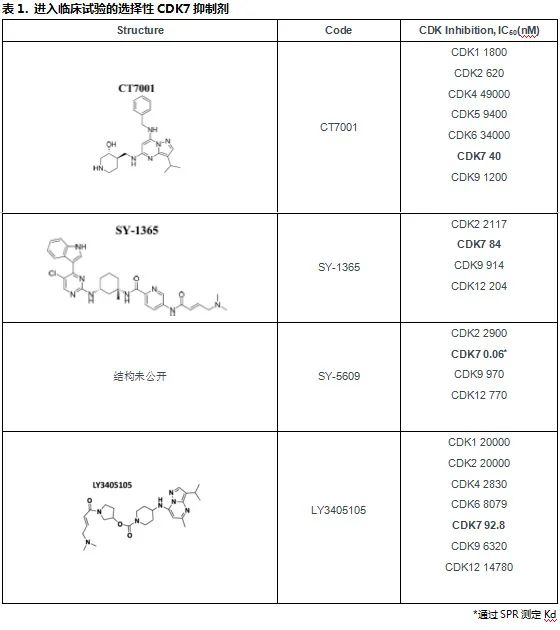
跟CDK4/6抑制剂开发过程类似(CDK4/6抑制剂上市前其实已有20年的研发历史,辉瑞2009年临床二期之前大家都持观望态度),这些选择性CDK7抑制剂临床候选化合物的开发过程并非一帆风顺。2017年11月,Carrick Therapeutics将CT7001推入1期临床, Clinical Trails上最新一次更新在2021年7月,状态为“进行中,未招募患者”。SY-1365,临床前研究表明,它可降低癌症驱动转录因子的表达水平,1期临床试验亦显示,接受了该药物治疗的部分晚期癌症患者病情保持稳定。2019年10月,Syros Pharmaceuticals宣布停止注射CDK7抑制剂SY-1365的进一步开发,优先开发高选择性的口服CDK7抑制剂SY-5609。
2020年10月,Syros在ENA会议上公布了SY-5609在晚期乳腺癌、结直肠癌、肺癌、卵巢癌、胰腺癌或其他Rb通路改变的实体瘤患者中进行的多中心、开放标记、剂量爬坡研究的1期临床试验初步数据。受试者中17名患者,符合安全性、PK和PD分析的条件。患者要么每天连续服用1、3、4或5 mg的单药SY-5609,要么连续服用3 mg的SY-5609与氟维司群联合治疗3周。参与研究的患者的中位年龄为64岁,接受了中位4线的既往治疗。SY-5609显示POLR2A mRNA表达呈剂量依赖性增加,这是一种用于检测CDK7生物活性的PD标记物。3 mg剂量组的患者POLR2A的增加达到了与临床前模型中的肿瘤消退相关的水平,以及与CDK7靶点结合的水平。无论是单一给药还是作为联合给药,PK都与剂量成正比,多次给药的蓄积较少,稳态血药浓度和半衰期适合每日一次给药。SY-5609单药不良反应多为低度,最常见的不良反应是恶心、腹泻、疲劳、血小板减少和呕吐。每日连续给药的MTD为3 mg。SY-5609与氟维司群联合用药的安全性与SY-5609单药一致。单药SY-5609治疗的13例患者中,5例可评价疗效,其中3例病情稳定,2例病情进展;在联合队列治疗的4名患者中,有1名患者的反应可评估,且病情进展。可见,SY-5609在1期临床中展现出了早期疗效的信号,但较窄的治疗窗限制了其给药剂量,Syros正在探索修改给药频率的临床试验方案。
2021年01月26日,Lilly将CDK7抑制剂LY-3405105从其研发管线中移除,官网肿瘤管线也看不到该项目的信息。苏州信诺维最新公开的CDK7抑制剂专利WO2021121390,其结构参照礼来的专利,区别仅仅是五并六元环的C/N替换。目前并不清楚二者的研发进展。
2021年1月27日,Exelixis的CDK7共价抑制剂XL-102临床试验在ClinicalTrails登记,适应症为晚期实体瘤或者转移性实体瘤,临床将扩展到卵巢癌、乳腺癌与前列腺癌。Exelixis在2019年与Aurigene签订了合作协议,并支付1750万美元首付款,以获得多至6个项目的独家许可合作。2020年底,Exelixis再支付1200万美元现金,以及未来潜在高达4.3亿美元的里程碑和销售提成获得了XL-102的独家许可。
综上所述,CDK7抑制剂具有治疗多种难治肿瘤适应症的巨大商业潜力,也同时面临如何提高治疗窗的巨大挑战。
湃隆生物在2021年7月21日的最新发布中提到“高效、高选择性、非共价的 CDK7 抑制剂在卵巢癌患者的原代组织样本中,展现出增强的肿瘤细胞毒性以及在肿瘤微环境中对免疫细胞的选择性”,不禁让我们猜想其分子可能具有某些和以上分子不同的独特性质或不同的结合位点,可以扩大治疗窗,让我们拭目以待未来有更多数据对外披露。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论