
引言
2022年5月10日,药审中心承办了齐鲁制药有限公司和Arbutus Biopharma Corporation提交的1类生物制品AB-729注射液的临床申请。该药为一款针对乙肝的RNAi疗法!Arbutus原研,齐鲁制药花2.8亿元引进,获得其在大中华区的开发和商业化权益。
(图源:CDE官网)
关于AB-729注射液
据药融云数据库显示,AB-729注射液是Arbutus Biopharma研发的针对乙肝(HBV)的皮下递送RNAi疗法,采用了Arbutus的新型共价偶联N-乙酰半乳糖胺(GalNAc)递送技术靶向肝细胞。RNAi(RNA干扰)即通过小分子双链RNA干扰目标基因的表达,抑制特定蛋白质的产生,是21世纪分子生物学领域最重要的突破之一。通过这一机制,AB-729可以降低包括乙肝表面抗原(HBsAg)在内的各种HBV病毒抗原的表达,这被认为是重新唤醒患者免疫系统对抗病毒的关键先决条件。
AB-729基本信息
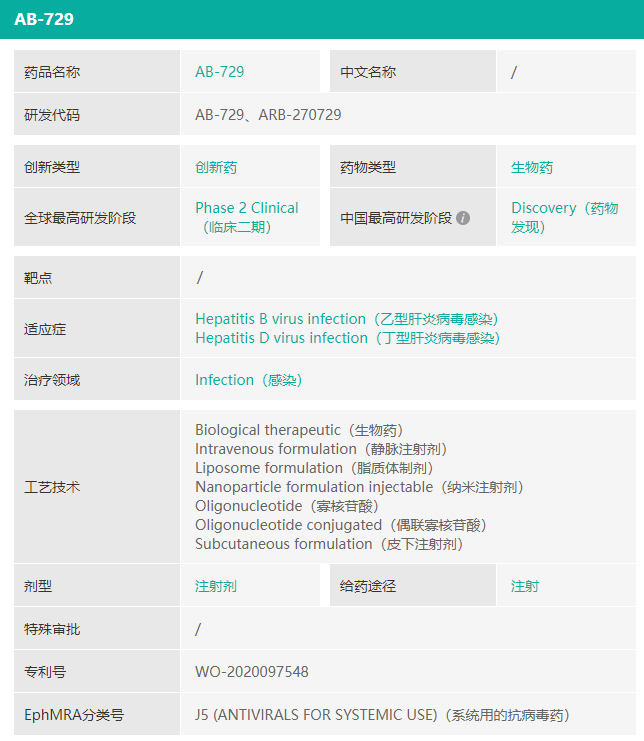
截图来源:药融云全球药物研发数据库
根据公开信息,2021年12月13日,齐鲁制药与Arbutus宣布达成独家许可协议和战略合作,齐鲁制药向Arbutus支付4000万美元预付款以及2.45亿美元的后续里程碑付款,获得了AB-729在大中华区的开发和商业化权益。

而Arbutus正在推进AB-729的一项IIa期随机、开放标签、概念验证临床试验,主要目的是评估AB-729加Peg-IFNα-2a在NA抑制的慢性HBV感染受试者中的安全性和耐受性。 此前,研究 AB-729 的单剂量和多剂量的安全性、耐受性、药代动力学和药效学的多队列Ia/Ib期临床试验的数据表明:AB-729在48周的给药期间通常是安全的并且耐受性良好。 长期使用AB-729使75%的患者的HBsAg水平<100 IU/mL。初步数据表明,AB-729长期抑制HBsAg会增强患者对HBV的特异性免疫反应。
关于Arbutus
Arbutus是一家临床阶段的生物制药公司,致力于利用其广泛的病毒学专业知识开发针对特定病毒性疾病的新疗法。Arbutus目前的重点领域包括乙型肝炎病毒(HBV)和冠状病毒。

(图源:产品管线)
参考来源:
[1] CDE官网
[2] 药融云数据库
[3] Arbutus Biopharma官网
[4] RNA Interference (RNAi) | nih.gov
想要解锁更多药企创新药信息吗?查询药融云数据库(https://www.pharnexcloud.com/?zmt-mhwz)掌握药企创新药产品布局、基本信息、最新进展、研发阶段、临床试验信息、市场规模与前景,可否投入研发!注册立享15天免费试用和虎年首份医药数据大礼包!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论