
11月12日,来凯医药与齐鲁制药就AKT强效抑制剂 LAE002(afuresertib)签订中国地区独家许可协议。按协议,首个适应症在中国获批新药申请前,来凯最高可获5.3亿元不可退还的首付款及临床开发里程碑付款,加上其他里程碑款项,最高达20.45亿元。此外,来凯还有权按中国地区未来净销售额收取梯度销售分成,比率从十余到二十余个百分点不等。

截图来源:企业公告
LAE002(afuresertib)作为AKT强效抑制剂,具备独特优势。它能同时抑制三种AKT亚型(AKT1、AKT2及AKT3),是全球仅有的两种处于晚期临床开发阶段、针对乳腺癌及前列腺癌的AKT抑制剂之一。
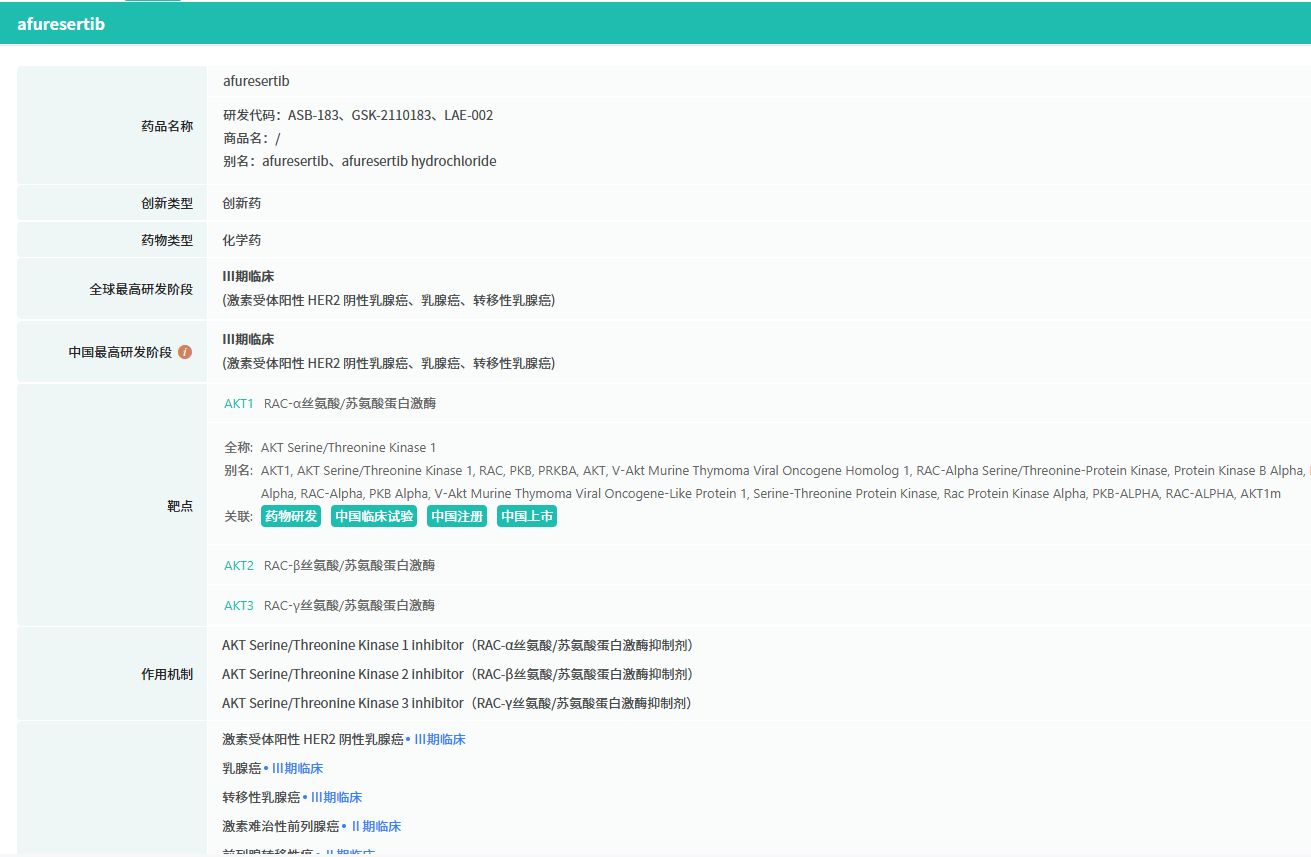
截图来源:摩熵医药数据库-全球药物研发数据库
乳腺癌已成为全球女性的“头号杀手”,每年新增病例约229万例,导致66.6万人失去生命。在中国,乳腺癌在女性癌症发病中位居第二,其中70%的患者属于HR+/HER2 -型(激素受体阳性/HER2阴性)。多数患者初始治疗可从一/二线内分泌+CDK4/6抑制剂和/或化疗中获益,但一段时间后,大部分会产生耐药,导致治疗失败。患者迫切需要耐药后的新型治疗选择,而AKT抑制剂正是这一类患者的新希望。
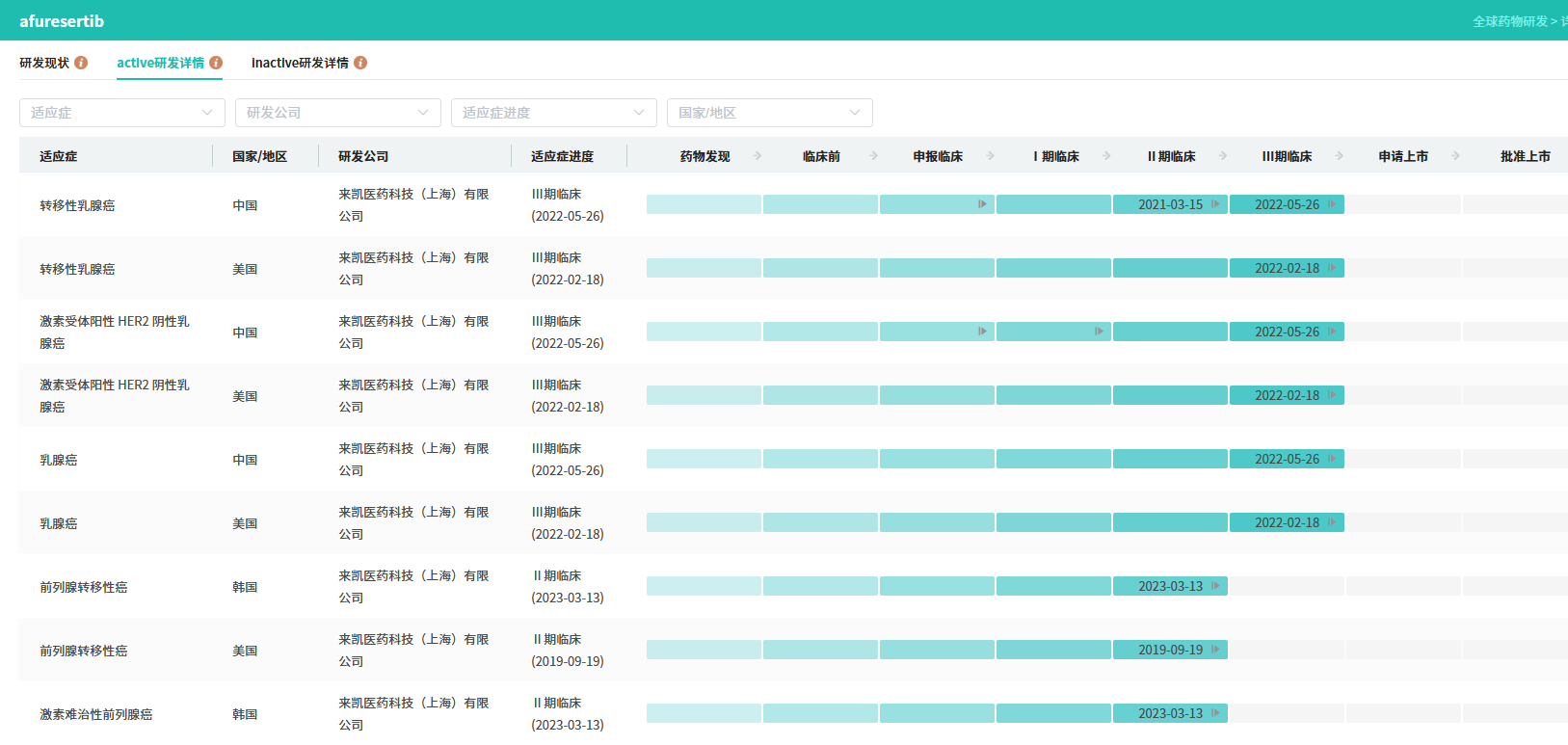
截图来源:摩熵医药全球药物研发数据库
目前,LAE002(afuresertib)针对HR+/HER2 -乳腺癌的III期临床试验(AFFIRM - 205)招募工作正按计划有序开展。来凯医药将负责完成本次III期临床试验,目标是在2025年第四季度完成受试者入组,并计划于2026年向中国国家药品监督管理局药品审评中心(CDE)提交新药上市申请(NDA)。
此次来凯医药与齐鲁制药的合作,是医药领域的一次强强联合。随着临床试验的推进和新药上市申请的提交,LAE002有望早日造福中国乳腺癌患者,为他们的生命健康带来新的曙光。
参考来源:
[1] 企业公告/官方披露
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 针对肥胖症治疗!来凯医药自研单抗 I 期临床完成首例受试者用药
2. 来凯医药携手礼来加速LAE102减肥药研发,股价暴涨48%
3. 齐鲁制药、正大天晴帕妥珠单抗生物类似药同日获批,乳腺癌治疗市场迎新变局
想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!




































![医药高地:核药!恒瑞医药镥[177Lu]氧奥曲肽注射液获批临床](https://oss-personal-public.bcpmdata.com/images/covers/202302/09/e3938ad9f1d23e2fd043611c4a98c02a.png)



















 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论