
2023年1月13日,恒瑞医药(600276.SH)发生32笔大宗交易,总成交3631.12万股,成交金额13.5亿元,成交均价37.19元,折价5.30%。恒瑞医药本周五收盘报价39.27元,涨幅3.92%,成交金额27.63亿元,目前市值2505亿元;周五恒瑞医药大宗交易成交金额占当日成交金额48.87%。
本月恒瑞医药有多笔大宗交易,金额在千万到数亿不等,1月13日13.5亿元的大宗交易实属少见。
据上交所官网,恒瑞医药部分大宗交易如下:
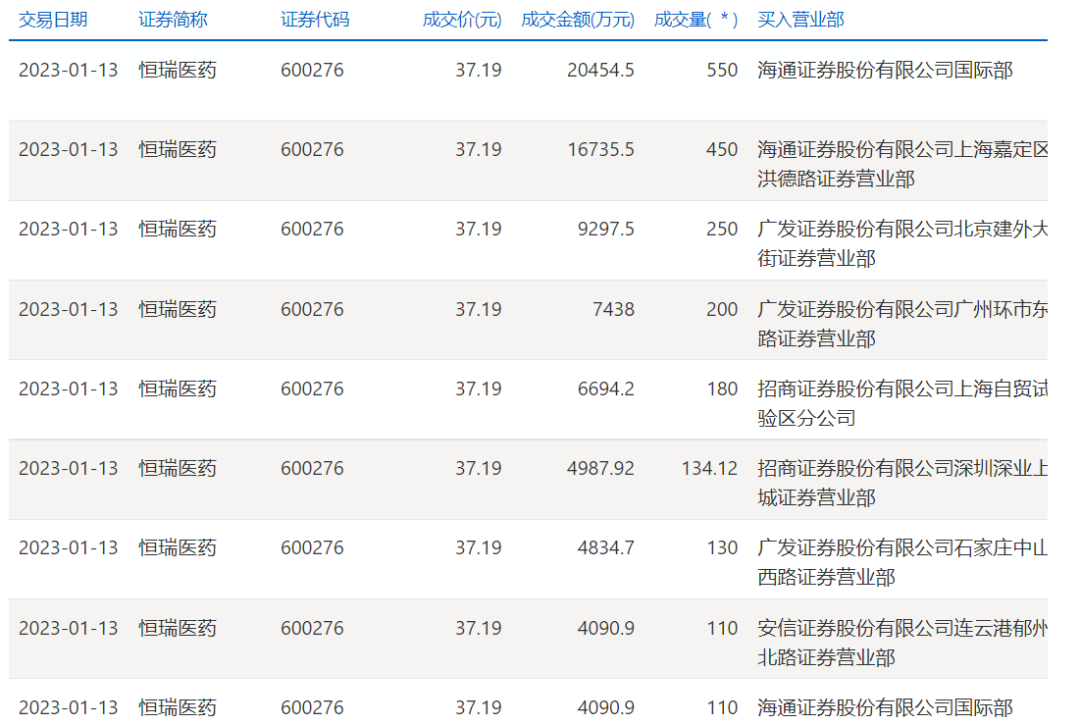
回购股份情况:
恒瑞医药在2023年1月4日公告,回购公司股份的进展情况:截至2022年12月31日,公司通过集中竞价交易方式累计回购股份12,000,031股,占公司总股本的比例为0.19%,成交的最高价为34.90元/股,最低价为27.08元/股,已支付的总金额为397,984,751.63元(不含交易费用)。2022年3月13日回购方案显示:回购价格不超过人民币60.22元/股(含),回购资金总额不低于人民币6亿元且不超过12亿元。
恒瑞医药的PI3Kδ抑制剂林普利塞(因他瑞)开出首批处方。据中国证券报·中证网,1月13日记者从恒瑞医药获悉,近日,林普利塞片(商品名:因他瑞)正式进入临床应用,由哈尔滨血液病肿瘤研究所马军教授和苏州大学附属第一医院吴德沛教授开出首批处方。据药融圈监测:林普利塞片零售价格为22800元人民币(《22800元!国内原研新药,林普利塞片价格出炉》)。
林普利塞是恒瑞医药引进的1类新药,由璎黎药业研发,是一种磷脂酰肌醇 3-激酶-δ(Phosphoinositide 3-kinase-δ,PI3Kδ)小分子抑制剂。据药融云数据库显示,2021年2月,恒瑞医药与璎黎药业达成协议,璎黎药业授予恒瑞医药针对林普利塞在大中华地区的联合开发权益以及排他性独家商业化权益,预计总支付金额两千万。
恒瑞医药与璎黎药业关于林普利塞的交易信息
截图来源:药融云全球医药交易数据库
林普利塞于2022年11月正式获批上市,用于治疗既往接受过至少两种系统性治疗的复发或难治(R/R)滤泡性淋巴瘤(FL)成人患者。作为我国首个高选择性PI3Kδ抑制剂,林普利塞采用创新性的药物结构,使其选择性更高、特异性更强,有助于减少高血糖、高血压及腹泻等不良反应情况的发生。同时,林普利塞的给药方式为口服给药,给药频次为一日一次且不受餐食影响,更有助于提升患者依从性,便于临床长期治疗和有效管理。
总结
今年开年,恒瑞医药在重要人事方面也有较大变化。恒瑞医药聘任原基石药业(02616.HK)创始人江宁军担任公司副总经理、首席战略官,负责公司临床研究和商务拓展工作。由孙飘扬、张连山和江宁军组成恒瑞医药战略决策小组,全面负责恒瑞医药的战略和研发决策。
作为国内创新药企的标杆,截至目前恒瑞医药已有12个创新药上市,8个已经进入国家医保。本轮医保谈判,公司有达尔西利、恒格列净、瑞维鲁胺3个新产品,以及卡瑞利珠单抗、吡咯替尼、瑞马唑仑的多项新适应症通过医保谈判形式审查。此外公司还有5个处于NDA阶段的创新药和10余个处于III期阶段的创新药,在火热的ADC领域,公司的领衔产品SHR-A1811已处于临床III期,目前已有8款ADC候选药物进入临床阶段。未来恒瑞医药将迎来多个重要时间节点,在创新药领域的布局,或将陆续开花结果。
2022年恒瑞医药获批临床的1类新药(统计截止于11月5日)
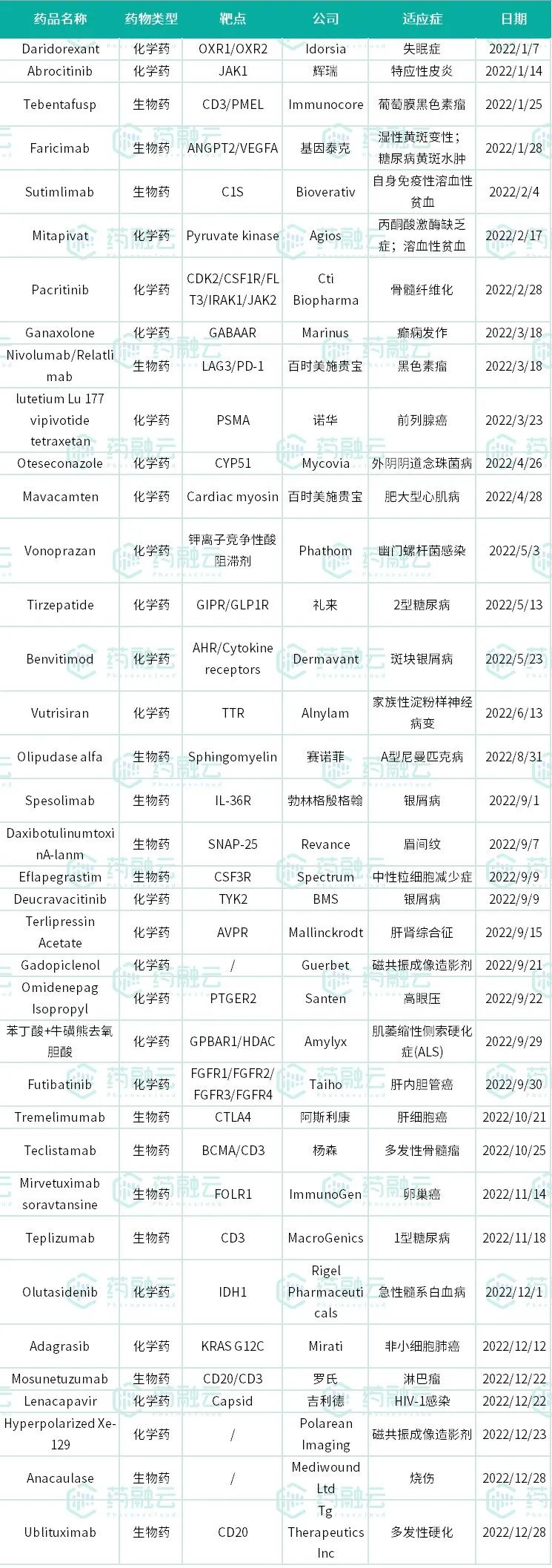
数据来源:药融云数据库
参考资料:
[1] 恒瑞医药公告
[2] 中证报
[3] 上海证券交易所
[4] 国金证券
[5] 药融云数据库
想要解锁更多药企信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药企公司基本信息、投融资情况、产品管线分布、药物销售情况与各维度分析、药物研发情况、年度报告、最新进展动态、临床试验信息、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>





















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论