
今日,珠海联邦的3.3类治疗用生物制品利拉鲁肽注射液的上市申请获得CDE受理。这是该品种第5家申报上市的本土药企。
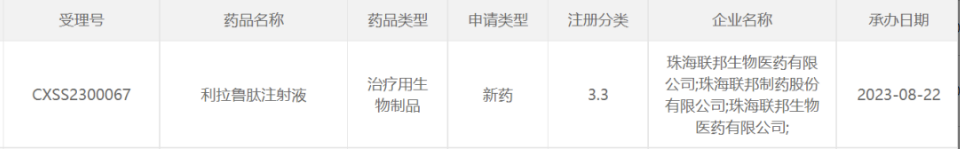
截图来源:CDE官网
利拉鲁肽注射液的原研企业为丹麦诺和诺德公司(Novo Nordisk A/S),其糖尿病适应症于2009年获得欧洲药品管理局(EMA)批准,2010年获得美国食品药品管理局(FDA)批准,商品名:Victoza®,2011年获得中国国家食品药品监督管理局(现中国国家药品监督管理局,NMPA)批准,商品名:诺和力®。
据药融云数据库,目前国内利拉鲁肽有2款相关制剂获批上市:利拉鲁肽注射液有原研诺和诺德和华东医药(国产首家)获批,德谷胰岛素利拉鲁肽注射液则是原研独家获批生产销售。其中,利拉鲁肽注射液近两年院内销售额在14亿元左右。据诺和诺德财报,2023年上半年,利拉鲁肽降糖版Victoza销售额为9.7亿元,减重版Saxenda销售额为1.07亿元。
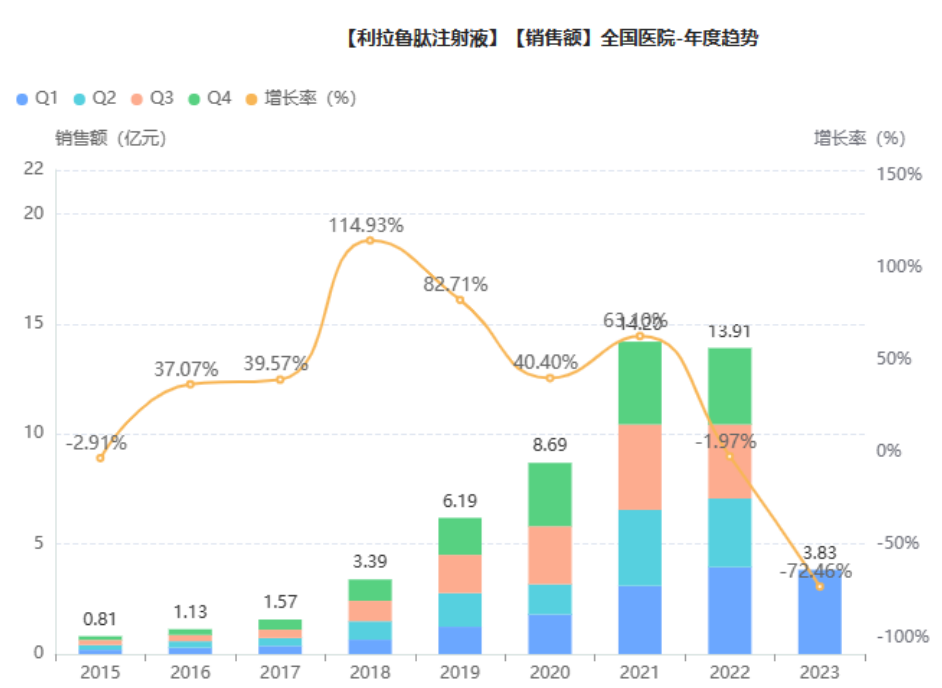
截图来源:药融云全国医院销售数据库
华东医药的利拉鲁肽注射液最早于今年3月获批上市,用于治疗糖尿病;今年7月,其肥胖或超重适应症的上市许可申请获得批准。
除了已获批的华东医药和此次的珠海联邦,另有通化东宝、翰宇药业、正大天晴的利拉鲁肽注射液也已申报上市,均在审评审批中。
<END>
要解锁更多企业药品研发信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论