
11月14日,据CDE官方网最新公示,百济神州研发的1类新药BG-60366片的临床试验申请已成功获得受理。这一消息标志着百济神州在创新药物研发领域又迈出了重要一步。
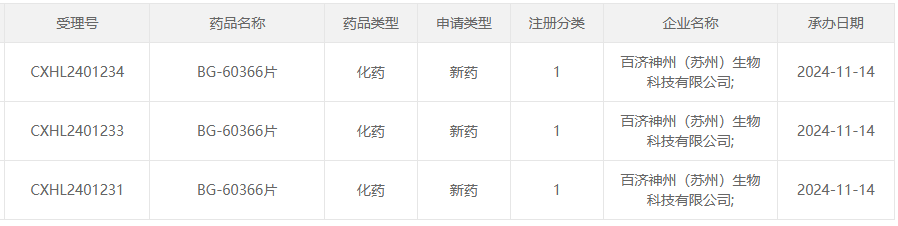
截图来源:CDE
据百济神州最新公布的第三季度报告显示,BG-60366是一款具有差异化作用机制的新型EGFR降解剂(EGFR CDAC)。该药物通过独特的机制,有望实现EGFR信号的完全抑制,为癌症治疗提供新的可能。
值得注意的是,这是BG-60366首次在中国申报新药临床研究(IND)。百济神州方面预计,该药物有望在2024年第四季度按计划进入临床阶段,为患者带来新的治疗希望。
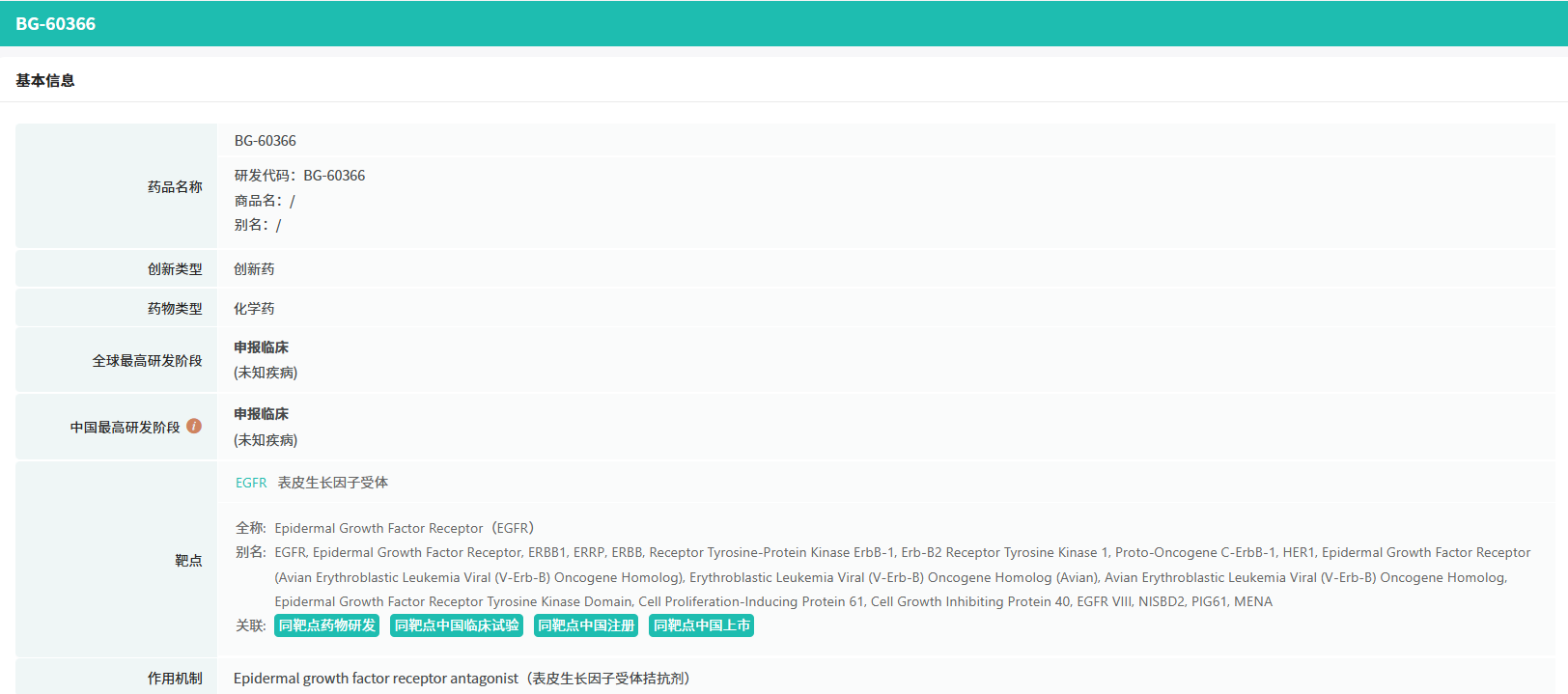
截图来源:摩熵医药全球药物研发数据库
据摩熵医药数据库显示,BG-60366作为百济神州研发的新型EGFR嵌合式降解激活化合物(CDAC),具有广泛覆盖多种EGFR突变的能力。它能够破坏EGFR支架功能,从而产生持久的信号抑制作用。在前期治疗线中,BG-60366的非冗余机制有望有效防止耐药性的发生,为患者提供更长久的治疗效果。






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论