
关注全球创新药研发进展,分析国内新药注册申报情况,了解全球在研创新药积极/失败临床结果最新动态,掌握国产创新药国际化、跨国企业创新药在华动态.....尽在《药融云医药行业观察周报》。
据《药融云医药行业观察周报》数据统计,在2023.06.12-2023.06.18期间,有全球有这些创新药研发取得阶段性的进展呢?一起来看看。
1.迪哲医药EGFR-TKI「舒沃替尼」3期临床在欧盟获批
迪哲医药的高选择性EGFR-TKI舒沃替尼一线治疗EGFR20号外显子插入(EGFRexon20ins)突变型晚期非小细胞肺癌(NSCLC)的全球多中心、随机对照、3期临床试验(悟空28,WUKONG28)近日获欧盟批准开展。
靶向治疗是EGFR敏感突变晚期NSCLC一线治疗的首选方案,而EGFRexon20ins作为EGFR突变罕见靶点,传统1-3代TKI治疗效果都不甚理想。目前针对该靶点的一线治疗仍以化疗为主,尚缺乏有效的靶向治疗药物。
舒沃替尼全球研发进度查询
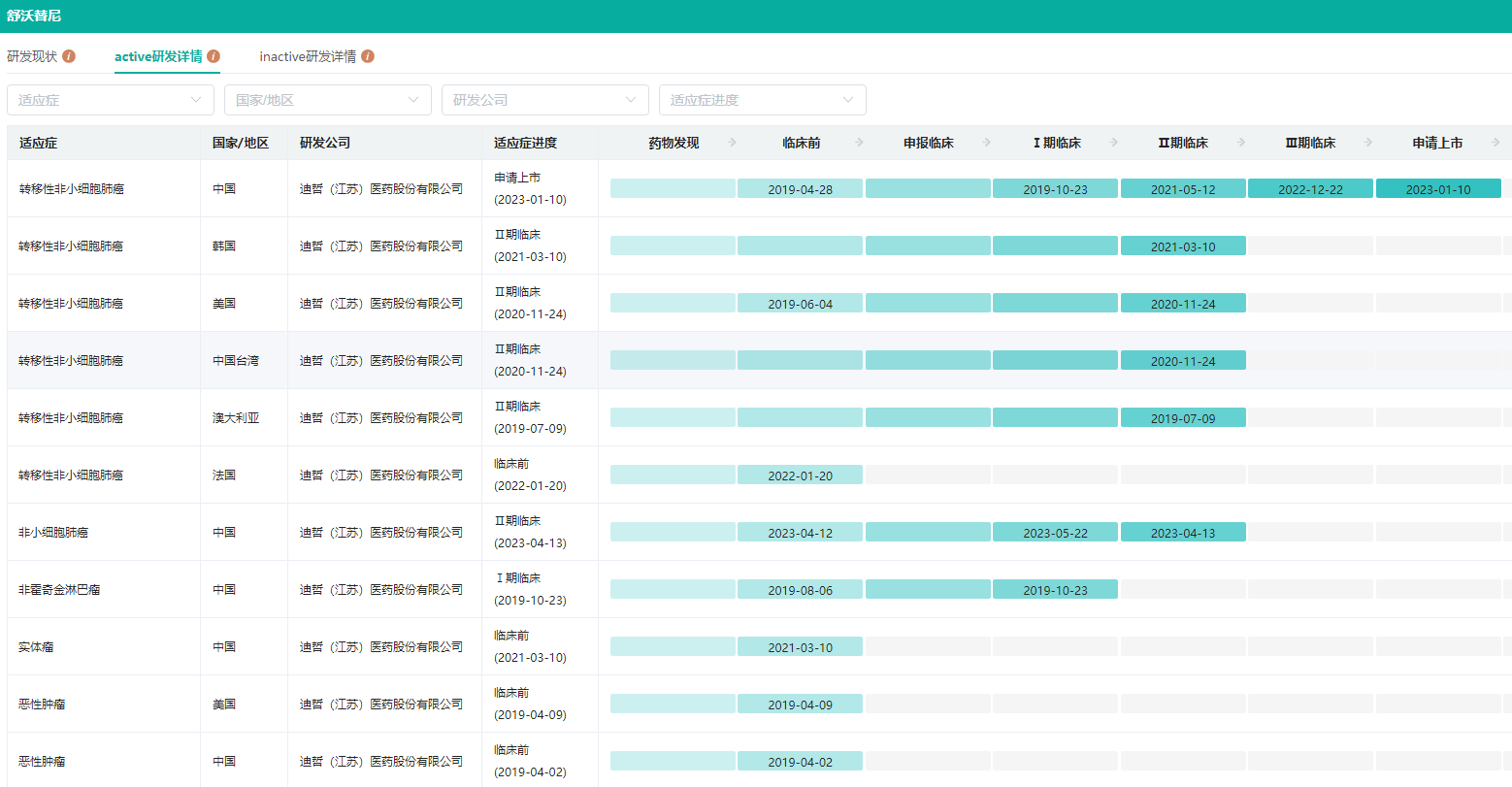
图片来源:药融云全球药物研发数据库
舒沃替尼是迪哲医药研发的一款针对多种EGFR突变亚型的高选择性EGFR酪氨酸激酶抑制剂(TKI),也是一款针对EGFRexon20ins突变型晚期NSCLC的1类新药。迪哲医药基于特有的转化科学技术平台,从源头突破难治靶点——EGFRexon20ins突变,并保留了舒沃替尼对EGFR敏感突变、T790M等多种突变的有效活性。
药融云数据库显示,舒沃替尼分别于2020年12月和2022年1月获得中国、美国“突破性疗法认定(BTD)”,成为迄今为止肺癌领域首个且唯一获得中、美两国双BTD的I类新药。
舒沃替尼获得中国突破性疗法认定-审评时间轴
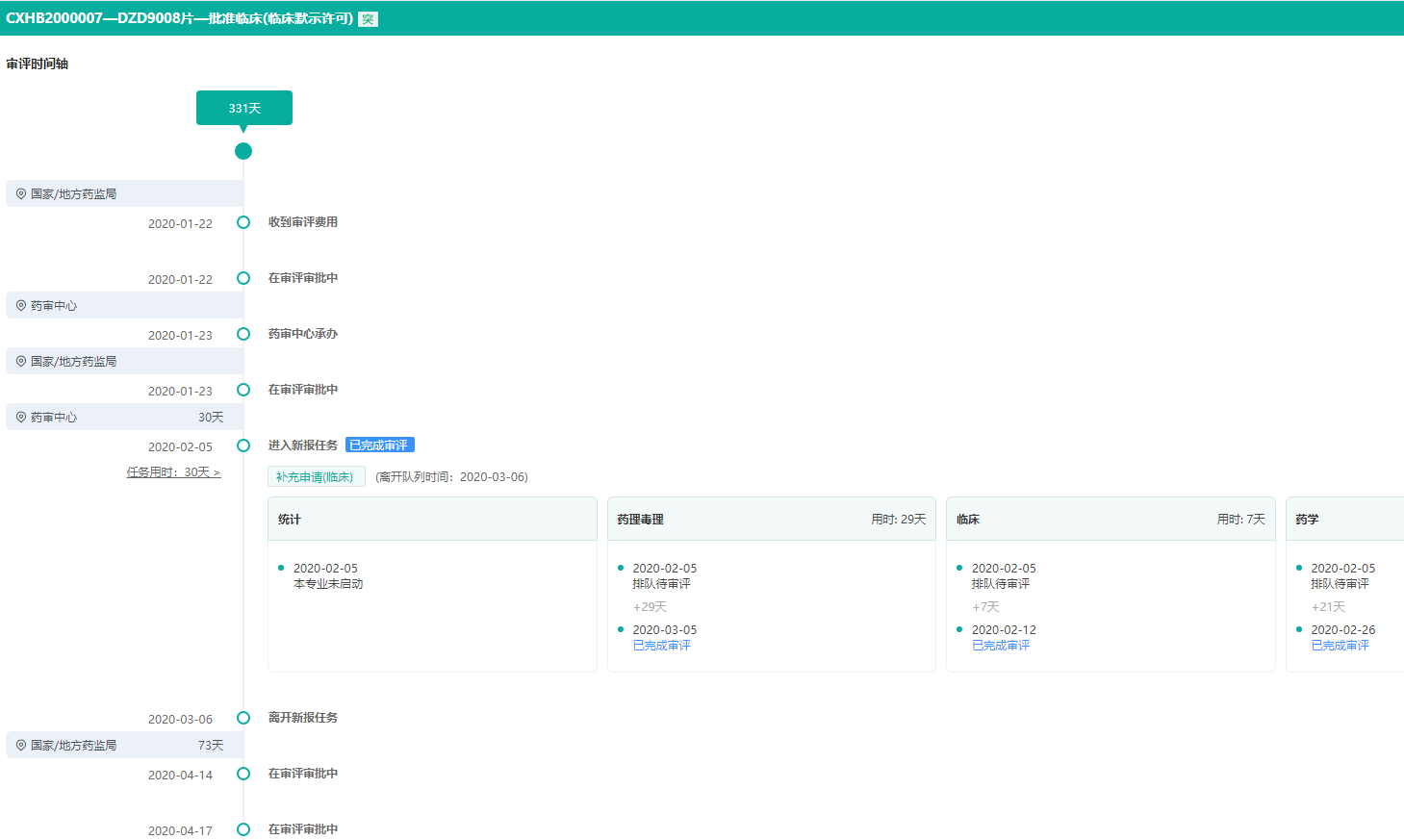
图片来源:药融云中国药品审评数据库
目前,EGFR-TKI是治疗EGFR突变型晚期NSCLC的重要手段。奥希替尼、阿美替尼、伏美替尼三款第三代EGFR-TKIs 已经获批上市用于治疗一线EGFR 突变的NSCLC 患者;贝福替尼二线适应症率先获批,三代EGFR-TKI 格局即将改变。
2.阿斯利康「依库珠单抗」在中国获批第三个适应症
阿斯利康的依库珠单抗注射液在国内获批新适应症,用于治疗抗乙酰胆碱受体(AChR)抗体阳性的难治性全身型重症肌无力(gMG)成人患者。
药融云数据库显示,这是继阵发性睡眠性血红蛋白尿症(PNH)和非典型溶血性尿毒症综合征(aHUS)之后,依库珠单抗在中国获批的第三个适应症。截至目前,依库珠单抗已在在全球多个国家和地区获批多项适应症,并在拓展新适应症。
依库珠单抗注射液(eculizumab,商品名:舒立瑞/Soliris)是一款C5补体抑制剂,通过选择性抑制末端补体C5的激活来发挥作用。
依库珠单抗在研适应症查询
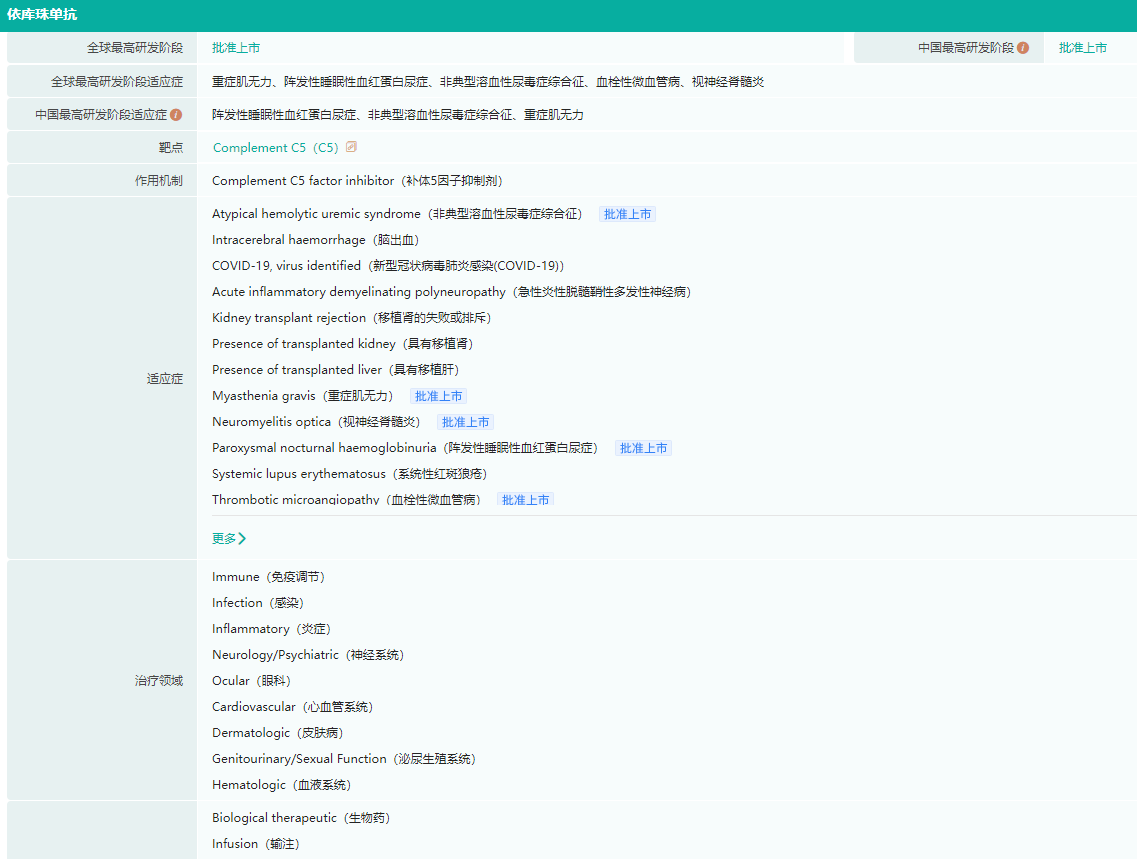
图片来源:药融云全球药物研发数据库
全身型重症肌无力(gMG)是一种罕见的、慢性的,由神经肌肉接头传递障碍引起的自身免疫性疾病,主要表现为肌肉功能丧失、骨骼肌波动性无力及严重衰弱。乙酰胆碱受体(AChR)抗体是MG最常见的致病性抗体,约80%的患者可检测到AChR抗体,这意味着AChR抗体与神经肌肉接头(NMJ)的信号受体结合,这种结合激活了补体系统。补体在先天免疫和抗体介导的免疫中起着重要作用,补体的激活导致膜攻击复合物(MAC)的形成,从而导致神经肌肉接头传递障碍,进而引发神经肌肉传递异常和与MG相关的特征性肌肉无力。
3. 迈威生物抗IL-11单抗在美国获批临床
迈威生物研发的抗IL-11单抗9MW3811注射液临床试验申请正式获得美国FDA批准,可针对特发性肺纤维化开展临床试验。
特发性肺纤维化是一种原因不明、以弥漫性肺泡炎和肺泡结构紊乱、最终导致肺间质纤维化为特征的疾病。9MW3811是其研发的靶向人白介素-11(IL-11)的人源化单克隆抗体,可高效阻断IL-11下游信号通路的活化,抑制IL-11诱导的病理生理功能,从而达到对纤维化疾病和肿瘤的治疗效果。
药融云数据库显示,9MW3811已在澳大利亚、中国、美国三地分别获批开展临床试验。其中,2023年2月在澳大利亚开展的临床试验处于剂量爬坡阶段,阶段性数据显示其安全性良好。后又于3月,收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,用于晚期恶性肿瘤和特发性肺纤维化的临床试验获得批准。
9MW3811国内获批临床耗时69天
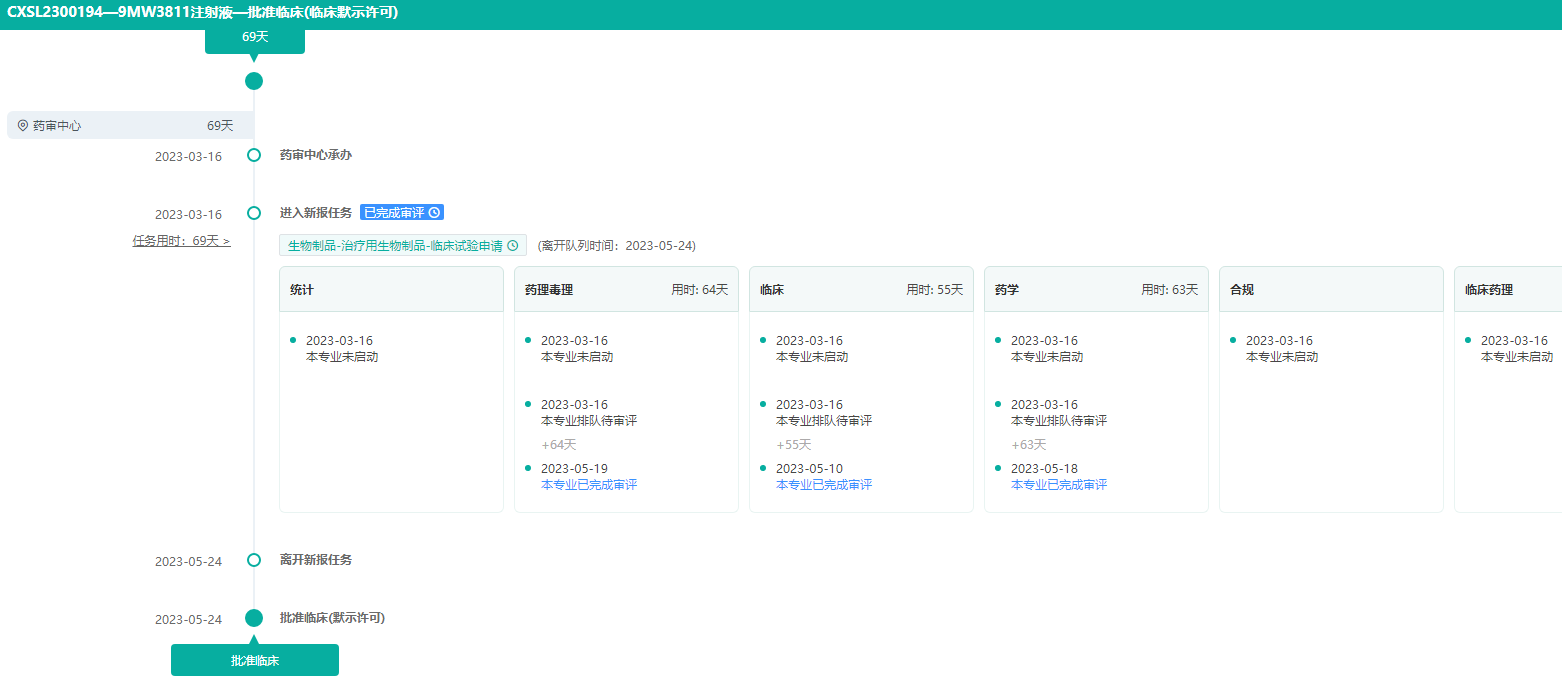
图片来源:药融云中国药品审评数据库
4. 罗氏神经罕见病新药「利司扑兰」适应症拓展在华获批
罗氏(Roche)的神经罕见病创新药物利司扑兰口服溶液用散的适应症拓展,已经获中国国家药监局(NMPA)批准。此次获批则将利司扑兰的适用人群拓展至16日龄及以上的脊髓性肌萎缩症(SMA)患者。
SMA是一种严重的进行性神经肌肉疾病。根据中国《脊髓性肌萎缩症多学科管理专家共识》,流行病学研究表明,约80%患者在出生后18个月内起病。该病通常由运动神经元生存蛋白(SMN)的缺失或功能异常所致,患者运动、呼吸、吞咽以及脾脏、心脏、胰腺等多器官均会受影响,甚至威胁生命。
人体内的SMN1基因和SMN2基因可以生成SMN蛋白,SMN1基因占主导作用,SMN2基因产生约10%的SMN蛋白。利司扑兰是一种SMN2基因mRNA剪接修饰剂。它通过双位点特异性调控SMN2(SMN1的同源基因)的剪接,促进保留外显子7,提高功能性SMN蛋白水平。该药还可穿透血脑屏障,分布于中枢和外周,提高全身多系统SMN蛋白水平,且保持稳定。
利司扑兰口服溶液用散-审评时间轴
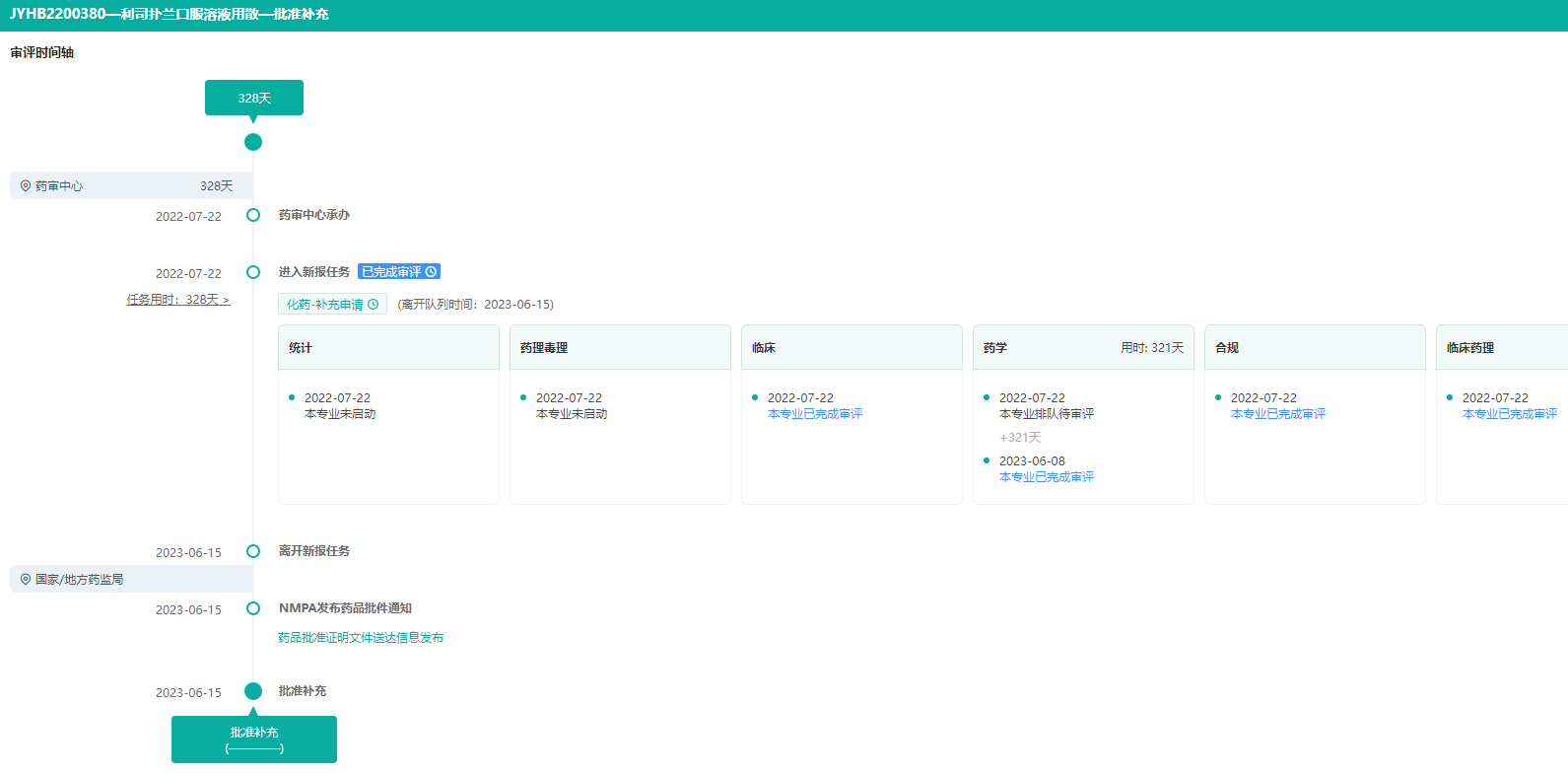
图片来源:药融云中国药品审评数据库
药融云数据库显示,目前全球共有三款SMA治疗药物上市,分别是诺西那生(nusinersen)、利司扑兰(risdiplam)和onasemnogene abeparvovec。国内已获批上市的有诺西那生、利司扑兰。
利司扑兰口服溶液用散,用于治疗2月龄及以上SMA患者。这是首个在中国获批治疗SMA的口服疾病修正治疗药物。2023年3月份该药进入了医保目录,大幅减轻了患者负担,提升了治疗可及性。
5.康哲药业创新鼻喷雾剂获批,用于癫痫发作急救
康哲药业引进的5.1类新药地西泮鼻喷雾剂上市申请已获得批准,是国内首个地西泮鼻喷雾剂。地西泮鼻喷雾剂是一种经鼻给药的苯二氮卓类药物,用于癫痫发作急救。
药融云中国药品批文数据库显示,地西泮片目前拥有113个在使用批文,涉及国药集团、科伦药业、力生制药、信谊制药、百正药业、丹东医创药业、长征药业等生产企业。地西泮注射液拥有23个在使用批文,涉及哈药集团、倍特药业、济川药业、三峡制药等生产企业。
地西泮生产批文查询(部分展示)
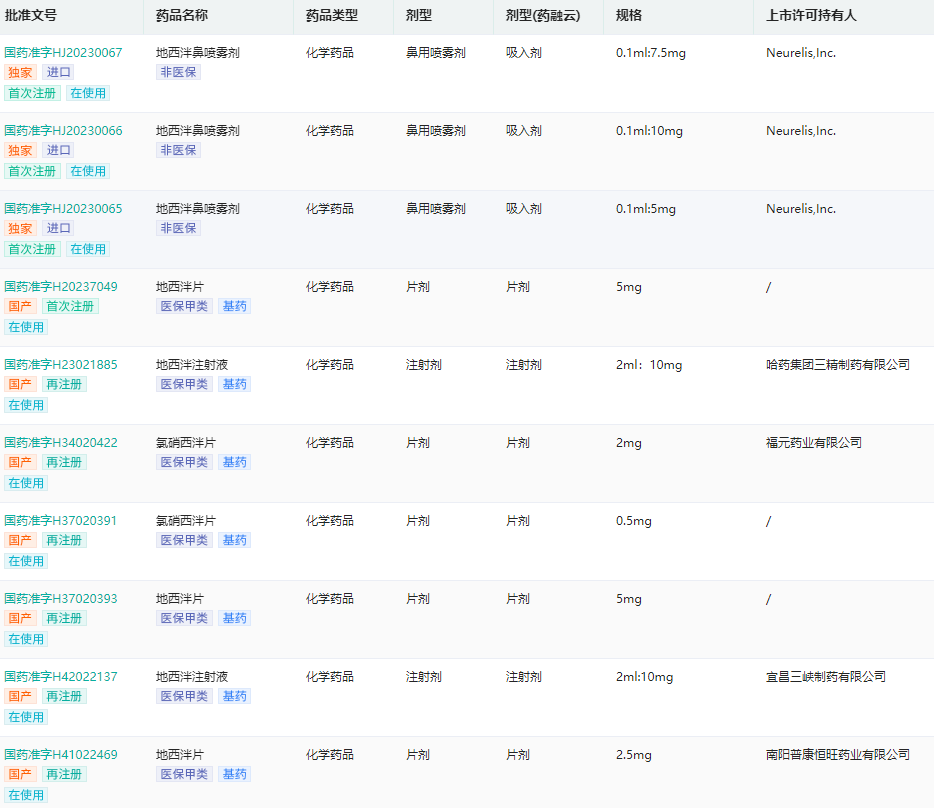
图片来源:药融云中国药品批文数据库
癫痫是常见的一种神经系统疾病。约有30%的病人在使用了稳定的抗癫痫药物后,仍出现不受控制的癫痫发作,这类疾病又被称为丛集性癫痫发作,这种发作可以发生在成人和儿童中,也可以发生于各种类型癫痫,还可能一天之内发作多次。由于丛集性癫痫一般会突然发作,如果不能识别并提早干预,可能会导致严重的后果。
据悉,与静脉注射地西泮相比,地西泮鼻腔喷雾剂的绝对生物利用度较高,变异性低。此外,它还具有多重优势,包括:对多种癫痫发作类型有效;吸收迅速,起效快,患者间生物利用度一致;容易准备和使用(包括病人在意识未发生改变的时间间隔内);具有持续的疗效时间;副作用小或少。该产品不但为癫痫患者丛集性发作时提供有效、便捷、安全的急救治疗以解救发作,还能极大地提高患者和照看者的生活质量。
想要了解更多全球在研新药的详细动态,请登录药融云数据库进行查询;或者关注“药融云(yrydata)”公众号,后台回复关键词“报告”领取完整报告内容。
想要解锁更多药品信息吗?查询药融云数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、通过一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!

<END>






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论