
在现代创新药研发的漫长链条中,有一个至关重要却常常被低估的节点:从化合物首次合成(First Synthesis, FS)到首次人体给药(First Dose in Man, FIM)的过渡期。
如何在这段被称为“死亡之谷”的区间内最大限度地缩短时间(FS-to-FIM),不仅考验着研发团队的科学智慧,更是决定药企能否在红海竞争中抢占先机的核心壁垒。本文将穿透历史的周期,以百时美施贵宝(BMS)在20世纪90年代的经典战略为蓝本,结合当下高度复杂的分子实体与虚拟Biotech生态,全景拆解加速早期药物开发的底层逻辑。
一、 历史的倒影:从“顺其自然”到“时间焦灼”
要洞察当下的战略,我们必须先回溯行业的发展轨迹。在20世纪80年代以前,药物发现与开发的界限相对模糊。
1. 早期研发的“古典时代”
在早期的施贵宝医学研究所(Squibb Institute for Medical Research,后并入BMS),新药研发主要依赖于体内表型筛选。

- 化学家们更倾向于对熟悉的结构(如天然产物或“me-too”类化合物)进行修饰,而在合成之初甚至并不完全清楚其确切的生物作用机制。
- 彼时,评价化合物潜力的核心在于其是否在动物模型(如原发性高血压大鼠SHR模型、感染小鼠模型等)中展现出优于阳性对照药的体内活性。
- 在这一阶段,“成药性”并非核心痛点,因为那时的活性分子普遍具备低分子量(<500 Da)、含碱性胺基且易成水溶性盐的特征。
经典降压药纳多洛尔(康加尔多)的诞生便印证了这一模式:基于简单的结构预测进行合成,在证实其体内活性后,便迅速以四种非对映体混合物的形式推向市场。
2. 监管收紧与“时间膨胀”
然而,随着20世纪80年代制药行业步入黄金期,药物发现(专注构效关系SAR)与药物开发(专注ADME与毒理)开始明确分工。进入90年代,新靶点的大量涌现、临床验证的缺乏以及监管政策的收紧,导致研发周期被不断拉长。
一项塔夫茨基准研究(Tufts benchmarking study)揭示了令人警醒的数据,其报道了活性分子从首次进行药理试验到首次进行人体研究的时间(以月为单位)。
- 20世纪60年代:首次人体给药平均耗时 18个月。
- 20世纪70年代:上升至 27个月。
- 20世纪80-90年代:平均耗时已达 31~34个月。
与开发时间延长形成致命对冲的,是新药市场独占期的急剧缩水。第一代重磅药物(如卡托普利)尚能享受4.7年的市场独占期,而到了90年代末,神经氨酸酶抑制剂(如达菲、瑞乐砂)的首发优势仅剩下短短的几个月,甚至几近于无。
卡托普利的化学结构
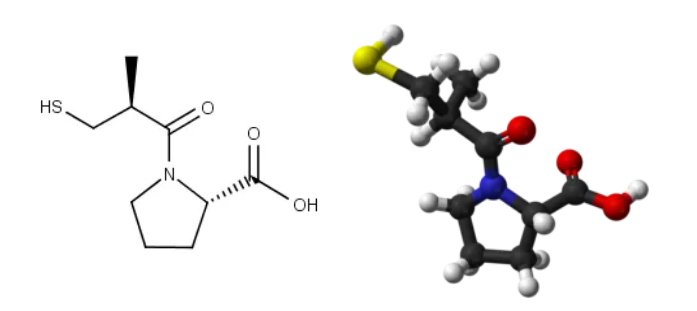
图源:摩熵医药数据库
在巨额研发投入与短暂回报期的双重挤压下,“提速”成为了关乎企业生死存亡的必答题。
二、 BMS的破局之战:重构发现与开发的边界
面对行业困局,BMS在90年代初启动了激进的内部改革,核心目标直指压缩开发时间。他们对过往推进最快的项目(如卡托普利、氨曲南等,平均FS-to-FIM时间仅为12.8个月)进行了深度复盘。
复盘结果显示,决定项目速度的核心不在于运气的加持,而在于极具前瞻性的管理机制。BMS最终提炼出了四大破局策略,这些策略在今天看来依然是教科书级别的操作 :
1. 前置并行工程
针对导致延迟的第二大元凶——化合物供给断裂,BMS彻底抛弃了后置的工艺放大逻辑。他们提出了“前瞻性工艺研究策略”:在先导化合物优化阶段的最后6个月,工艺化学家就必须强行介入药物发现流程。团队组建了名为“确定我们的原材料”的特种小组,紧跟构效关系(SAR)的演进,在最终候选分子被锁定之前,就提前评估并确立了适合百克级至公斤级放大的盐型与多晶型物。这一举措使得分子在正式立项进入开发阶段时,用于限速的GLP毒理学研究的原料药已经准备就绪,彻底消灭了长达数月的工艺摸索空窗期。
2. 跨部门深度整合
为了根治部门墙带来的协作阻力,BMS在发现后期组建了“开发协调团队(DCT)”。这是一个由一线科研人员(通常是具有极强解决问题能力的化学、制造和控制(CMC)专家)全权领导的多学科矩阵式组织,其成员横跨了ADME、药物安全评估(DSE)以及临床供应链部门。DCT被赋予了极高的战术决策权,他们不受常规僵化管理制度的束缚,唯一的使命就是制定综合时间线并积极调配所有关联资源,以最小化FS-to-FIM周期。BMS甚至为这些未来领袖制定了为期两天的密集闭门培训,涵盖矩阵团队管理、基因毒性杂质控制以及同位素标记合成等硬核议程。
3. 极致的流程优化
魔鬼往往隐藏在细节之中。DCT在审查毒理学研究时间线时敏锐地捕捉到一个荒谬的现象:部分实验室在等待原料药合成完毕并运抵现场后,才开始着手订购用于GLP测试的实验动物,这导致了数周的无谓等待。通过引入适度的财务风险评估,BMS强制要求在原料药预计可用的数周前提前预订动物资源,将给药动物的空窗期与API的交付期完美重叠。仅这一项看似微不足道的供应链调度优化,就为整个项目硬生生抢回了2周的宝贵时间。
4. 文化重塑与团队狂热
流程的物理改变必须辅以化学层面的文化催化。BMS极力在发现化学家、分析研究员与工艺药师之间培养一种真诚的“主人翁意识”。这种热情并非来源于强迫性的加班,而是基于解决前沿科学挑战的成就感。在早期的 氨曲南(Aztreonam,单环β-内酰胺类抗生素)项目中,团队成员甚至自发制作并佩戴印有“我喜欢单环菌素”的红心纽扣。这种极具个人色彩的情感投射在枯燥的实验室中产生了奇妙的共振,成为了跨越无数技术死胡同的强效心理润滑剂。
氨曲南的化学结构
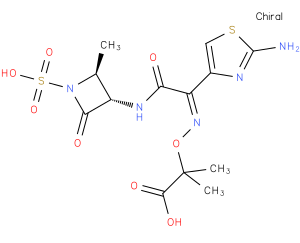
图源:摩熵医药数据库
通过这套近乎严苛的组合拳,BMS在计划实施的第一年内就收到了令人震惊的回报。原本平均需要35个月的FS-to-FIM周期被大幅度腰斩,许多常规项目在不到两年的时间内轻松完成,而最顺利的明星项目,甚至在短短367天内就跑完了从首次合成到受试者体内给药的全程。BMS在1990年代奠定的这套加速理论,至今仍被全球各大药企奉为金科玉律。
三、 现代启示录:应对复杂分子的化学突围
时至今日,随着高通量筛选和靶向制剂平台的普及,候选分子的结构复杂性呈指数级上升。在BMS看来,化学复杂性是一个动态的、随时间变化的外部现象,它直接决定了工艺团队能否在规定时间内交付高质量的化合物。
在向开发阶段过渡的前6~9个月,新药研发团队必须做出第一个也是最重要的战略决策:是继续沿用发现阶段的合成路线,还是投入资源开发全新的合成技术?
经典案例:JAK2抑制剂 BMS-911543 的极速突围
BMS-911543 的开发完美诠释了“磨刀不误砍柴工”的现代工艺逻辑。
BMS-911543 的化学结构
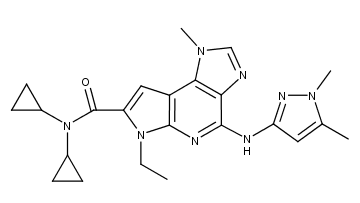
图源:摩熵医药数据库
- 初始困境:发现团队提供的原始合成路线长达19步,不仅效率极低,而且如果强行放大,将耗尽庞大的研发资源。
- 果断重构:BMS迅速集结高级化学家团队,从市售原料出发,并行探索替代路线。
- 惊艳交付:在短短7个月内,一条全新的10步线性合成路线(总收率11%)被成功确立。这不仅解决了工艺安全问题,更在概念提出后的1年内,奇迹般地交付了600g毒理学样品和2.2kg的I期临床样品。
BMS-911543 项目从药物发现阶段向临床开发阶段过渡期的合成工艺进化全景对比
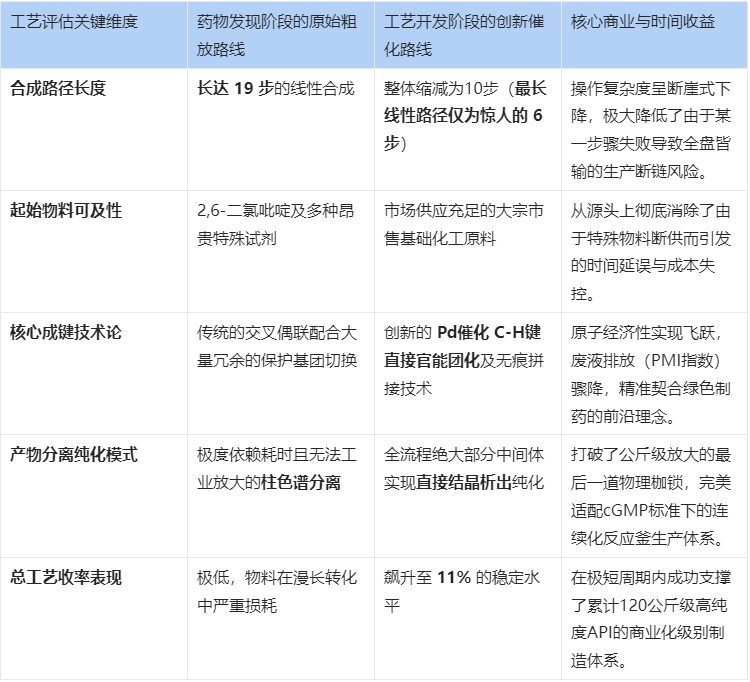
这一案例深刻表明:对基于首要原则的底层化学创新进行早期投资,是化解复杂性、跑赢时间差的最有效利器。
四、 虚拟化生存:CRO/CMO 生态下的并联引擎
BMS-911543 的辉煌固然令人心潮澎湃,但这很大程度上是依赖于资金雄厚、人才济济、试错底气十足的大型跨国药企(Big Pharma)的“巨舰逻辑”。然而,将目光投向当下医药创新的另一股绝对中坚力量——数以千计的中小型生物技术公司(Biotech),情况则呈现出另一番景象。
由于资本环境的严冬与资源聚焦的必然要求,现代的Biotech公司在组织架构上往往呈现出极其明显的“虚拟化”特征。它们可能在人工智能靶点发现、单细胞测序或前沿空间转录组学等深水区拥有独步天下的技术壁垒,但一旦涉及到需要耗资数亿美元自建的CMC(化学、制造和控制)工艺实验室、GMP标准的原料药/制剂放大车间以及庞大的临床运营团队时,它们往往一筹莫展。对于这些与时间赛跑、与融资里程碑对赌的Biotech而言,如何能够以轻资产的模式,完美复制甚至超越BMS当年那种极致的FS-to-FIM竞速曲线?
通过与具备顶尖能力的合同研究组织(CRO)以及合同定制研发生产机构(CDMO)进行深度绑定,Biotech企业能够实现跨空间的“并行活动”。例如,在优化含有多个复杂片段(ABCDE)的分子路线时:
① 委托一家CRO并行制备公斤级的A和B独立片段。
② 同时调度第二家CRO的高级FTE(全时当量)团队,攻克低收率的核心合成步骤。最终,将一条总收率仅为4.6%且严重依赖色谱分离的路线,蜕变优化为收率高达43%的商业化路线。
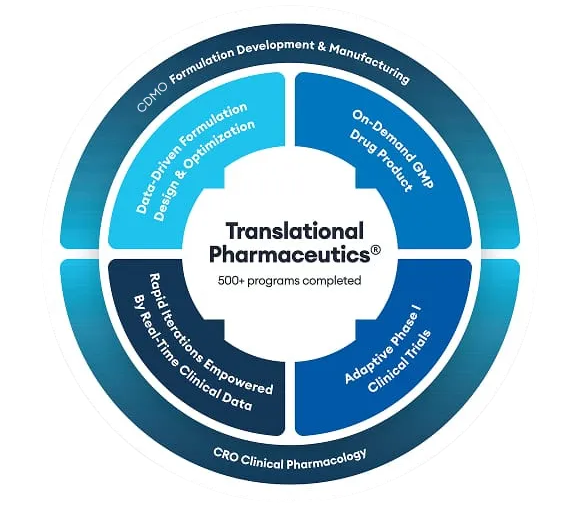
此外,一体化平台的崛起正在进一步重塑时间线。例如,Quotient Clinical 推出的 Translational Pharmaceutics 平台,能够将制剂开发、cGMP生产与临床研究无缝桥接 。该平台甚至支持在给药前实时生产药品(如短效脂质口服胶囊),根据临床实时数据动态调整剂量,彻底消灭了FIH(首次人体试验)前冗长的临床批次生产和等待时间。
五、未来已来——硅基算力、自动化与转化科学的终极交响
纵观全篇,我们已经详尽地梳理了制药工业为跨越“死亡之谷”所做出的种种卓绝努力。从1980年代以前闭门造车、依赖动物模型的“经验试错”,到1990年代BMS通过打破部门物理藩篱、强势引入“并行介入”与“矩阵协调(DCT)”所引发的管理学流程革命;再到当代面对结构犹如迷宫般的复杂分子时,通过前置工艺介入与尖端金属催化技术(如C-H键活化)实现降维打击;直至今天,由Biotech与一体化CDMO构建的敏捷共生网络。
然而,如果我们要为这张面向下一个十年的研发加速全景图画上最后的点睛之笔,就必须承认,仅仅依靠人类管理学层面的流程压榨与顶尖化学家肉身在实验室里的手工试错,已经无可避免地触及了碳基生命的效率天花板。立足当下的前沿,以生成式人工智能(Generative AI)和大语言模型(LLMs)为代表的硅基浪潮,正在以排山倒海之势,为FS-to-FIM这一人类科学史上最艰难的征途注入属于未来的狂暴加速度。
1. 生成式AI:重塑逆合成规划的神级外脑
正如Li和Eastgate在其“当前复杂性”模型中所深刻指出的,分子的外在合成难度受制于人类已知的化学工具组合。在过去,要寻找类似于BMS-911543那条能够将19步削减至10步的绝世工艺路线,高度依赖于全球屈指可数的顶尖工艺化学大拿们的灵光一现、深厚的直觉积淀以及无数个日夜在通风橱前的繁重试错。
如今,生成式AI与计算机辅助合成规划(Computer-Assisted Synthesis Planning, CASP)正在无情地颠覆这一陈旧的知识传承模式。通过深度学习人类历史上数以亿计的化学反应数据库,结合量子化学底层规则,当代最先进的AI大模型能够在区区几分钟内,穷举并并行评估数万条潜在的逆合成裂解路线。它们不仅能够预测一个分子的理论可合成性,更能在图纸阶段就主动识别并规避那些可能导致微量重金属残留、极高废液排放或易爆风险的危险转化步骤。
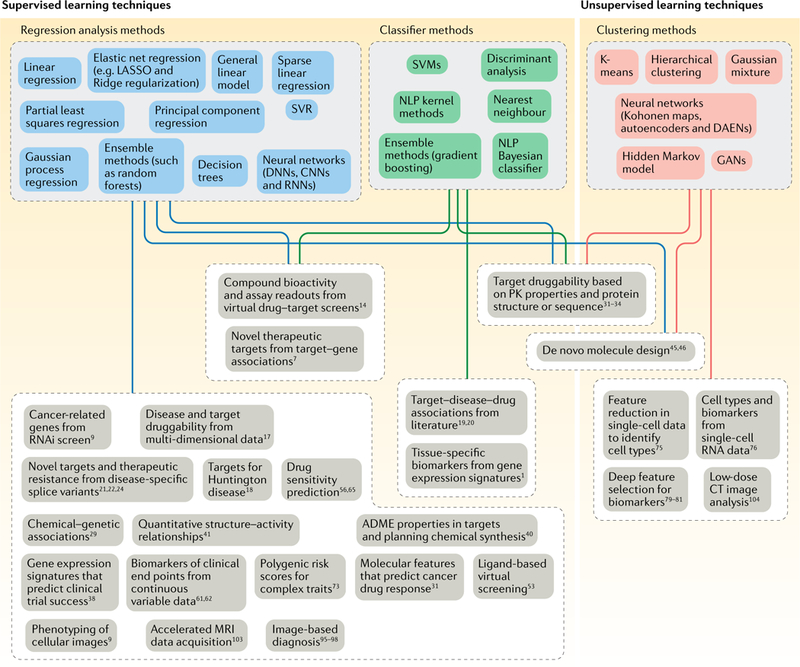
机器学习工具及其在药物发现中的应用(doi:10.1038/s41573-019-0024-5)
这意味着,在极早期的靶点锁定与先导化合物设计阶段,AI就如同拥有了未卜先知的能力。它能提前将那些“在计算机屏幕上亲和力无敌,但在工厂反应釜里根本无法量产”的废柴分子剔除出局,从而将前瞻性工艺的防线向极度前端再次推进,彻底消灭了进入开发期后才发现路线走不通的灾难性回溯。
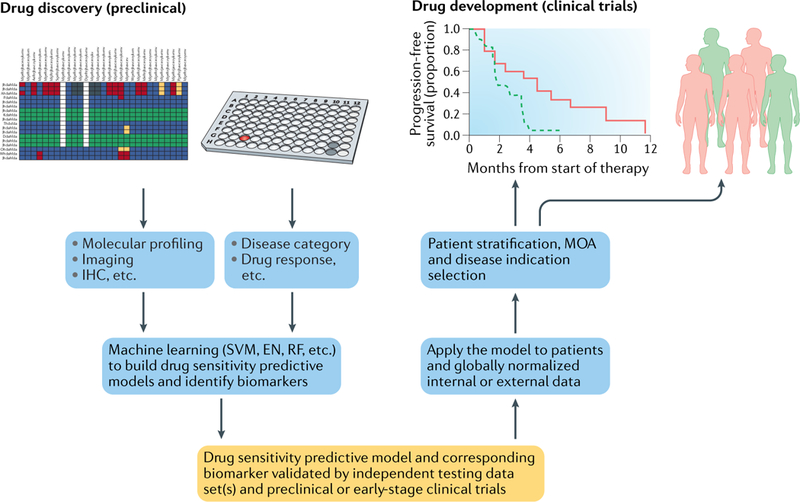
利用预测性生物标志物支持药物发现和开发
2. 18个月的硅基奇迹:数字化时代的“极速冲刺”
在这场硅基革命中,以英矽智能(Insilico Medicine)为代表的AI驱动型先锋药企,已经向整个守旧的制药工业展示了算法带来的恐怖破坏力。在一项旨在攻克特发性肺纤维化(IPF)的创新药攻坚战中,该公司利用其自研的AI引擎生成对抗网络,不仅独立发现了未见经传的全新致病靶点,更是从零开始由AI亲手设计出了代号为ISM001-055的全新小分子实体。
Insilico Medicine公布利用生成式人工智能发现的新型疗法的研发候选药物基准和时间表
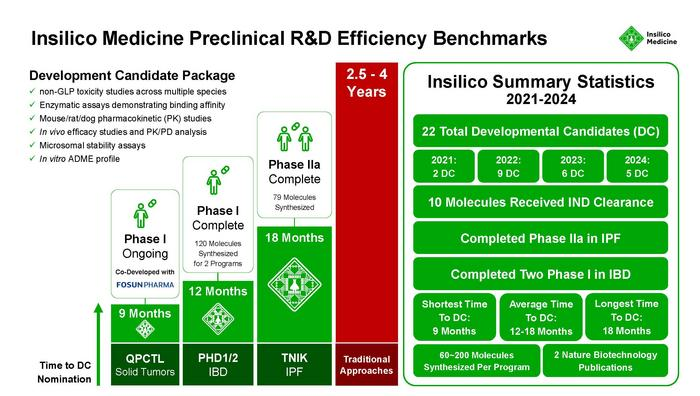
更为惊世骇俗的是,从AI系统正式启动靶点运算,到完成临床前候选药物(PCC)的所有验证,并最终将该药物推向首次人体试验(FIH),整个跨度仅仅耗时约18个月,且总资金消耗控制在令人难以置信的数百万美元级别。回想一下前文A.D. Little报告中记载的,1990年代传统药企平均需要31个月以上才能走完的FS-to-FIM泥泞之路 ,在AI大语言模型与干湿实验室融合的加持下,时间仿佛被折叠了。
3. 自动化武装的“未来实验室”与数字终点
算力狂飙的终极载体,是彻底消除实验室人力执行瓶颈的硬件革命。根据德勤(Deloitte)2024年的高阶洞察报告,受制于全球宏观经济的通胀压力、临床试验极度复杂的招募环境以及新一轮高价值资产专利到期的悬崖逼近,大型药企正面临前所未有的提升研发投资回报率(IRR)的生存压力。
在这一背景下,不惜重金打造高度自动化的“未来实验室”已成为巨头们的共同选择。通过部署超高通量化学反应筛选阵列(HTE)、24小时无人值守的全自动结晶筛选机械臂以及贯穿全局的云计算数据管理中台,企业能够在几天之内自动跑完上万个反应条件,瞬间收集以往需要大批人工耗费数月才能积累的溶解度曲线、多晶型相图及工艺稳健性海量数据。
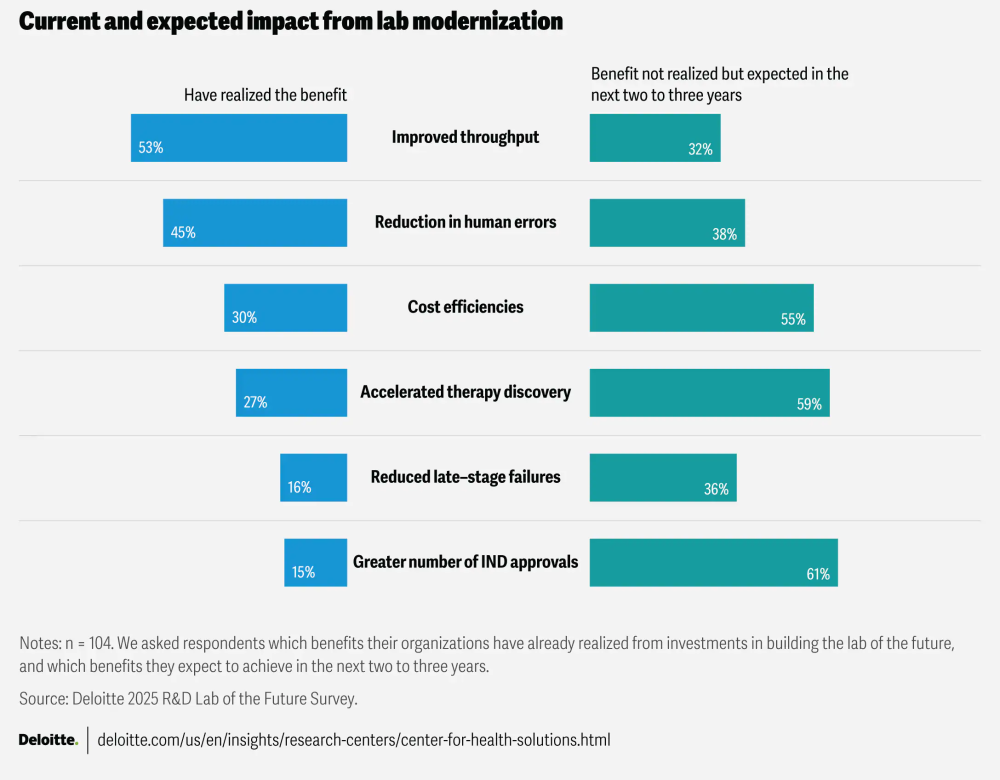
数字化复利可重塑研发深度与速度
不仅如此,结合塔夫茨中心(Tufts CSDD)2024年披露的最新数字型终点(Digital endpoints)临床策略,通过可穿戴设备实时捕获一期临床受试者的生理参数,研发团队甚至可以在IND申报正式获批前,就凭借无懈可击的全维度CMC数据包与数字孪生(Digital twin)模拟器,建立起必胜的信心。这种软硬件的极致结合,彻底夯实了早期开发协调团队(DCT)的火力底座,令新药驶入临床的每一个环节都严丝合缝。
结语
回顾半个世纪的研发史,药物发现向开发的过渡,已经从简单粗暴的“把化合物扔过墙”演变为了高度精密的跨学科系统工程。
无论是在BMS这样的大型跨国药企,还是在依靠CRO驱动的初创Biotech,并行前置、跨界整合、底层工艺创新 始终是压缩 FS-to-FIM 时间线的核心法则。在新药研发这场与时间的惨烈赛跑中,只有那些能够将“化学复杂性”转化为“工程执行力”的团队,才能真正跨越死亡之谷,将前沿的分子科学转化为造福患者的临床曙光。
扩展阅读:
1. 深度解析原料药(API)的早期工艺开发:从“科学发现”到“临床验证”的破局之路
2. 新药研发全景图:从分子发现到临床确证,再到上市后监测的挑战
3. 新药研发密码:构效循环、利平斯基五规则与PROTACs新范式大揭秘
查数据,找摩熵!想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论