这样一块高速增长的“肥肉”,自然引来无数仿制玩家。截至目前,除原研艾伯维外,尚无本土企业成功冲线;但在CDE,已有超过40家企业按仿制4类递交了上市申请,包括石家庄四药、齐鲁制药(海南)、海南合瑞制药、重庆圣华曦药业等,抢仿之势可谓白热化。
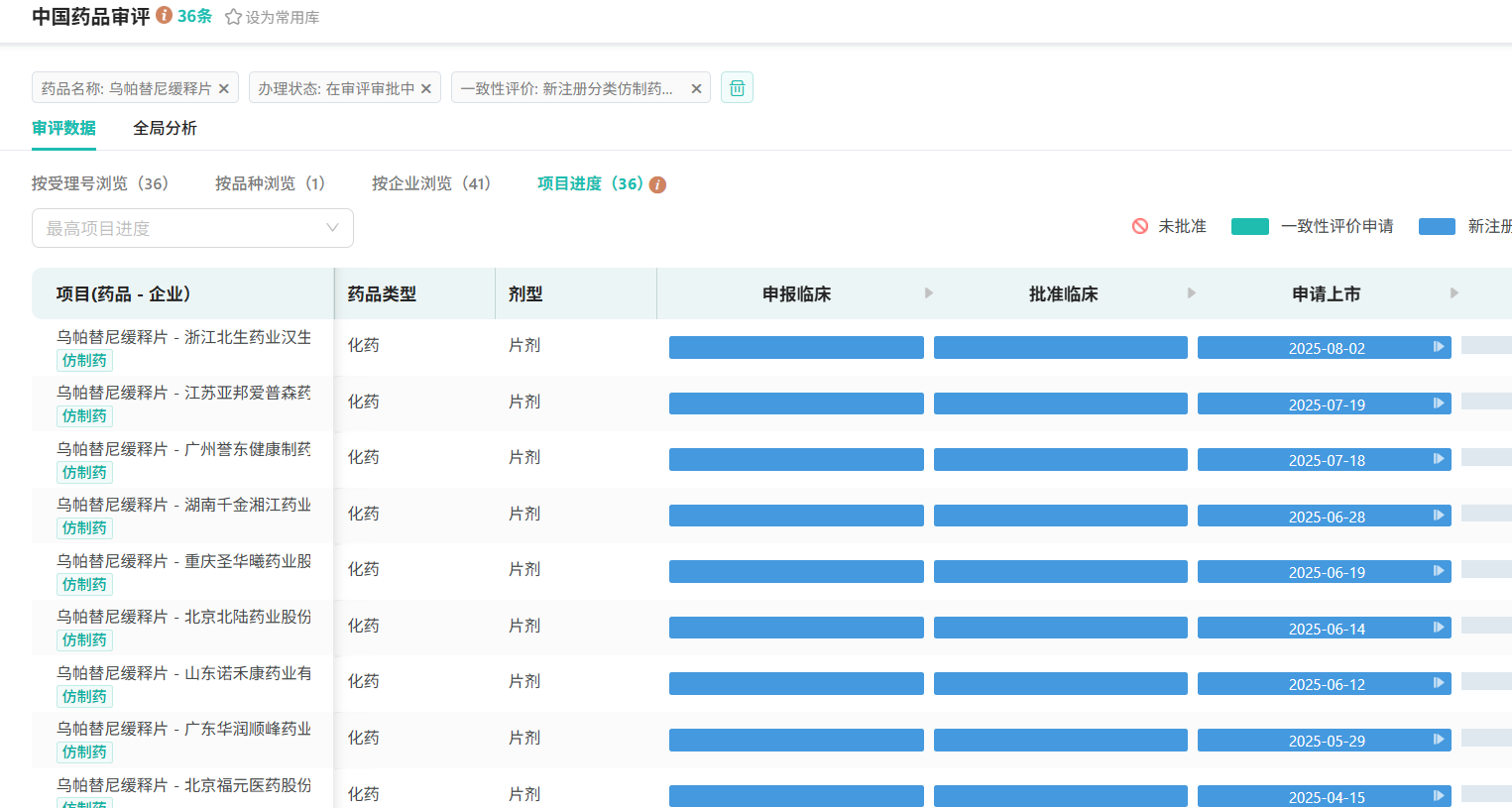
查数据,找摩熵!图源:摩熵医药-中国药品审批数据库
二、专利墙倒了,技术墙还在
过去,乌帕替尼 在中国市场的仿制难点之一是专利——核心化合物及组合物专利原定2030年才到期。但2022年底,四川国为率先发起专利挑战,直击化合物专利。

查数据,找摩熵!图源:摩熵医药-全球上市药品专利数据库
2023年7月,国家知识产权局一锤定音:化合物专利被宣告全部无效,组合物专利也被削去大半。专利壁垒轰然倒塌,仿制大军瞬间蜂拥而上。
然而,专利只是第一道关,技术门槛依旧高企。
从参比制剂看,国内收载了三个来源:
- 国内上市原研(15/30/45mg)
- 欧盟上市(45mg)
- 美国上市(15mg)
原料药端,转A状态的仅有天地恒一、四川国为两家,另有20余家仍在审或未过评。
真正的“拦路虎”,出现在BE(人体生物等效性)试验策略上。
三、复星万邦的“翻车”样本:BE豁免不是万能钥匙
复星万邦 此番申报覆盖了15mg、30mg、45mg三个规格,但仅在45mg大规格做了BE试验,对两个小规格直接申请豁免。
结果很干脆:15mg、30mg规格的上市申请仅启动了药学和临床药理审评,没等到发补环节即被拒。审评逻辑很清晰——在没有充分BE证据的情况下,小规格的安全有效性无法确认,豁免请求不成立。
这相当于给所有寄望“用小规格BE豁免换时间和成本优势”的玩家泼了一盆冷水:在大品种、复杂制剂面前,监管并不会因为专利已破就放宽技术要求。
结语
复星万邦的失利,不是孤例,而是当下抢仿大战的一个缩影:专利可以攻破,但科学规律无法绕行;市场规模再诱人,也抵不过一次不够严谨的试验设计。
乌帕替尼缓释片的四连败提醒所有仿制药企:
靠“抢跑”和“豁免”博首仿的时代正在退场,未来的竞争,拼的是从原料到制剂、从药学到临床的全链条硬核能力。
当审评员只凭数据和标准判卷时,你的BE试验够不够扎实、工艺能不能一次做对,才是决定能否在黑匣子里脱颖而出的唯一答案。
毕竟,不管审评员叫什么名字,严谨的科学标尺,永远不会因一次电话或一份“巧妙”的豁免申请而倾斜。
参考来源:
[1] CDE/NMPA官网
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 60亿美金大单品乌帕替尼:专利“破局”,35+家药企竞逐首仿,石家庄四药新入场
2. 乌帕替尼缓释片全球60亿销售额耀眼,原研独占国内市场将破?九华华源等25+药企争夺首仿!
3. 自免药物乌帕替尼全球热销近60亿,山东齐都药业等多家药企竞逐国内首仿!
查数据,找摩熵!想要解锁更多药品信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药品各国上市情况、药品批文信息、销售情况与各维度分析、市场竞争格局、一致性评价情况、集采中标情况、药企申报审批信息、最新动态与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!



























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论