
近期,来自中国台湾的上市药企台康生技(6589)(11/12)宣布,继 EG12014 之后再次与国际生物类似药巨头山德士(Sandoz AG; SIX:SDZ/OTCQX:SDZNY)签订第二款自主开发的治疗HER2阳性乳腺癌生物类似药 EG1206A(Pertuzumab Biosimilar to Roche Perjeta®),授权范围为全球独家销售合约(中国台湾、中国大陆、中国澳门、韩国、蒙古、文莱、柬埔寨、印度尼西亚、老挝、缅甸、菲律宾与日本除外)。
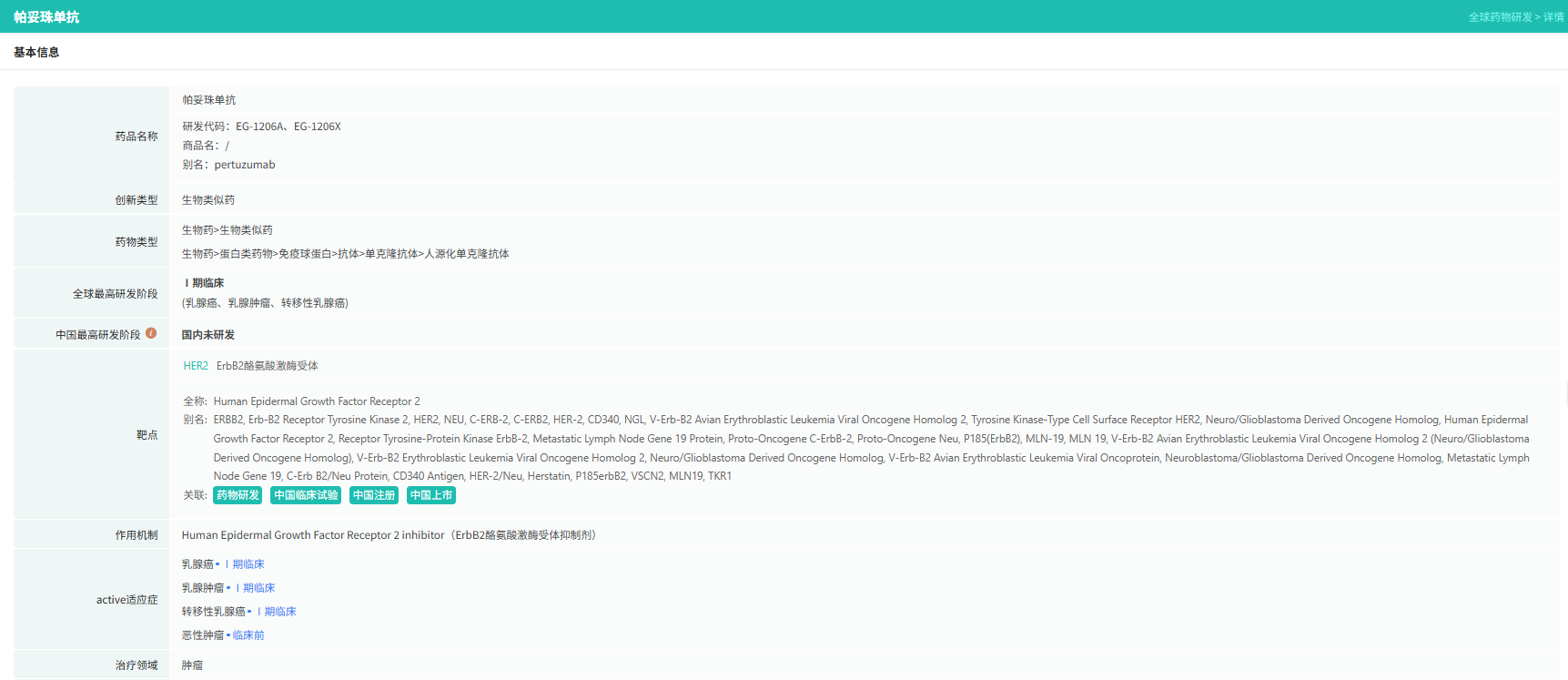
截图来源:摩熵医药数据库-全球药物研发数据库
根据此次BD交易协议约定,台康除可获得总额达1.52亿美元的签约及里程碑(Milestones)金外,还将根据市场销售表现获得销售奖励金(Sales Incentives);同时,在产品上市后,也将享有一定比例的销售分润(Profit Share)。
台康将负责本产品的开发、生产制造及药品供应。
EG1206A(Pertuzumab Biosimilar)已完成临床药代动力学(Pharmacokinetic)临床试验,并于今年10月取得美国食品药品监督管理局(FDA)及欧盟药品管理局(EMA)同意纳入精简开发路径、豁免三期临床比较疗效试验的正面意见。
本次签约是台康生物类似药开发的又一重大里程碑。该协议进一步加强了台康与山德士的伙伴关系,双方此前已签订 EG12014(Trastuzumab Biosimilar含150 mg与420 mg剂型)全球商业化协议。EG12014 也已获欧盟委员会批准,并正在向美国FDA提交上市许可申请(BLA)。
目前全球约有230万乳腺癌患者,其中约20%为HER2阳性患者。
Trastuzumab 联合 Pertuzumab 疗法已成为此类患者标准治疗。近期临床研究显示,Pertuzumab 联合 Trastuzumab deruxtecan(Enhertu®)有望成为HER2阳性转移性乳腺癌患者新的第一线治疗标准。因此,未来 EG1206A 市场将进一步扩大。台康除已推出第一代产品 EG12014 外,一旦第二代产品 EG1206A 上市,将为HER2阳性乳腺癌患者提供更多治疗机会。根据原厂罗氏2024年报数据,Pertuzumab 全球销售额达36.16亿瑞士法郎(约40.03亿美元)。
注明:台康生技EirGenix Inc.最早成立于2012年12月21日。2024年,山德士的净销售额达104亿美元。
参考来源:
[1] NMPA/CDE官网
[2] 摩熵医药(原药融云)数据库
[3] FDA/EMA/PMDA
[4] 中国台湾省股市资讯网
[5] https://zh-tw.eirgenix.com/
扩展阅读:
2. 生物类似药赛道内卷加剧,正大天晴、齐鲁、华东医药等药企之门大开……
3. 石药集团申报乌司奴单抗生物类似药上市获受理,或添银屑病治疗新选择
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论