
11月26日,博安生物发布公告宣布,公司自主研发的 博优景®(阿柏西普眼内注射溶液)正式获得中国国家药品监督管理局的上市批准,用于治疗成人的新生血管(湿性)年龄相关性黄斑变性(nAMD)和糖尿病性黄斑水肿(DME)。
博安生物于2020年与欧康维视达成合作协议,共同开展 博优景® 在中国的Ⅲ期临床试验,并授予欧康维视该产品在中国大陆的独家推广及商业化权利。

博优景®是艾力雅®(英文商品名:EYLEA®)的生物类似药,其活性成分阿柏西普为一种人源化融合蛋白,能够与血管内皮生长因子(VEGF-A、VEGF-B)及胎盘生长因子(PlGF)结合,与抗VEGF单抗类药物相比作用靶点更广泛。作为nAMD、DME等多种眼底疾病的一线用药,阿柏西普对眼内VEGF的抑制时间久,可有效改善视力,具有长期疗效,且总体安全性和耐受性良好。
在全球范围内,EYLEA®已获批的适应症包括:nAMD、DME、视网膜静脉阻塞(RVO)继发黄斑水肿、糖尿病视网膜病变(DR)、近视脉络膜新生血管(mCNV)和早产儿视网膜病变(ROP)。在中国,艾力雅®获批用于治疗nAMD和DME。
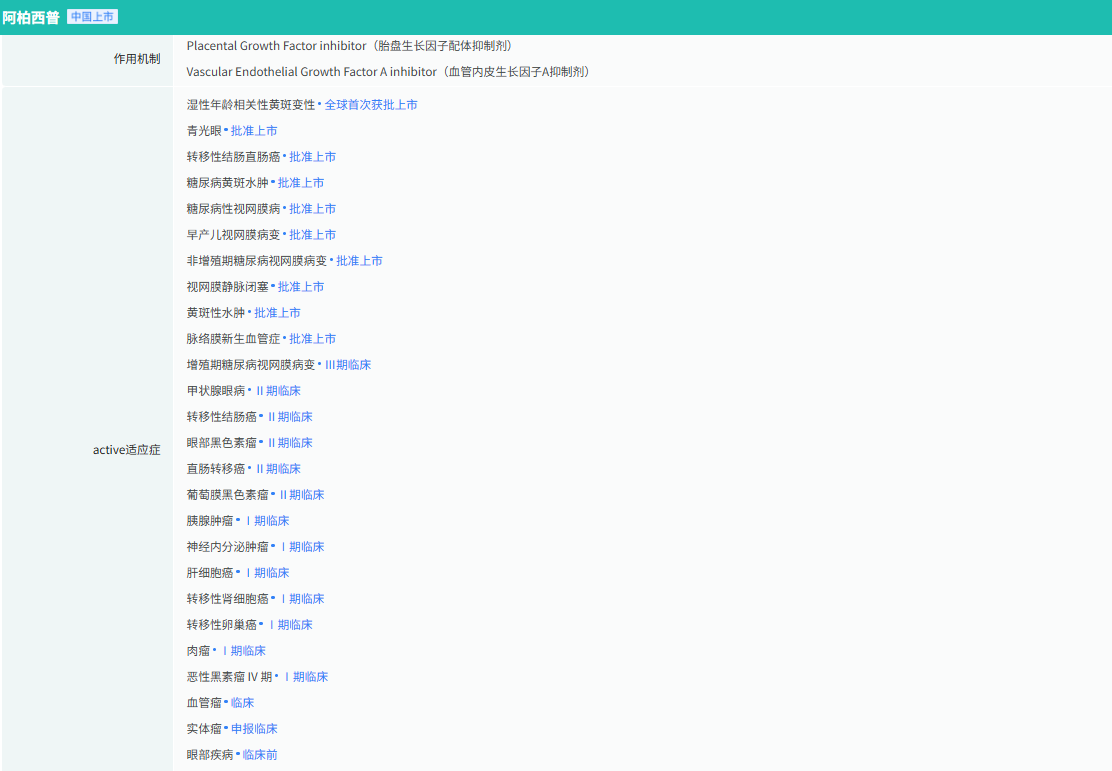
截图来源:摩熵医药数据库-全球药物研发数据库
据悉,博优景®的研发过程严格遵循生物类似药相关指导原则,通过药学、非临床、临床一系列逐步递进的研究,完整而严谨的确证了其与原研药的整体相似性。二者在质量、有效性、安全性和免疫原性上高度相似,无临床意义上的差异。
博优景®的I期临床试验结果显示,博优景®组与原研参照药组的安全性、耐受性一致并可比;Ⅲ期临床试验结果显示,博优景®组与原研参照药组在4周、8周、12周、16周、20周和24周时 “眼最佳矫正视力”(BCVA)均较基线显示出具有临床意义的显著改善(采用ETDRS视力表),疗效高度可比、起效迅速并持久,达到了所有研究终点。
参考来源:
[1] 企业公告
[2] 摩熵医药(原药融云)数据库
扩展阅读:
1. 眼科AAV基因疗法!GenSight三期临床试验积极,被证实具有持久效力
3. 2022年眼科用药TOP10品种出炉!百亿黄金赛道,迎来最新加码
想要解锁更多药物研发信息吗?查询摩熵医药(原药融云)数据库(vip.pharnexcloud.com/?zmt-mhwz)掌握药物基本信息、市场竞争格局、销售情况与各维度分析、药企研发进展、临床试验情况、申报审批情况、各国上市情况、最新市场动态、市场规模与前景等,以及帮助企业抉择可否投入时提供数据参考!注册立享15天免费试用!























































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论