7月中国临床试验进展要点
- 7月CDE新公示临床试验共计312项,生物制品77项,中药/天然药物6项,化学药物共计229项,化药占73%
- 试验药物品种中,奥卡西平片、SHR0302片、替格瑞洛片、非洛地平缓释片和他达拉非片等药物成最热登记品种
- 从临床分期来看,临床I期81项,临床II期35项,临床III期42项, 临床IV期3项,大多数试验处于临床早期阶段
- 从试验状态来看,307项正在进行中,5项试验已完成,其中3项为BE试验
- 新公示BE试验135项,较上月上升42%,浙江诺得药业以7项试验占据BE试验申办单位榜首
- 新公示进口及国内新药167项,诺华、阿斯利康、罗氏等多家企业相关药物处于临床后期
- 江苏恒瑞以11项试验位居临床试验申办单位榜首,北京肿瘤医院成最热试验机构
数据统计时间段为2021年7月1日-2021年7月31日,药融云将定期公示一致性评价过评信息,关注公众号即可定期查看。如有疏漏,欢迎指正!
7月公示312项试验,化药占73%奥卡西平片等药物成最热品种
2021年7月1日至7月31日,CDE新公示临床试验共计312项。从药品类型来看,生物制品77项,中药/天然药物6项,化学药物共计229项,占试验总数的73%,其中包括BE试验134项。
7月新公示临床试验药品分类
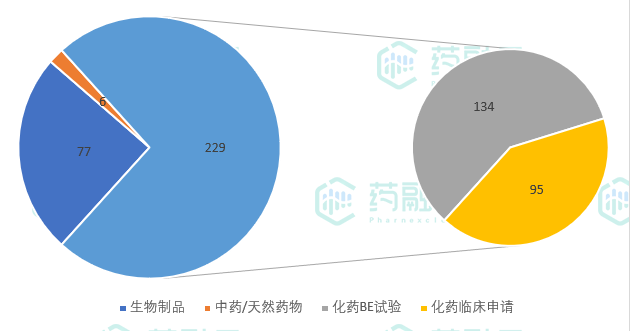
数据来源:药融云中国临床试验数据库
CDE新公示的临床试验药物品种中,共有32个登记试验数≥2的药物品种,其中25项为BE试验品种,奥卡西平片、SHR0302片、替格瑞洛片、非洛地平缓释片和他达拉非片以3个登记试验位居前列。
登记试验数≥3的药物品种

数据来源:药融云中国临床试验数据库
大多数试验处于临床早期3项BE试验已完成
从临床分期来看,临床I期81项,临床II期35项(含I/II期),临床III期42项(含II/III期、I/II/III期), 临床IV期3项,其他试验151项(主要是BE试验)。
7月新公示临床试验分期
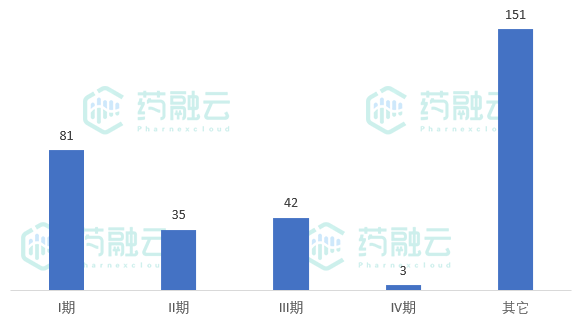
数据来源:药融云中国临床试验数据库
新公示的312项临床试验中,307项正在进行中,5项试验已完成,其中3项为BE试验,涉及浙江九洲生物和宜昌人福药业。
7月新公示临床试验状态
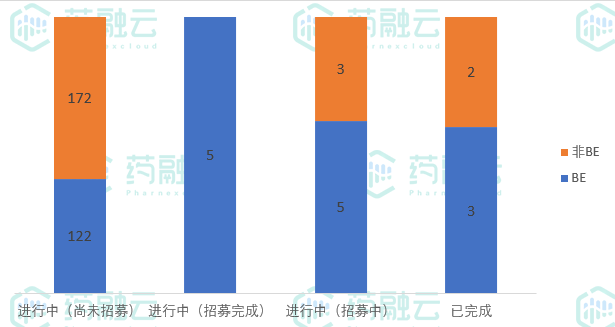
数据来源:药融云中国临床试验数据库
BE试验数较上月上升42%诺得药业申报BE试验最多
7月新公示BE试验135项,较上月(95项)上升42%。浙江诺得药业以7项试验占据BE试验申办单位榜首。
BE试验登记数≥3的申办单位
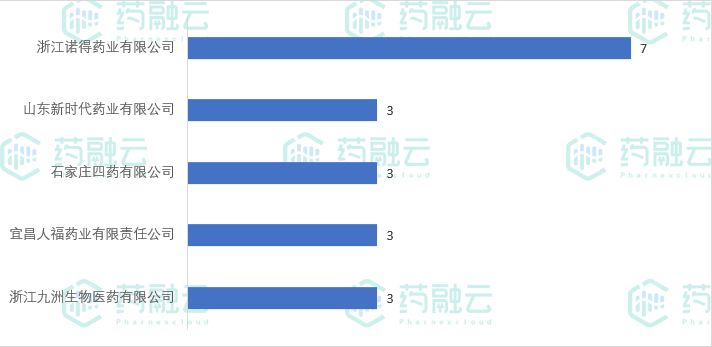
数据来源:药融云中国临床试验数据库
新公示进口及国内新药167项,诺华、阿斯利康等企业相关药物进入临床后期
7月新公示进口药试验40项,其中爱可泰隆医药的马昔腾坦片和默沙东的MK-7684A注射液已进入临床IV期,艾伯维、诺华、阿斯利康、罗氏等共有17款药品进入临床III期。
国内新药试验127项,涉及实体瘤、流感、糖尿病等多个适应症,相比进口药,国内新药仅18%的药物进入临床后期。安科生物的注射用重组人生长激素和北京科兴的23价肺炎球菌多糖疫苗进入临床IV期。另有21款药品进入临床III期,其中不乏15价肺炎球菌结合疫苗、注射用卡瑞利珠单抗、索凡替尼等热门药物。
7月新公示进入III/IV期的进口药试验
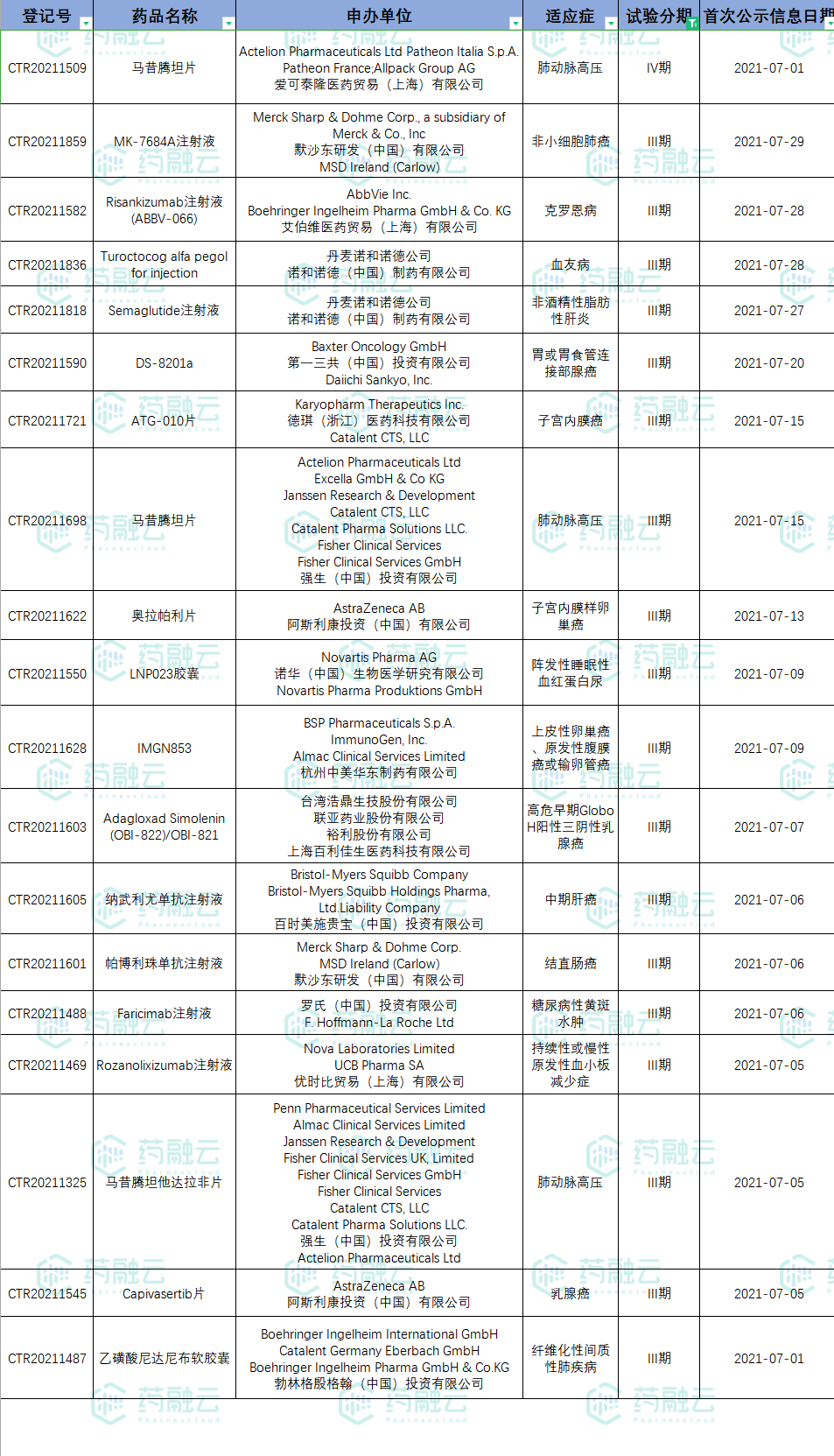
数据来源:药融云中国临床试验数据库
7月新公示进入临床III/IV期的国内新药试验
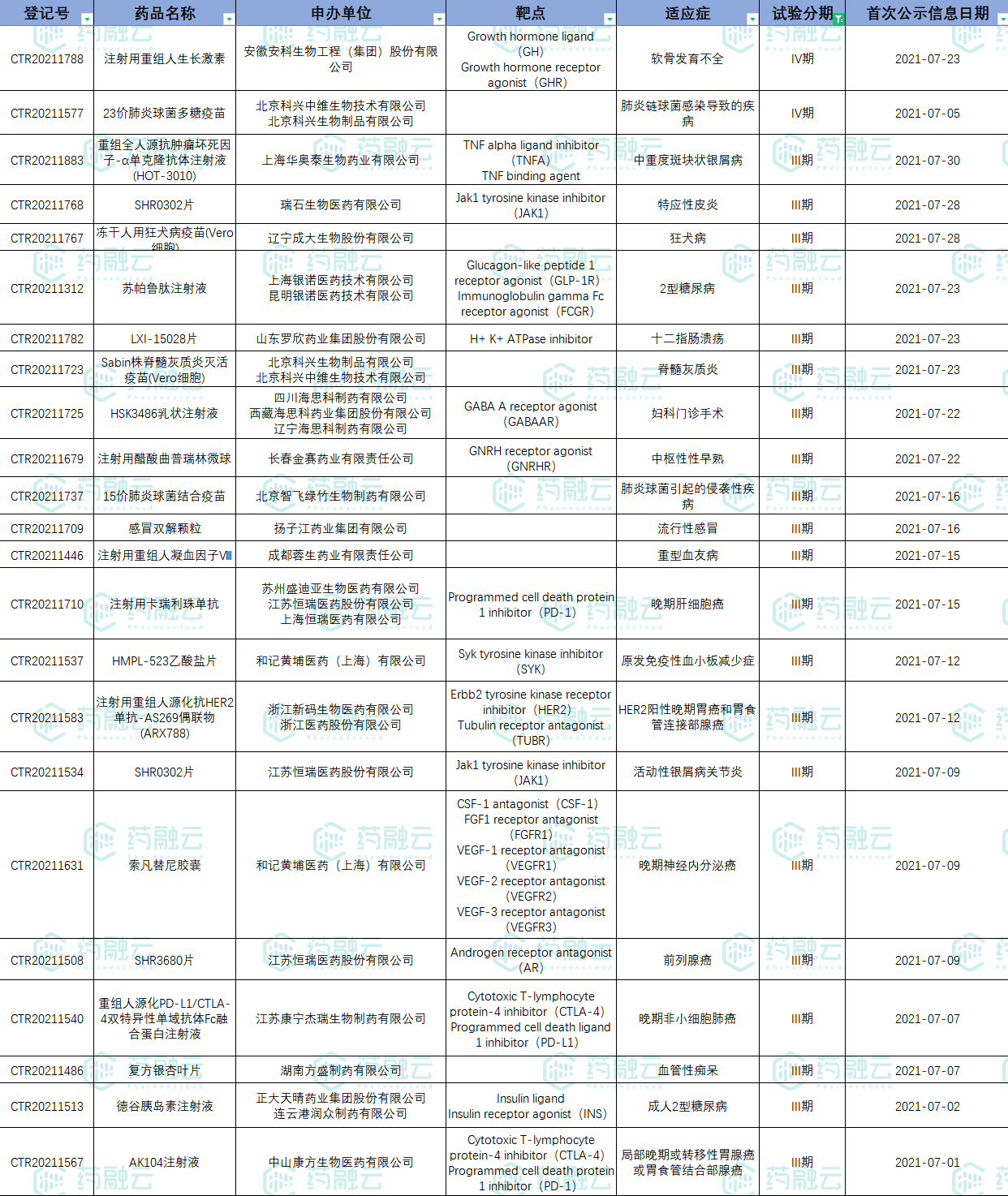
数据来源:药融云中国临床试验数据库
6款重点新药介绍,涉及罗氏、优比时等多家企业
Faricimab注射液
申办药企:罗氏
Faricimab 是罗氏开发的一款同时靶向 VEGF 和 Ang2 的双特异性抗体,是专门为玻璃体内注射而设计的首个双特异性抗体。该候选药可在抑制 VEGF 活性的同时,还可通过抑制 Ang2 活性来改善血管稳定性,降低视网膜炎症。目前,罗氏正在开发 Faricimab 用于治疗湿性年龄相关性黄斑变性(AMD)、糖尿病性黄斑水肿(DME)等适应症,并已进入到 III 期临床阶段。根据罗氏早前公布的数据,在治疗糖尿病性黄斑水肿患者的2期临床试验中,与活性对照相比,faricimab显著改善了患者的视力。
Rozanolixizumab注射液
申报企业:优比时
Rozanolixizumab是一款靶向新生儿Fc受体(FcRn)的“first-in-class”疗法,为人源化单克隆抗体,具有高亲和力。该产品旨在减少致病性免疫球蛋白G(IgG)抗体,阻断IgG再循环过程。FcRn受体的作用是防止IgG的降解,因此通过防止IgG与FcRn的结合,能够导致介导自身免疫性疾病的IgG抗体更快耗竭,从而减轻疾病症状。
Capivasertib片
申报企业:阿斯利康
Capivasertib(AZD5363)是由阿斯利康开发的一款高选择性口服小分子AKT抑制剂。PI3K/AKT/mTOR是细胞内重要的信号通路之一,在调节细胞生长、运动、存活、代谢和血管生成过程中起着重要作用。然而,PI3K/AKT/mTOR通路的过度激活不仅会导致肿瘤的发展,还会引起耐药性的产生。在乳腺癌、结直肠癌和血液癌症等几乎所有的人类癌症中,几乎都存在PI3K/AKT/mTOR通路失调的现象。
乙磺酸尼达尼布软胶囊
申报企业:勃林格殷格翰
尼达尼布(Nintedanib)是一种口服小分子酪氨酸激酶抑制剂,通过竞争性抑制成纤维细胞生长因子受体(FGFR 1-3)、血管内皮生长因子受体(VEGFR 1-3)、血小板源性生长因子受体(PDGFR α和β)等受体酪氨酸激酶,阻断对成纤维细胞的增殖、迁徙和转换起关键作用的信号传导,从而抑制肺纤维化病变。
AK-104注射液
申报企业:康方生物
AK104是康方生物自主研发的新型的、潜在下一代首创PD-1/CTLA-4 双特异性肿瘤免疫治疗药物,旨在实现与肿瘤浸润淋巴细胞(TIL),而不是正常外周组织淋巴细胞的优先结合。AK104同时靶向两个经过验证的免疫检查点分子:程序性细胞死亡蛋白1(PD-1)及细胞毒性T淋巴细胞相关蛋白4(CTLA-4),因此已显示出PD-1及CTLA-4单克隆抗体联合疗法的临床疗效以及PD-1和CTLA-4单克隆抗体联合疗法无法提供的良好安全性。
司美格鲁肽注射液
申报企业:诺和诺德
司美格鲁肽是一款人胰高血糖素样肽-1(GLP-1)类似物,以葡萄糖浓度依赖性机制促胰岛素分泌并抑制胰高血糖素分泌,可使2型糖尿病患者血糖水平大幅改善,并且低血糖风险较低。每周只需给药一次,安全强效降糖的同时兼顾心血管代谢综合获益。
江苏恒瑞申办11项试验,北京肿瘤医院成最热试验机构
临床试验申办单位中,有6家企业申办登记数超4个,其中江苏恒瑞以11项登记试验位高居榜首。
临床试验机构中,北京肿瘤医院以8项登记试验位列第一,华西医院、复旦大学附属中山医院以7项登记试验紧随其后。
7月临床试验登记数≥4的申办单位
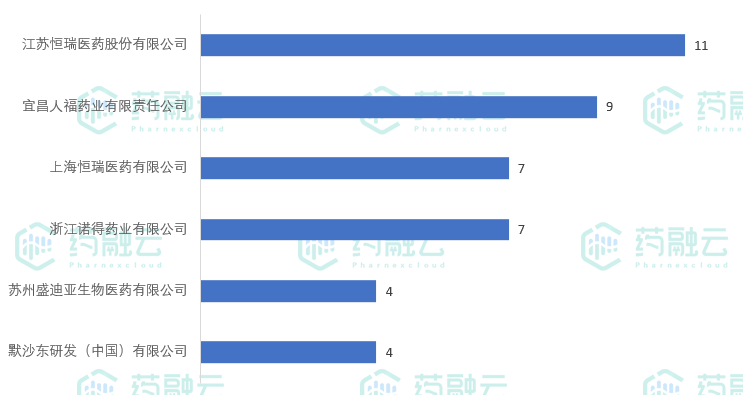
数据来源:药融云中国临床试验数据库
7月临床试验登记数≥4的试验机构
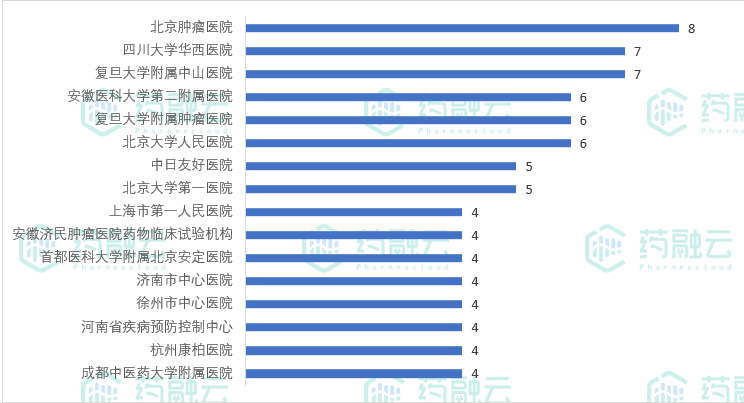
数据来源:药融云中国临床试验数据库






















































 川公网安备51019002008863号
川公网安备51019002008863号 本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
本网站未发布麻醉药品、精神药品、医疗用毒性药品、放射性药品、戒毒药品和医疗机构制剂的产品信息
收藏
登录后参与评论
暂无评论